 |
Квантовая теория строения атома
|
|
|
|
Химия
Часть I. Общая химия
Государственное бюджетное образовательное учреждение
высшего профессионального образования
«Северный государственный медицинский университет»
Министерства здравоохранения Российской Федерации
Северный научный центр РАМН
Химия
Часть I. Общая химия
Методические рекомендации
Архангельск
Печатается по решению центрального координационно-методического совета Северного государственного медицинского университета
Авторы-составители:
Е.А. Айвазова, кандидат биологических наук, заведующая кафедрой общей и биоорганической химии СГМУ; Е.А. Журавлева, кандидат биологических наук, доцент кафедры общей и биоорганической химии СГМУ; Т.А. Корельская, кандидат химических наук, доцент кафедры общей и биоорганической химии СГМУ; Г.П. Суханова, кандидат технических наук, доцент кафедры общей и биоорганической химии СГМУ; Н.А. Матонина, старший преподаватель кафедры общей и биоорганической химии СГМУ; Д.Р. Гамыркина, ассистент кафедры общей и биоорганической химии СГМУ.
Рецензенты:
И.А. Крылов, доктор медицинских наук, заведующий кафедрой фармакологии СГМУ;
М.В. Никитина, кандидат химических наук, доцент кафедры химии ИЕНБ САФУ им. М.В. Ломоносова.
Методические рекомендации содержат материал по основным разделам общей химии и предназначены для самостоятельной работы студентов лечебного, педиатрического, стоматологического факультетов и медико-профилактического отделения факультета медицинской профилактики и экологии. В каждом разделе содержится теоретический материал, вопросы и задания для самоподготовки.
Могут быть полезны студентам других факультетов медицинских ВУЗов, учителей гимназий, лицеев и школ с углубленным изучением химии.
|
|
|
© Северный государственный
медицинский университет, 2015
ВВЕДЕНИЕ
Для успешного усвоения знаний в смежных дисциплинах студент медицинского ВУЗа должен хорошо усвоить теоретические основы химии. Этому несомненно способствует решение логических и расчетных задач, касающихся основных разделов общей химии: строение атома, химическая связь, термодинамика, кинетика, физико-химические свойства растворов.
Решение задач является важнейшим средством формирования химического мышления, одним из путей осуществления связи теории с практикой, практического применения полученных знаний. Велика и развивающая функция решения задач: формирование рациональных приемов мышления и устранение формализма знаний, развитие самостоятельности.
Данные методические рекомендации соответствуют программе по химии лечебного, педиатрического, стоматологического факультетов и факультета медицинской профилактики. В каждом разделе представлено краткое теоретическое введение, облегчающее понимание основных положений изучаемой темы, приведены вопросы и задания для самостоятельного решения.
РАЗДЕЛ I. Строение атома и химическая связь
Актуальность
Все разнообразие объектов живой и неживой природы состоит из атомов тех или иных химических элементов. Наблюдаемые свойства различных веществ окружающего мира (способность к окислению, восстановлению, комплексообразованию, диссоциации, гидролизу, растворимости и т.д.) в итоге определяются строением электронных оболочек атомов, образующих данное соединение. Однако, свойства веществ определяются не только строением их атомов, качественным и количественным составом, но и внутренней структурой молекул, типом химических связей между атомами, их образующих. От типа данных связей и их свойств зависит скорость и направление протекания реакций.
|
|
|
Знание материала данной темы необходимо для изучения строения и свойств различных неорганических и органических биологически активных соединений.
Цель: сформировать современные представления о строении атома, природе химической связи и её влиянии на строение и свойства химических соединений.
Строение атома
Атом – это электронейтральная частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов.
Атом – это наименьшая частица химического элемента, сохраняющая все его химические свойства.
Химический элемент – совокупность атомов с одинаковым зарядом ядра. Атомы данного элемента характеризуются одинаковыми свойствами.
Квантовая теория строения атома
Электрон в атоме может находиться только во вполне определенных состояниях. При переходе электрона из одного состояния в другое энергия поглощается или выделяется порциями – квантами энергии.
В 1913 г. Нильс Бор предложил квантовую теорию строения атома водорода, которая была основана на следующих постулатах:
1) в изолированном атоме электрон движется по круговым стационарным орбитам, на которых он не излучает и не поглощает энергии. Каждой такой орбите соответствует определенное значение энергии (E1, E2, E3,…n), где n– целое число, отвечающее возможному стационарному состоянию;
2) переход электрона из одного стационарного состояния (E2) в другое (E1) сопровождается испусканием кванта монохроматического (λ = const) излучения с частотой 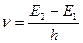 .
.
|
|
|


