 |
Строение различных видов костной ткани. Строение кости как органа
|
|
|
|
ГРУБОВОЛОКНИСТАЯ КОСТНАЯ ТКАНЬ. Наиболее распространена в эмбриональном периоде как провизорная костная ткань. У взрослых особей она сохраняется в области швов черепа, в местах прикрепления сухожилий к кости, возникает при заживлении переломов. Состоит эта ткань из клеток и межклеточного вещества. Преобладающими клетками являются остеоциты, которые лежат в костных полостях — лакунах — и имеют длинные отростки, которыми контактируют друг с другом. Межклеточное вещество образовано коллагеновыми (оссеиновыми) волокнами и основным веществом. Основное вещество минерализовано, в его составе уменьшено содержание гликонротеинов и повышено содержание лимонной и других кислот, образующих связи с кальцием. Снаружи кость покрыта надкостницей, состоящей из фиброзного и камбиального слоев. В камбиальном слое содержатся остеобласты. Механические свойства грубоволок-нистой костной ткани по сравнению с пластинчатой снижены, поэтому в ходе эмбриогенеза и при регенерации она закономерно замешается пластинчатой костной тканью. Грубоволокнистая костная ткань может возникать в патологических условиях мри резкой периодической активации остеобластов неизвестной этиологии (болезнь Педжета).
|
ПЛАСТИНЧАТАЯ КОСТНАЯ ТКАНЬ. Пластинчатая костная ткань — это наиболее распространенный вид костной ткани. Из нее построен весь скелет человека. Она состоит из костных пластинок, структурно-функ- циональных единиц этой разновидности костной ткани. Каждая костная пластинка, в свою очередь, состоит из клеток остеоцитов и межклеточного вещества. Коллагеновые волокна в пластинках имеют параллельное расположение, при этом их направление в соседних пластинках противоположное. Данное обстоятельство обеспечивает прочность кости. Строение дентинной костной ткани см. выше.
|
|
|
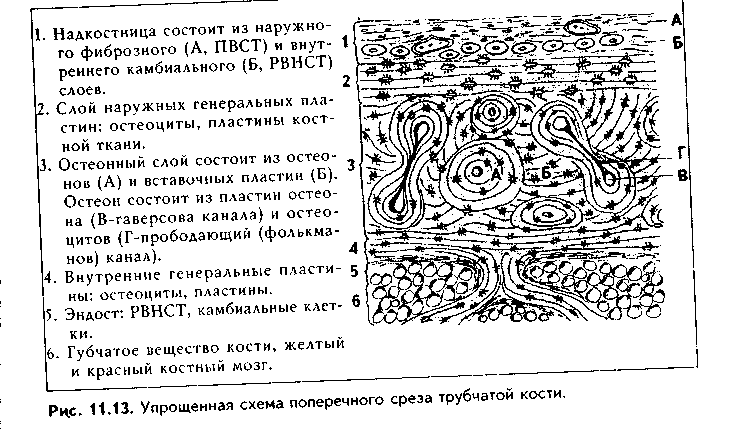
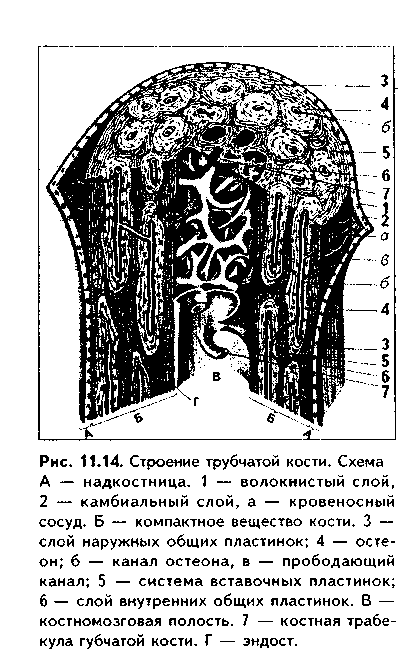
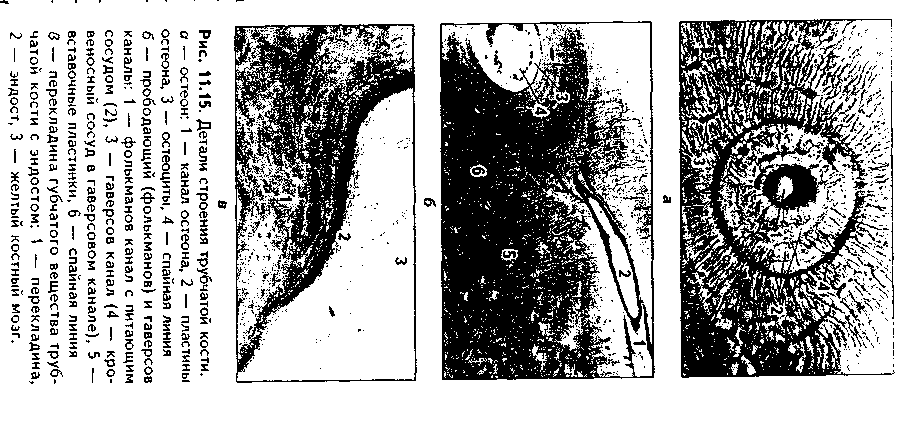
СТРОЕНИЕ КОСТИ КАК ОРГАНА. Пластинчатая костная ткань является основной тканью, из которой построены кости скелета. Как органы кости содержат также и другие ткани: плотную и рыхлую волокнистые, жировую, нервную (нервные волокна и окончания). Кость имеет собственную систему кровоснабжения и лимфообращения. Разберем строение кости как органа на примере трубчатой кости (рис. 11.13, 11.14, 11.15).
Трубчатая кость состоит из диафиза и двух эпифизов. Она построена из пластинчатой костной ткани. Лишь в местах костных бугорков есть грубоволокнистая костная ткань. В кости выделяют компактное, с плотным расположением пластин (занимает 80%), и губчатое, с рыхлым, сете-видным расположением пластин, вещество (20% всей кости). Компактное вещество имеет высокую прочность, более низкий уровень метаболизма, в связи с чем обновляется медленнее и меньше подвержено возрастным изменениям. Губчатое вещество формирует трехмерную сеть анастомозирую-щих друг с другом трабекул, в состав которых входят костные пластины. Общий их объем в 10 раз больше объема компактной кости, а площадь достигает 10 м2. Между пластинами находятся остеоциты, количество которых существенно превышает таковое в компактной кости. Трабекулы губчатой кости создают каркас на котором располагается костный мозг. Губчатая кость мета болически высокоактивна, быстро обновляется и чаще, чем компактная, подвергается патологическим изменениям. Е< роль в поддержании мииераль ного гомеостаза более значительна. Вместе с тем, благодаря своей архитектонике губчатая кость обладает достаточно высокой прочностью.
|
В диафизе кости отчетливо выделяются следующие слои:
1. Надкостница, в которой имеются свои два слоя: наружный фиброзный и внутренний камбиальный. Наружный слой образован плотной волокнистой неоформленной, внутренний — рыхлой волокнистой неоформленной соединительной тканями. Надкостница выполняет функции: 1) опорно-механическую — связывает компактное вещество кости с окружающими тканями; 2) трофическую — содержит кровеносные сосуды, которые под прямым углом прободают кость и осуществляют ее питание; 3) регенераторную — в камбиальном слое содержит остеогенные клетки (периваскулярные клетки), при необходимости превращающиеся в активные остеобласты. В надкостнице содержатся также предшественники остеокластов. Благодаря надкостнице осуществляется аппозиционный рост кости (в отличие от хряща кость способна расти в толщину только за счет аппозиционного роста). Надкостница плотно прикрепляется к компактной кости при помощи коллагеновых волокон, входящих в нее под прямым углом из слоя наружных генеральных пластин (шарпеевские волокна).
|
|
|
2. Слой наружных генеральных пластин. Располагаются параллельно друг другу и окружают диафиз по окружности (не полиостью). Между пластинами и лакунах лежат остеоциты.
3. Остеонный слой. В этом слое есть два основных образования: остео-ны и вставочные пластины. Каждый остеон — это структурно-функциональ-ная единица кости. Он состо- I ит из канала остеона (гавер- U сова канала), и котором ле- в жат кровеносные сосуды (арте- к риола, венула или капилляр), | питающие участок кости. Вок- | руг сосудов находится пери- § васкулярное пространство, | заполненное РВНСТ и жиро- | вой тканью. Вокруг сосудов располагаются остеогенные (пе-риваскулярные) клетки и остеокласты. Снаружи от канала остеона лежат пластины остеона, между которыми в лакунах находятся остеоциты. Наружной границей остеонов является спайная (цементирующая) линия, имеющая толщину до 2 мкм, практически лишенная волокон и представленная основным веществом. Строение остеона отражает ход его образования: активированные остеобласты последовательно, вокруг сосуда, синтезируют межклеточное вещество. Так создаются концентрические пластины, а остеобласты превращаются в остеоциты. Между остеонами лежат вставочные пластины. Это остатки старых, разрушающихся остеонов.
|
|
|
|
4. Слой внутренних генеральных пластин. Имеют строение, сходное с наружными генеральными пластинами.
5. Эндост, или внутренняя надкостница. По строению аналогична надкостнице, однако тоньше ее. В эндосте также содержатся остеогенные клетки и остеокласты.
Кроме каналов остеона, или гаперсовых каналов, в кости есть фолькма-новы, или прободающие каналы. Они идут из надкостницы перпендикулярио диафизу кости и содержат питающие кровеносные сосуды. При пом о щи фолькмановых каналов часто соединяются несколько гаверсовых кап.! лов, которые имеют направление, параллельное диафизу. Все вещество кости пронизано системой канальцев, в которых лежат отростки остеоцитоп. Эти канальцы связывают друг с другом лакуны, в которых лежат остеоциты, i: единую лакунарно-канальцевую систему кости. Вместе с системой га версовых и фолькмановых каналов эта система формирует мощную транс-портно-эвакуаторную дренажную систему кости, обеспечивающую транспорт к ее структурам и от них питательных веществ, метаболитов и газов, а также минеральных веществ. Как отмечалось, в работе этой системы важная роль принадлежит подвижным отросткам остеоцитов.

|
ГИСТОГЕНЕЗ КОСТНЫХ ТКАНЕЙ
Источником развития костных тканей является склеротомная мезенхима. Различают два способа развития костной ткани: прямой остеогистоге-нез, или развитие костной ткани непосредственно из мезенхимы, и непрямой остеогенез, или развитие костной ткани на месте хряща (который также первоначально образуется из мезенхимы).
ПРЯМОЙ (МЕМБРАНОЗНЫЙ) ОСТЕОГЕНЕЗ (рис. 11.16). Он состоит из нескольких стадий.
1. Стадия образования остеогенного островка. В месте образования кости мезенхимные клетки теряют отростки, округляются, цитоплазма их становится базофильной. Клетки делятся митозом и образуют клеточные скопления — остеогенные островки. Одновременно из окружающей мезенхимы образуются кровеносные сосуды, и островок обильно кровоснабжает-ся (рис. 11.16 я).
|
|
|

|
2. Стадия остеоида, или первичной костной ткани (остеоид показан на рис. 11.16 б). В эту стадию мезенхимные клетки дифференцируются в остеобласты, которые начинают продуцировать межклеточное вещество. Образуются оссеиновые волокна и гликозаминогликаны, протеогликаны и гликопротеины.
3. Стадия кальцификации, или минерализации межклеточного вещества. Осуществляется за счет деятельности остеобластов. Механизмы минерализации кости описаны выше. Образуются фосфаты кальция, которые соединяются вместе и формируют кристаллы гидроксиапатита. В итоге формируется грубоволокиистая костная ткань.
4. Стадия перестройки грубоволокнистой костной ткани в пластинчатую. В эту стадию активируются остеокласты, которые разрушают участки грубоволокнистой костной ткани (рис. 11.16 в, г). В участки разрушения (лакуны Хаушипа) прорастают кровеносные капилляры, вокруг которых концентрируются активные остеобласты, формирующие пластины остеона.Постепенно вся грубоволокнистая кость разрушается, а на ее месте образую i ся остеоны, т.е. развивается пластинчатая костная ткань. Из окружающей мг зенхимы образуется надкостница с двум'я слоями. Она обеспечивает регеж рацию и питание кости. Формируются также наружные и внутренние rem ральные пластины.
5. Стадия возрастных и функциональных изменений костной ткани.! эту стадию происходит постоянное разрушение стареющих и образовашк новых остеонов.
НЕПРЯМОЙ (ЭНДОХОНДРАЛЬНЫЙ) ОСТЕОГЕНЕЗ. Этот вил остеогенеза характерен для всех костей скелета. Он также протекает и несколько стадий (рис. 11.17, 11.18).

|

|
1. Стадия образования хрящевой модели будущей кости.
Из мезенхимы но общим механизмам хондрогенеза (см. хрящевую ткань) образуется гиалиновый хрящ, который формирует модель кости с диафизом и эпифизами. За счет постоянного деления хрящевых клеток в надхрящнице эта модель увеличивается в размерах и принимает форму будущей кости.
2. Стадия развития пери-хондральной костной манжетки и начала эндохондрального окостенения. В эту стадию надхрящница хрящевой модели постепенно превращается в надкостницу, которая богато васкуляризуется и в которой образуются остеобласты с выраженной активностью щелочной фосфатазы. Они продуцируют межклеточное вещество кости, которое минерализуется. Так образуется перихондральная костная манжетка, состоящая из грубоволокиис-той костной ткани (рис. 11.18 а). Она называется зоной перихонд-рального окостенения, которая есть только в диафизе. С образованием костной манжетки она нарушает питание хряща, лежащего кнутри, отсекая его от сосудов надкостницы. В результате хрящ в этих зонах начинает разрушаться. В нем появляются вакуолизированпые (пузырчатые) хондроциты. Однако достаточно быстро из надкостницы внутрь хряща по каналам, образованным в костной манжетке остеокластами (иногда их называют хондрок-ластами) врастают кровеносные капилляры, вместе с которыми мигрируют остеобласты. Остеобласты начинают синтетическую деятельность и образуют остеоны пластинчатой кости взамен разрушающегося хряща. Так формируется зона эндохондрального окостенения, или эндохондраль-ная кость (рис. 11.18 б). Образовавшись в центральной части диафиза, oh.i распространяется в сторону эпифизов. В отличие от перихондралыюй кос ти, эндохондральная кость сразу формируется как пластинчатая кость.
|
|
|
3. В третью стадию две зоны окостенения — перихондральпая и эпдо хондральная — сливаются вместе. Одновременно перихондральпая кость начинает разрушаться остеокластами и перестраиваться в пластинчатую кость. В эту же стадию хрящ внутри диафиза разрушается, формируете;! костномозговая полость (рис. 11.18 е).

|
В нее заселяются кроветворны' клетки. Образуются наружные и внутренние генеральные пластинки. Ил этой стадии вся костная ткань диафиза представлена пластинчатой костью.
4. Стадия эндохондрального окостенения эпифизов. В предыдущей стадии основные события происходили в диафизе. Эпифизы в это вре-
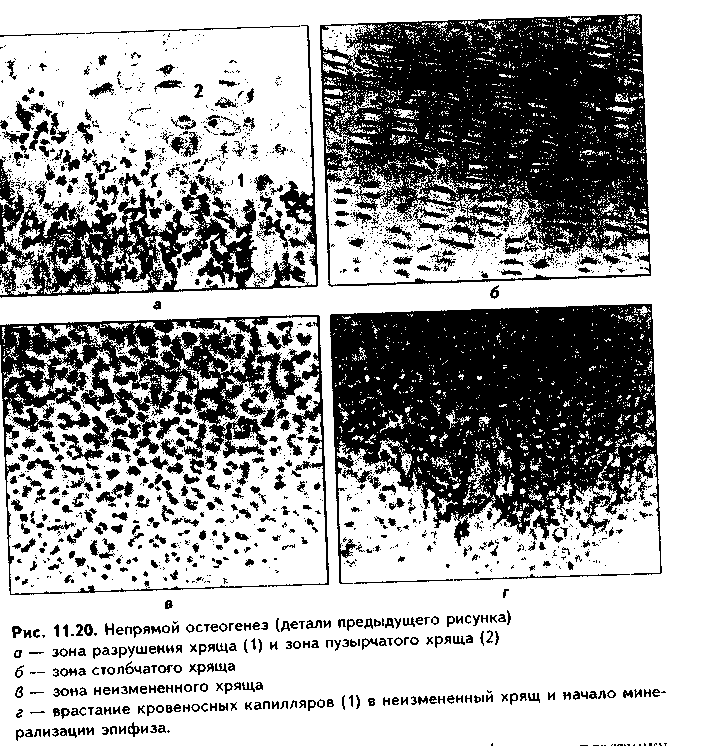
мя состоят из интактной хрящевой ткани. При этом в эпифизах отчетливо выделяются четыре зоны (рис. 11.19, 11.20): 1) периферическая, или зона интактного хряща; 2) зона столбчатого хряща; 3) зона пузырчатого (дегенерирующего) хряща; 4) зона разрушения хряща. В четвертую стадию (вскоре после рождения ребенка) в хрящ эпифиза из окружающей надкостницы врастают кровеносные сосуды, вокруг которых концентрируются остеобласты, продуцирующие и минерализующие межклеточное вещество. Однако эти изменения происходят только в части зоны неизменного хряща. Остальные зоны эпифизарного хряща остаются неминерализованными. Они образуют метаэпифизарную хрящевую пластинку роста, фактически состоящую из четырех описанных выше зон. За счет размножения хрящевых клеток в этой пластинке кость растет в длину, а за счет надкостницы — в толщину.
5. Стадия минерализации метаэпифизарной пластинки роста. В эту стадию (в возрасте 20—25 лет) в метаэпифизарную иллшп^ роста врастают кровеносные ах'уды, а с ними остеобласты, которые образуют межклеточное вещество кости. Оно минерализуется. Теперь вся кость построена из костной ткани.
6. Стадия функциональной и возрастной перестройки кости. Продолжается в течение всей жизни. Суть ее заключается в постоянном разрушении старых и формировании новых остеонов, нарастании их количества и размеров при физической нагрузке и уменьшении при гипокинезии.
РЕГУЛЯЦИЯ МИНЕРАЛИЗАЦИИ КОСТИ И ХРЯЩА. Процесс минерализации кости и хряща находится под строгим контролем организма и зависит от многих факторов. Особенно велика роль эндокринной системы в регуляции образования кости. 1. Гормон паращитовидных желез паратгормон (паратирин) опосредс ванно через остеобласты стимулирует остеокласты, что ведет к резорбции ми нерального и органического компонентов кости и повышению уровня каль ция в крови. Одновременно паратирин подавляет функции остеобластов.
2. Гормон щитовидной и паращитовидных желез кальцитонин оказывает на клетки костной ткани противоположный эффект: тормозит актин ность остеокластов и стимулирует функцию остеобластов. В результат i этого в костной ткани стимулируются процессы остеогенеза.
3. Гормон щитовидной железы тироксин у молодых особей ускоряет образование и созревание новой костной ткани. У пожилых людей он вызывает резорбцию кости.
4. Соматотропин (гормон роста передней доли гипофиза) стимулируем остеобласты, а также деление хрящевых клеток в пластинке роста. Одновременно он подавляет ее минерализацию.
5. Половые гормоны оказывают на развитие кости сложное влияние. С одной стороны, они стимулируют остеобласты, подавляют остеокласты и способствуют росту костей в длину. С другой стороны, резкое повышение содержания половых гормонов в крови при преждевременном половом созревании, вызванном опухолями половых желез и др., ведет к минерализации пластинок роста в костях и низкорослости. При гииогонадизме, напротив, отмечается гигантизм.
6. Кортизол (гормон коры надпочечников) снижает синтез коллагена в костной ткани и способствует развитию остеопороза (уменьшению плотности костной ткани).
7. Гормон кальцитриол (витамин D3) стимулирует поглощение кальция костной тканью, биосинтез органического матрикса кости.
Витамины также играют важную роль в регуляции остеогенеза. Особенно важен витамин С, который стимулирует остеобласты и синтез ими межклеточного вещества кости. Недостаток его (при котором развивается цинга) ведет к дефектам коллагеногенеза и синтеза гликозаминогликанов. Витамин А также стимулирует остеобласты и подавляет остеокласты. При его недостатке нарушается минерализация кости, а при избытке происходит ее резорбция.
РЕГЕНЕРАЦИЯ КОСТНОЙ ТКАНИ. Физиологическая регенерация костной ткани заключается в постоянной перестройке кости. Она призвана не только привести в соответствие строение кости с нагрузками на нее, но и поддерживать минеральный гомеостаз. Осуществляется за счет соче-танной деятельности остеобластов и остеокластов, которые находятся в надкостнице, эндосте и каналах остеонов. В норме большая часть их пребывает в состоянии покоя и активируется при инициации перестройки. Активация остеобластов ведет к одновременной активации остеокластов и наоборот (функциональное сопряжение остеобластов и остеокластов). За счет деятельности этой функциональной пары клеток происходит следующая цепь событий в кости: активация клеток, осуществляющих разрушение кости —> резорбция старой кости -» реверсия (переход от резорбции кости к остеосигенезу) —> остеогенез.
Репаративная регенерация костной ткани происходит после переломов. Осуществляется за счет деятельности остеобластов, формирующихся из остеогенных (периваскулярных) клеток. Регенерация кости протекает в
несколько стадий.
1. Стадия разрушения поврежденных структур кости и деления остеогенных клеток. В эту стадию происходит разрушение поврежденных элементов кости и возникает воспалительная реакция. Одновременно пери-васкулярные клетки превращаются в остеобласты, которые приступают к синтезу межклеточного вещества.
2. Стадия образования и дифференцировки тканевых структур кости. Остеобласты выселяются в место перелома и образуют компоненты межклеточного вещества. Одновременно с образованием остеобластов в силу генетического родства формируются линии фибробластов и хондробластов, причем хондроидная ткань получает преимущественное развитие. В результате формируются соединительнотканная или (чаще) хрящевая мозоли.
3. Стадия первичной костной структуры. Хрящевая (соединительнотканная) мозоль минерализуется и превращается в костную мозоль. Одновременно восстанавливается сосудистая система кости.
4. Стадия окончательной перестройки регенерата. Вначале костная мозоль состоит из грубоволокнистой костной ткани, которая потом заменяется на пластинчатую. Происходит резорбция избытка кости и восстановление костномозговой полости.
Приведенная схема регенерации кости наблюдается при так называемом вторичном костном сращении, когда костные отломки недостаточно сближены и закреплены. Эта ситуация встречается в клинике наиболее часто. При хорошей иммобилизации и репозиции (сопоставлении) отл.омков регенерация происходит более быстро и экономно с незначительным разрушением костной ткани по обе стороны от перелома. При этом практически сразу образуется пластинчатая костная ткань без формирования соединительнотканной и хрящевой мозолей (первичное костное сращение).
Стимуляция регенерации кости. Стимуляция регенерации костной ткани может осуществляться применением анаболических гормонов, витаминов, препаратов ДНК, РНК и др. Она происходит также при введении в зону дефекта костных опилок, а также трансплантации аллогенной кости. Широко используется также применение метода дистракции (растяжения) кости по Г.А. Илизарову (аппарат Илизарова). Метод основан на пьезоэлектрическом эффекте кости: ее растяжение вызывает формирование положительного заряда, а сжатие — отрицательного электрического заряда. К положительному заряду тропны остеокласты, которые при растяжении и,: чинают осуществлять резорбцию костной ткани. Однако в силу coup;! жения функции остеобластов и остеокластов через определенное врем -происходит активация последних и выработка ими межклеточного вещг ства. Повторная дистракцпя ведет к повторению цикла. В результате пси ледовательных дистракций происходит постепенное новообразование и о. зревание костных структур, увеличивается межотломковый костный рек нерат, который в средней части сохраняет соединительнотканную струкг> ру, на основе которой и происходит костеобразование. Этот метод позж ляет, во-первых, эффективно лечить переломы, т.к. аппарат Илизароп. позволяет хорошо сопоставить и иммобилизировать отломки, в результа те очень рано создается возможность включения конечности в функции (нагрузка на нее ведет к активации остеобластов). Во-вторых, метод по зволяет увеличивать длину конечностей для исправления дефектов скелета.
РОСТ КОСТИ. Рост кости в длину происходит за счет метаэпифи зарной пластинки роста. Наблюдается до периода полового созревания после наступления которого половые гормоны способствуют подавлении! митозов клеток и минерализации хряща метаэпифизарной пластинки Рост кости в толщину происходит за счет надкостницы. При этом физический труд способствует размножению клеток в надкостнице, и кость ста новится толще.
ЭКТОПИЧЕСКИЙ РОСТ КОСТИ. Эктопический остеогенез. - это образование кости в нетипичных местах. Наиболее часто он имеет место при дистрофическом обызвествлении омертвевших тканей или тканей, находящихся в состоянии глубокой дистрофии. При этом большое значение имеет ощелачивание среды и увеличение активности щелочной фосфата-зы, выделяемой из погибших клеток. Эктопическое костеобразование мо жет иметь место в оболочках глаза, стенках сосудов, почках, щитовидной железе, сухожилиях, поперечнополосатых мышцах, рубцах: зоне инфаркта миокарда, зонах хронического воспаления и др.
Причины эктопического остеогенеза до конца не исследованы. В условиях эксперимента воспроизвести его до последнего времени было достаточно трудно. Существуют два методических приема для получения эктопической кости: 1) трансплантация в соединительную ткань слизистой оболочки моченого пузыря; 2) трансплантация кусочка кости с убитыми костными клетками.
В настоящее время установлено, что причиной эктопического костеоб-разования является стимуляция при этом выделения индукторов остеогенеза. Такими индукторами являются прежде всего морфогенетические белки кости (МБК). Они способствуют превращению стволовых клеток РВНСТ в остеогениые клетки. В настоящее время эти белки выделены и используются для изучения эктопического остеогенеза. Их введение в РВНСТ вызывает костеобразование.
Эктопический остеогенез имеет существенное клиническое значение, т.к. приводит к нарушению функций органов, в которых происходит, и может явиться причиной смерти.
ВОЗРАСТНЫЕ ИЗМЕНЕНИЯ ХРЯЩЕВЫХ И КОСТНЫХ ТКАНЕЙ. У молодых индивидуумов в костной ткани преобладают анаболические процессы, процессы созидания. В межклеточном веществе отмечается преобладание органического компонента над минеральным. В результате этого кости детей гибкие, меньше подвергнуты переломам, а если таковые имеют место, то происходят поднадкостнично, по тину "зеленой ветки", т.е. без смещения костных отломков. Максимум массы костной ткани достигается примерно к 20—25-ти годам. После этого возраста процессы резорбции костной ткани начинают преобладать над процессами костеоб-разования. С возрастом количество минеральных веществ увеличивается, они преобладают над органическими, что обусловливает повышенную ломкость костей. Этому же способствует остеонороз — разрежение костной ткани при старении. Его развитию способствуют: нарастающая атрофия половых желез и снижение в результате концентрации половых гормонов (особенно эстрогенов, поэтому у женщин часто наблюдается менопаузаль- ный остеонороз); снижение функциональной нагрузки на кость, что ведет к активации остеокластов. У старых людей в результате остеолиза резко увеличивается диаметр гаверсовых каналов, что ведет к уменьшению общей массы костной ткани. Существенно нарушается заживление переломов костей.
Глава 12
МЫШЕЧНЫЕ ТКАНИ
Общая морфофункционалытя характеристика. Мышечные ткани пр«ставляют собой тип тканей, объединенных общей функцией — функцт сократимости. Скелетная мышечная ткань обеспечивает передвижение те.; в пространстве. Гладкая мышечная ткань приводит в движение степ к: внутренних органов и сосудов. Сердечная мышечная ткань осуществля< движение кропи по сосудам. Мионейральная ткань обеспечивает изменен!;. размеров зрачка, а миоэпителиальная ткань способствует выведению сскре та из желез. Таким образом, двигательные процессы в организме разнооб разиы, но основой их является сокращение миофибрилл — специальны органоидов движения, состоящих из актиновых и миозиновых филаментоь Двигательные процессы, основанные на взаимодействии сократимых бел ков цитоскелета, имеют место в любой клетке организма, однако в мышеч ной ткани они являются основной и практически единственной функцией Структурной основой этой функции являются сформировавшиеся в фило генезе на базе сократимых белков цитоскелета миофибриллы. Следователь но, второе, что объединяет вес виды мышечных тканей — это наличие в цитоплазме специальных органелл движения миофибрилл.
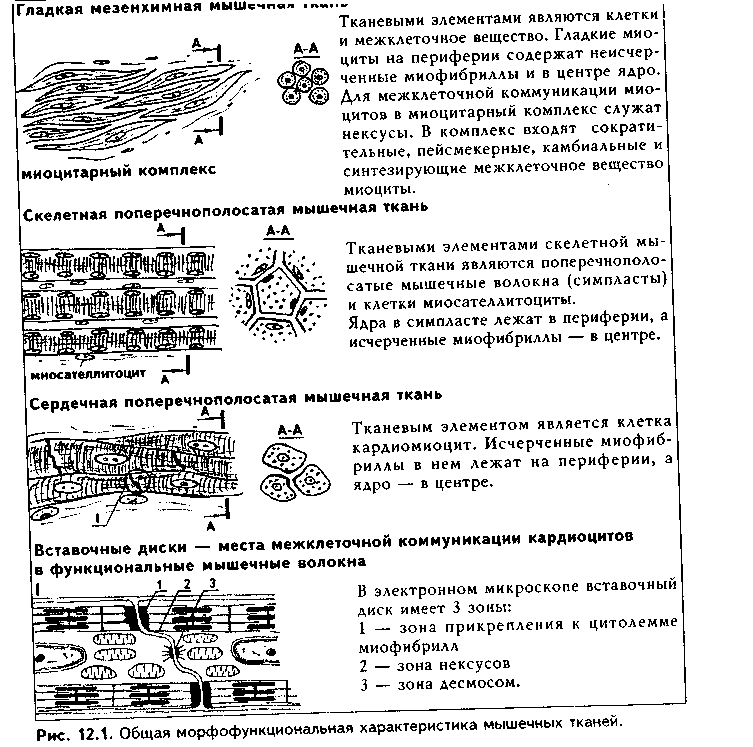
В остальном между пятью указанными выше видами мышечных тканей больше различий, чем сходства. Они имеют разное происхождение. Источником развития скелетной мышечной ткани являются миотомы сомитов. Сердечная мышечная ткань имеет источником развития миоэпикардиальную пластинку, часть висцерального листка спланхнотома. Источник развития гладкой мышечной ткани — мезенхима, в основном спланхнотомная. Мионейральная ткань развивается из нейроэктодермы, а миоэпителиальная — из кожной эктодермы. Тканевыми элементами скелетной мышечной ткани являются симпласты и клетки миосателлитоциты. Все остальные мышечные ткани построены исключительно из клеток: в сердечной мышечной ткани они называются кардиомиоцитами, в гладкой — гладкими миоцитами, в мио-нейралыюй — мионейроцитами, в миоэнителиадыюй — миоэпителиоцитами (или корзинчатыми клетками). Мышечные ткани выполняют своп функции при тесном взаимодействии с нервной тканью. При этом скелетная мышечная ткань получает соматическую двигательную иннервацию, остальные виды мышечной ткани иинервируются вегетативной нервной системой. Регенераторные свойства мышечных тканей различные. Скелетная мы
шечная ткань содержит камбиальные клетки (миосателлитоциты) и при необ
ходимых условиях регенерирует удовлетворительно, сочетая клеточную и
внутриклеточную регенерацию. Содержат камбий и хорошо регенерируют на
клеточном уровне гладкая мышечная ткань и миоэпителиальиая ткань. В сер
дечной мышечной ткани в дефинитивном состоянии стволовые клетки отсут
ствуют, поэтому у взрослого человека подавляющая часть кардиомиоцитов не
делится и при повреждении замещается соединительной тканью. Регенерация
этой ткани происходит только на внутриклеточном уровне. Регенераторные
свойства мионейралыгой ткани не изучены. Общая морфофункциональная
характеристика основных видов мышечных тканей приведена на рис. 12.1.
КЛАССИФИКАЦИЯ МЫШЕЧНЫХ ТКАНЕЙ Существует несколько подходов в классификации мышечных тканей.
1. Физиологическая классификация.
По этой классификации мышечные ткани делятся на произвольные и непроизвольные.
К произвольной мышечной ткани относится скелетная мышечная ткань. Ее сокращение контролируется сознанием. Сокращения у этой ткани быстрые, в сокращенном состоянии мышца может находиться относительно непродолжительное время, расслабление также осуществляется быстро.
К непроизвольным мышечным тканям относятся все остальные мышечные ткани. При этом у гладкой мышечной ткани сокращения происходят в течение достаточно длительного времени, в сокращенном состоянии гладкие миоциты могут находиться длительно, а процесс расслабления также длительный. У сердечной мышечной ткани сокращения автоматические. Отличия в сократительных актах объясняются особенностями иннервации мышечных тканей, а также наличием в сердечной мышечной ткани проводящих кардиомиоцитов (см. ниже).
2. Морфологическая классификация. Основана на структурном феномене наличия или отсутствия исчерченности миофибрилл. По этой классификации мышечные ткани делятся на:
1) исчерченные;
2) неисчерченные.
К неисчерченным мышечным тканям относятся мышечная ткань ме-зенхимного происхождения (сосудов и внутренних органов), эктодермаль-ного происхождения (миоэпителиоциты потовых, молочных, слюнных, слезных желез), мионейрального происхождения (мышцы суживающие и расширяющие зрачок). Компоненты миофибрилл в этих тканях расположены так, что отсутствует их исчерченность. К исчерченным мышечным тканям относят скелетную и сердечную мышечную ткани. В них миофиб-риллы построены из структурно-функциональных единиц саркомеров (см. ниже), в которых имеются светлые и темные участки, придающие миофиб-рилле и всему мышечному волокну исчерченность.
3. Гистогенетическая классификация мышечных тканей учитывает источники их развития. Эта классификация выглядит так:
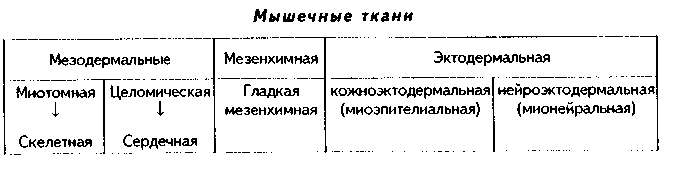
ХАРАКТЕРИСТИКА РАЗНОВИДНОСТЕЙ МЫШЕЧНЫХ ТКАНЕЙ.
ГЛАДКАЯ МЫШЕЧНАЯ ТКАНЬ.
МЕЗЕНХИМНАЯ ГЛАДКАЯ МЫШЕЧНАЯ ТКАНЬ
ГИСТОГЕНЕЗ. Источником развития гладкой мышечной ткани является н основном спланхнотомная мезенхима. Ее клетки мигрируют и окружают эпителиальные зачатки тех органов, в состав которых входит гладкая мышечная ткань. Начало дифферсицировки гладкой мышечной ткани характеризуется удлинением мезенхимных клеток и превращением их из звездчатых в веретеновидные. В цитоплазме клеток появляются органеллы белкового синтеза, осуществляющие синтез специфических белков миофибрилл. Из этих белков производится сборка большого количества миофибрилл, и клетки начинают реагировать на раздражение сокращением. Часть клеток остается в малодифферснцированном состоянии и служит источником для регенерации.

|
СТРОЕНИЕ. Во взрослом организме гладкая мышечная ткань входит в состав стенки органов пищеварительного тракта, образует мышечные оболочки кровеносных и лимфатических сосудов, бронхиального дерева, яйцеводов, матки, мочеточников, мочевого пузыря, входит в состав капсулы селезенки, есть в эндокарде. Гладкая мышечная ткань стенки сосудов по ряду морфофункциональных признаков отличается от гладкой мышечной ткани другой локализации.
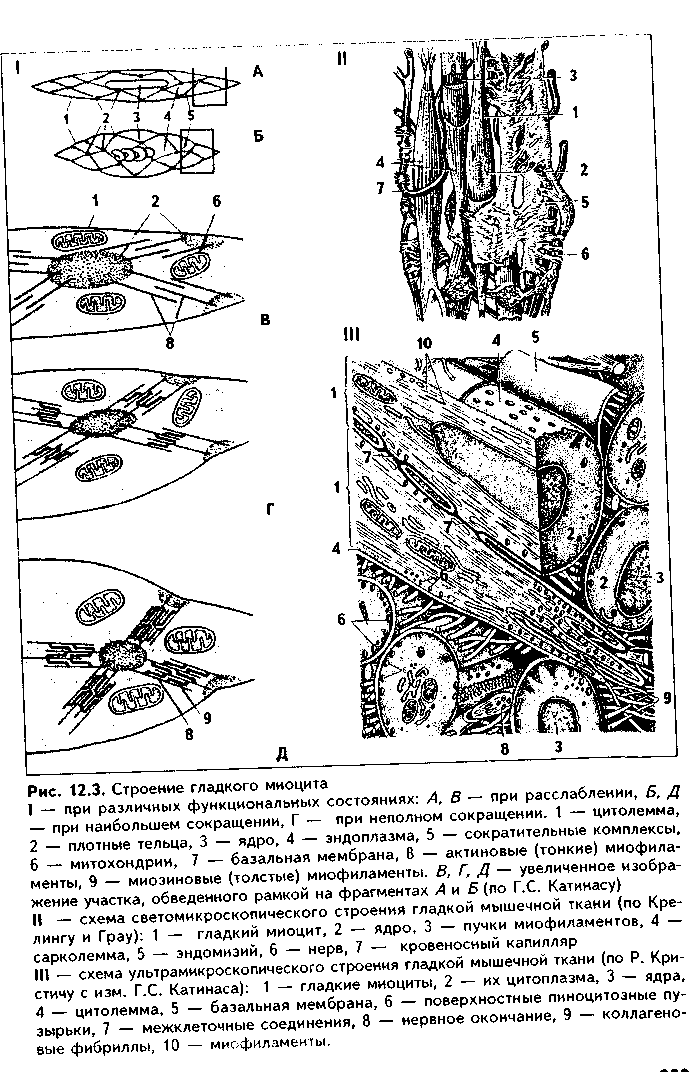
Структурно-функциональным тканевым элементом ткани является гладкий миоцит (иногда в качестве второго тканевого элемента называют межклеточное вещество, которое способны синтезировать миоциты). Гладкий миоцит (рис. 12.2) — клетка веретеновидной формы, длина может быть от 20 до 500 мкм, как, например, в матке, в мышечной оболочке которой миоциты имеют также особую (звездчатую) форму. Ядра клеток палочковидной или эллипсоидной формы, с плотным хроматином и 1—2 ядрышками. Гладкий миоцит покрыт цитолеммой. Снаружи от нее лежит тонкая базальная мембрана с ретикулярными фибриллами, которая отграничивает каждый гладкий миоцит от соседних миоцитов.
В цитоплазме гладких миоцитов имеются все органеллы общего назначения, лежащие в околоядерных участках цитоплазмы (рис. 12.3): гранулярная ЭПС, выполняющая синтез белков межклеточного вещества, комплекс Гольджи, митохондрии, многочисленные пузырьки, лежащие под цитолеммой (кавеолы) и открытые в сторону межклеточной среды. Этот везикулярный аппарат депонирует ионы Са2*, необходимые для сокращения, и является аналогом одновременно и саркоплазматического ретикулу-ма (СПР), и Т-трубочек в исчерченной мышечной ткани (см. ниже). В ми-оците имеются также и элементы редуцированного саркоплазматического ретикулума в виде пузырьков и небольших цистерн. С ними кавеолы мо- гут иметь связи. Кавеолы СИР содержат в своей мембр.; не белки транспорта кальки: В цитоплазме гладких миоцп тов есть включения гликоген;!
11а периферии миоцитоь под их цитолеммой находят; плотные тельца, состоящие и белка а-актинина — аналоги / линий саркомеров (см. ниже) Есть две разновидности плот ных телец: 1) связанные i внутренней поверхностью илазмолеммы (сарколеммы; миоцита при помощи комплекса адгезивных белков (винкули-на, тензина и др.). Эти плот ные тельца на самом деле представляют собой срезанные поперечно пластинки, имеющие вид длинных непрерывных ребер, которые лежат параллельно друг другу под сарколеммой; 2) свободно лежащие в цитоплазме (саркоплазме). Лежат в виде правильной цепочки. К плотным тельцам прикрепляются актиновые и промежуточные десминовые филаменты. Последние образуют сложную трехмерную сеть в саркоплазме. Важный компонент цитоплазмы гладких миоцитов — сократительные белковые нити, или миофиламенты, образующие миофибриллы. Эти нити расположены вдоль длинной оси миоцита, а по отношению друг к другу так, что не образуют поперечной исчерченности. Тонкие актиновые миофиламенты одним концом прикрепляются к плотным тельцам. Они в отличие от скелетной мышечной ткани состоят только из белка актина (мышечного и немышечного), не содержат тропонина и тропомиозина и более многочисленны. Актиновые филаменты взаимодействуют с толстыми мио-зиновыми филаментами, образуя так называемые сократимые единицы. В отличие от миозиновых филамептов скелетной мышечной ткани миозино-вые филаменты гладких миоцитов менее стабильны, а по мнению некоторых исследователей, молекулы миозина в состоянии покоя находятся в де-полимеризованной форме, и миозиновые филаменты организуются путем сборки непосредственно перед сокращением, вновь распадаясь после него. Поэтому в гладких мышечных тканях не формируются миофибриллы, сар-
комсры и отсутствует поперечная исчерченность. Сборка из молекул мио зипа толстых миозииовых филаментов происходит при инициации сокрп тения, и этот процесс, а также взаимодействие актиновых и миозиновьп филаментов активируют ионы кальция, поступающие из кальциевых депо -- СПР, кавеол и митохондрий. Образующиеся сократительные единицы направлены под углом к длине миоцита.
Механизм сокращения гладких миоцитов принципиально сходен с со кращением скелетных мышечных волокон и более подробно будет рассмотрен ниже. Он заключается во взаимодействии актиновых и миозииовых филаментов (теория скольжения X. Хаксли), которое инициируют ионы кальция, выделяемые СПР, митохондриями и кавеолами. Под действием нервного импульса из пиноцитозных пузырьков высвобождается Са2', который образует комплекс с кальцийсвязывающим белком кальмодулином. Комплекс "Са2+ — кальмодулин" активирует фермент киназу легких цепей миозина, фосфорилирующую легкие цепи миозина. Фосфорилирование миозина придает ему способность взаимодействовать с актиновыми фила ментами. В итоге головки молекул миозина сформированных и активиро ванных миозии
|
|
|


