 |
Титриметричний аналіз. Метод комплексонометрії
|
|
|
|
Титриметричний аналіз. Метод комплексонометрії
- В основі методу комплексонометрії лежить реакція:
а) нейтралізації;
б) окислення-відновлення;
в) комплексоутворення;
г) осадження.
2. Робочий розчин (стандартизований) методу трилонометрії:
а) нітрат срібла;
б) тіосульфат натрію;
в) трилон Б;
г) щавлева кислота.
3. У трилонометрії використовується індикатор:
а) метилоранж;
б) крохмаль;
в) еріохром чорний Т;
г) фенолфталеїн.
4. У трилонометрії застосовується титрування:
а) пряме;
б) обернене;
в) титрування по залишку;
г) титрування замісника.
- При визначенні точної концентрації робочого розчину у методі трилонометрії в точці еквівалентності, яка фіксується за допомогою індикатора:
а) розчин забарвлюється у синьо-блакитний колір;
б) розчин забарвлюється у рожевий колір;
в) розчин знебарвлюється;
г) розчин забарвлюється у вишнево-червоний колір.
- Індикатор еріохром чорний Т утворює з металами комплекси, які мають колір (метод трилонометрії):
а) вишнево-червоний;
б) жовтий;
в) безбарвний;
г) синій.
7. Органічні барвники, які утворюють з катіонами металу розчинні у воді забарвлені комплексні сполуки, причому комплекси індикатора з катіонами металу менш міцні, ніж внутрішньо комплексні солі металу з комплексоном:
а) комплексони;
б) органічні реагенти;
в) індикатори;
г) металіндикатори.
8. Визначення загальної твердості води проводять:
а) комплексонометричним методом: робочий розчин
трилону Б, рН< 7, аміачний буфер;
б) комплексонометричним методом: робочий розчин
трилону Б, рН 8-9, NH4OH + NH4CI;
в) комплексонометричний методом: робочий розчин МgCI2, трилону Б, буферна суміш СН3СООН + СН3СООNa, рН < 7, еріохром чорний Т;
|
|
|
г) комплексонометричним методом: робочий розчин трилону Б, стандартний розчин МgСІ2, еріохром чорний Т, буферна суміш NH4OH + NH4CI.
- При визначенні Са2+ трилонометричним методом в точці еквівалентності спостерігається зміна забарвлення:
а) за рахунок руйнування комплексної сполуки індикатора з катіоном металу і виділення індикатора у вільному стані;
б) з темно-вишневого до синьо – блакитного;
в) з синьо-блакитного до червоного;
г) знебарвлення розчину внаслідок утворення внутрішньо комплексних сполук трилону Б з іонами кальцію;
- Яка реакція лежить в основі трилонометричного титрування:
а) осадження;
б) комплексоутворення;
в) нейтралізації;
г) окислення – відновлення.
Фізико-хімічні методи аналізу. Колориметрія
- До оптичних методів аналізу належать:
а) кондуктометрія, потенціометрія, електрогравіметрія;
б) люмінесцентний, колориметричний, фотометричний;
в) колориметрія, нефелометрія, електрогравіметрія;
г) фотометрія, нефелометрія, рефрактометрія, поляриметрія.
- Оптичні методи встановлюють:
а) залежність між складом досліджуваної речовини та оптичною властивістю;
б) залежність між електрохімічними властивостями розчинів і складом досліджуваної речовини;
в) залежність розподілу речовини між двома фазами залежно від їх адсорбційної здатності;
г) залежність між складом досліджуваної речовини та здатністю до світлопоглинання.
- Фотометричні (колориметричні) методи аналізу базуються на реакціях:
а) окислення – відновлення; комплексоутворення;
б) світлопоглинання;
в) світлорозсіяння;
г) з утворенням забарвлених розчинних сполук.
- До методів візуальної колориметрії належать:
а) фотоелектроколориметрія;
б) метод стандартних серій, колориметричного титрування; розведення;
в) метод стандартних серій, спектрофотометричний, фотоелектроколориметричний;
|
|
|
г) метод колориметричного титрування, метод стандартних серій, інструментальні методи.
- Фізико-хімічні методи аналізу базуються на:
а) залежності фізичної характеристики речовин від їх хімічного складу;
б) визначенні складу речовини з використанням хімічних реакцій;
в) залежності між складом речовини та їх хімічними властивостями;
г) люмінесценції досліджуваних речовин, під дією ультрафіолетових променів.
- Колориметричні методи аналізу базуються на:
а) реакціях, що супроводжуються утворенням забарвлених розчинних сполук (іноді руйнуванням забарвлених сполук);
б) різному розподілу речовин між двома фазами залежно від їх адсорбційної здатності;
в) вимірюванні електропровідності розчину;
г). вимірюванні рівноважних електродних потенціалів.
- При проведенні колориметричного визначення:
а) вимірюють оптичну густину і коефіцієнт заломлення розчину перед проведенням хімічної реакції;
б) вимірюють різницю електродних потенціалів розчину;
в) проводять хімічну реакцію з утворенням забарвленої сполуки;
г) вимірюють інтенсивність світло поглинання утвореного розчину.
- Фізична величина, що характеризує ступінь поглинання світла при проходженні його через розчин, називається:
а) коефіцієнт заломлення світла;
б) інтенсивність розсіяння світла;
в) оптична густина;
г) молярний коефіцієнт світло поглинання.
- Інтенсивність поглинання світла залежить від:
а) температури розчину;
б) концентрації розчиненої речовини у розчині;
в) концентрації забарвленої сполуки в розчині;
г) товщини поглинаючого шару.
- Оптична густина розчинів пропорційна добутку концентрації забарвленої речовини та товщині поглинаючого шару – це формулювання:
а) закону розподілу Нернста;
б) закону дії мас;
в) закону Бугера – Ламберта – Бера;
г) закону Столетова.
- Молярний коефіцієнт світло погашення характеризує:
а) внутрішні властивості речовини;
б) чутливість можливого колориметричного визначення речовин;
в) коефіцієнт можливого розсіювання світла;
г) здатність речовини обертати площину поляризації світла.
- Знайдіть вираз закону Бугера – Ламберта – Бера:
а) lg  = E
= E 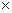 L × n;
L × n;
|
|
|
б) lg  = E
= E 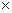 L × C;
L × C;
в)  ;
;
г)  .
.
- Методи візуальної колориметрії базуються на:
а) досягненні однакової інтенсивності забарвлення досліджуваного та стандартного розчинів, порівняння відбувається візуально;
б) порівнянні світлових потоків, яке здійснюється за допомогою фотометричних приладів;
в) на вимірюванні поглинання світлового потоку, що пройшов через забарвлений розчин;
г) на вимірюванні поглинання світла, що пройшов через забарвлений або безбарвний розчин.
- Для вимірювання інтенсивності забарвлення розчину використовують такі прилади:
а) рефрактометр;
б) фотоелектроколориметр;
в) флуорометр;
г) спектрофотометр.
15. Назвіть метод аналізу, при якому готують колориметричну шкалу, порівнюють забарвлення досліджуваного розчину із забарвленням серії стандартних розчинів:
а) метод фотометрії;
б) візуальна колориметрія;
в) метод колориметричного титрування;
г) метод стандартних серій.
16. Ряд розчинів з відомою концентрацією досліджуваної речовини, називається:
а) стандартними розчинами;
б) розбавленими розчинами з точно встановленим титром;
в) робочими розчинами;
г) колориметричною шкалою.
- Для виконання колориметричного титрування використовують:
а) два однакові циліндри, готують один стандартний розчин, два робочих розчини;
б) бюретку з стандартним розчином, дві конічні колби для титрування, мірну піпетку;
в) два циліндри, два стандартні розчини, бюретку, мірну піпетку, досліджуваний розчин;
в) два однакових циліндри, бюретку зі стандартним розчином досліджуваної речовини, розчин досліджуваної речовини, дистильована вода, реактиви.
- Основною умовою проведення колориметричного титрування є:
а) миттєва зміна забарвлення розчину;
б) однакові циліндри;
в) порядок додавання реактивів;
г) стійкість забарвлення стандартного розчину у часі.
- В методі розведення:
а) готують серію стандартних розчинів, забарвлення яких порівнюють з забарвленням досліджуваного розчину;
б) готують один стандартний розчин, порівнюють інтенсивність забарвлення стандартного розчину із забарвленням досліджуваного розчину в мірних циліндрах;
|
|
|
в) готують один стандартний розчин, порівняння інтенсивності забарвлення відбувається шляхом розведення водою найбільш інтенсивно забарвленого розчину проводять в градуйованих циліндрах;
г) готують серію стандартних розчинів в мірних колбах, вимірюють оптичну густину стандартних розчинів, будують калібрувальний графік, вимірюють оптичну густину досліджуваного розчину, порівняння інтенсивностей світлових потоків відбувається в фотоелектроколориметрах.
20. Виберіть формулу для обчислення результатів при проведенні колориметричного титрування:
а) m(речовини) =  ;
;
б) 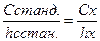 ;
;
в)  ;
;
г) m(Х)=  .
.
- Величина фотоструму, що виник, прямо пропорційна світловому потоку, що падає, - це формулювання:
а) закону Бугера – Ламберта – Бера;
б) закону Столетова;
в) закону дії мас;
г) закону Гесса.
- В фотоелектроколориметрії ступінь поглинання світла (інтенсивність забарвлення розчину) визначають за допомогою:
а) фотоелемента;
б) фотоелектроколориметра;
в) мікроамперметра;
г) світлофільтра, призми.
- Фотоефект – це явище:
а) світіння атомів, молекул та інших частинок, що виникає в результаті електронного переходу при повертанні із збудженого стану до основного;
б) відхилення стрілки амперметра при потраплянні світла на фотоелемент;
в) відриву електронів від атомів різних речовин під впливом світлової енергії;
г) зміни напряму прямолінійного поширення світла при переході з одного середовища в інше.
|
|
|


