 |
Исследование других органов 8 глава
|
|
|
|

|
После этого в режиме двухмерной ЭхоКГ, зарегистрированной из парастернального доступа по длинной оси ЛЖ, в середине систолы измеряют внутренний диаметр фиброзного кольца аортального клапана (D), автоматически рассчитывая площадь поперечного сечения корня аорты (рис. 2.30, в). Для расчета УО (мл) интеграл линейной скорости кровотока (в см) умножают на площадь поперечного сечения аорты — SAo (см2):

|
Понятно, что то же значение УО может быть получено при умножении средней линейной скорости кровотока (см/с) на продолжительность периода изгнания (ЕТ, в с) и площадь поперечного сечения аорты (см2):

|
где КДР и КСР — конечные диастолический и систолический размеры ЛЖ.

|
| Рис. 2.30. Эхокардиографическое определение ударного объема левого желудочка с помощью допплер-ЭхоКГ (схема). а — допплер-локация (импульсный режим) выходного отдела ЛЖ (LVOT); б — систолический спектр линейной скорости кровотока в выходном отделе ЛЖ; в — двухмерная ЭхоКГ (парастернальный доступ по длинной оси ЛЖ) и измерение внутреннего диаметра фиброзного кольца аортального клапана (D). ЕТ — продолжительность изгнания крови, V max — максимальная линейная скорость кровотока, VTI — интеграл линейной скорости кровотока, S Ao — площадь поперечного сечения корня аорты |
Скорость циркулярного укорочения волокон миокарда (VCF):
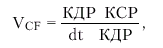
|
где dt — время сокращения ЛЖ.
При снижении сократимости миокарда ЛЖ значения обоих индексов уменьшаются, причем более чувствительным показателем считается скорость циркулярного укорочения волокон миокарда (VCF) (И.М. Хейнонен, Р.Е. Денисов). Следует помнить, что расчет приведенных индексов сократимости проводится по данным одномерной ЭхоКГ и дает лишь ориентировочное представление о сократительной функции ЛЖ. Нормальные значения %DS и VCF колеблются в довольно широких пределах.
|
|
|
Размер левого предсердия также несет важную информацию о функциональном состоянии левых отделов сердца. Его увеличение у больных ХСН косвенно свидетельствует о повышении давления наполнения и снижении функции ЛЖ. Размеры ЛП обычно измеряют в М-режиме из левой парастернальной позиции (рис. 2.31). При изменении угла наклона ультразвукового луча, показанного на рисунке, получают изображение аорты и левого предсердия, которое позволяет количественно оценить размеры этих отделов сердца. Как видно на рисунке, на экране сверху вниз определяются следующие структуры сердца: передняя стенка (RVW) и выходной тракт ПЖ (RVOT), основание аорты (Ао), полость ЛП (LА), задняя стенка ЛП.
Передняя и задняя стенки основания аорты визуализируются в виде параллельных волнистых линий толщиной 2–3 мм. Они смещаются к датчику (вверх) во время систолы ЛЖ, и в противоположную сторону (вниз) — во время диастолы. Амплитуда их движения в норме достигает 10 мм. Диаметр устья аорты (“1”) измеряют от наружной поверхности ее передней стенки до внутренней поверхности задней стенки.
В центре просвета аорты обычно визуализируется движение створок аортального клапана (АК): в систолу ЛЖ они расходятся, в диастолу смыкаются, образуя на эхокардиограмме типичную замкнутую кривую, напоминающую “коробочку”. Амплитуда раскрытия аортального клапана (“3”) в начале систолы ЛЖ в норме превышает 18 мм.
Задняя стенка ЛП на одномерной эхокардиограмме в этой позиции во время систолы желудочков смещается в сторону от датчика (вниз) примерно на 8–10 мм. Диаметр ЛП (“2”) измеряют в период максимального движения задней стенки аорты вперед (на экране — вверх) в конце систолы (или в самом начале диастолы) от наружной поверхности задней стенки аорты до эндокардиальной поверхности ЛП. В норме этот размер составляет 19–33 мм.
|
|
|
Следует отметить, что переднезадний размер ЛП, определяемый при М-модальном исследовании из парастернального доступа, обладает минимальной чувствительностью в диагностике дилатации предсердия, поскольку увеличение этого показателя обнаруживают, как правило, лишь на поздних стадиях расширения ЛП. Поэтому более предпочтительным является расчет объема ЛП по данным двухмерной ЭхоКГ (верхушечная позиция), который аналогичен определению объема ЛЖ по методу “площадь–длина” или по методу дисков (по Simpson).
В норме размер ЛП составляет 19–33 мм. Его увеличение до 40 мм и более свидетельствует о повышении давления наполнения ЛЖ и риска застойных явлений в малом круге кровообращения.
В табл. 2.7. представлены нормальные величины некоторых эхокардиографи ческих показателей глобальной систолической функции ЛЖ.
Таблица 2.7
Средние значения основных гемодинамических показателей по данным ЭхоКГ
| Гемодинамические показатели | М-режим | Двухмерная эхокардиограмма | ||
| Метод “площадь–длина” (апикальная позиция) | Метод дисков (по Simpson) | |||
| 4-камерная | 2-камерная | |||
| КДО м-ны (мл) | 110–145 | |||
| КДО ж-ны (мл) | ||||
| Индекс КДО (мл/м2) | 55–73 | |||
| КСО м-ны (мл) | 45–75 | |||
| КСО ж-ны (мл) | ||||
| Индекс КСО (мл/м2) | 23–38 | |||
| УО м-ны (мл) | 60–80 | |||
| УО ж-ны (мл) | ||||
| УИ (мл/м2) | 25–34 | 30–38 | 31–44 | 27–38 |
| ФВ (%) | 55–65 | |||
| МО (л/мин) | 3,5–4,5 | |||
| СИ (л/мин/м2) | 2,2–2,7 | |||
| ЛП м-ны | 19–33 мм | 41 мл | 50 мл | 41 мл |
| ЛП ж-ны | 34 мл | 36 мл | 32 мл | |
| Индекс ЛП | 14,5–29 мм/м2 | 24 мл/м2 | 21 мл/м2 | 21 мл/м2 |
| %DS (%) | 28–43 | – | – | – |
| VCF (с–1) | 0,8–1,2 | – | – | – |

|
| Рис. 2.31. Схема получения одномерной ЭхоКГ при сканировании из левого парастернального доступа на уровне створок аортального клапана. Обозначения те же. S — систола желудочков; RVOT — выносящий тракт ПЖ; RСС — правая коронарная створка аортального клапана; NСС — некоронарная створка аортального клапана; «1» — диаметр устья аорты; «2» — диаметр ЛП; «3» — амплитуда раскрытия аортального клапана |
Таким образом, основными гемодинамическими показателями, отражающими в первую очередь систолическую функцию желудочков, являются: УО, МО, СИ, ФВ, а также размеры ЛП, конечно-систолический (КСО) и конечно-диастолический (КДО) объемы ЛЖ.
|
|
|
Нормальные значения УО и МО, а также размеров и объемов камер сердца колеблются в широких пределах и зависят от роста, массы тела и пола пациента. Поэтому для характеристики центральной гемодинамики обычно используют индексы этих показателей, т.е. отношение последних к площади поверхности тела.
Наиболее ранним маркером уменьшения систолической функции ЛЖ является снижение ФВ ниже 40–45% (табл. 2.8). Понятно, что такое снижение ФВ, как видно из формулы его определения, как правило, сочетается с увеличением КСО и КДО, т.е. с дилатацией ЛЖ и его объемной перегрузкой. Такое сочетание особенно характерно для систолической формы ХСН. Следует, правда, иметь в виду сильную зависимость показателя ФВ от величины пред- и постнагрузки. Например, ФВ может уменьшаться не только при снижении сократимости миокарда желудочков, но и при гиповолемии (шок, острая кровопотеря и т.д.), уменьшении притока крови к правому сердцу, а также при быстром и резком подъеме АД (подробнее см. главу 1).
Таблица 2.8
Характеристика систолической функции левого желудочка в зависимости от величины ФВ
| Фракция выброса, % | Характеристика систолической функции ЛЖ |
| до 50–55 | Нормальная |
| 45–50 | Несколько сниженная |
| 35–45 | Умеренно сниженная |
| 25–35 | Значительно сниженная |
| < 25 | Резко сниженная |
Если у больного с ХСН имеется умеренно выраженная систолическая дисфункция ЛЖ, то уменьшение ФВ в течение некоторого времени может не сопровождаться снижением сердечного выброса, т.е. значений СИ. Это происходит, главным образом, в результате действия двух факторов:
- увеличения ЧСС, что способствует сохранению МО на уровне нижней границы нормы, несмотря на падение значений УО;
- включения механизма Старлинга: большее растяжение мышечного волокна умеренно дилатированного желудочка (тоногенная дилатация) способствует увеличению силы сокращения, т.е. сохранению УО почти на нормальном уровне.
Естественно, дальнейшее прогрессирование систолической дисфункции у больных ХСН приводит к уменьшению как ФВ, так и СИ и, соответственно, еще большему увеличению КСО, КДО и миогенной дилатации ЛЖ.
|
|
|
 Запомните
1. Важнейшими гемодинамическими показателями систолической функции ЛЖ являются сердечный индекс — СИ (в норме 2,2–2,7 л/мин/м2) и фракция выброса ЛЖ — ФВ (в норме 55–60%). 2. Умеренно выраженная систолическая дисфункция ЛЖ сопровождается: снижением ФВ ниже 40–45%; увеличением КСО и КДО (т.е. наличием умеренной дилатации ЛЖ); сохранением в течение некоторого времени нормальных значений СИ. 3. При выраженной систолической дисфункции ЛЖ происходит: дальнейшее падение величины ФВ; еще большее увеличение КДО и КСО (выраженная миогенная дилатация ЛЖ); уменьшение СИ ниже 2,2 л/мин/м2. Запомните
1. Важнейшими гемодинамическими показателями систолической функции ЛЖ являются сердечный индекс — СИ (в норме 2,2–2,7 л/мин/м2) и фракция выброса ЛЖ — ФВ (в норме 55–60%). 2. Умеренно выраженная систолическая дисфункция ЛЖ сопровождается: снижением ФВ ниже 40–45%; увеличением КСО и КДО (т.е. наличием умеренной дилатации ЛЖ); сохранением в течение некоторого времени нормальных значений СИ. 3. При выраженной систолической дисфункции ЛЖ происходит: дальнейшее падение величины ФВ; еще большее увеличение КДО и КСО (выраженная миогенная дилатация ЛЖ); уменьшение СИ ниже 2,2 л/мин/м2.
|
Методика эхокардиографи ческой оценки диастолической функции ЛЖ описана в разделе 2.7.
Оценка систолической функции правого желудочка
Более сложной оказывается оценка глобальной систолической функции правого желудочка (ПЖ). Неплохие результаты могут быть получены при измерении диастолического размера ПЖ при регистрации М-модальной ЭхоКГ из парастернального доступа по короткой оси сердца (рис. 2.32). В норме КДРПЖ составляет около 15–20 мм, а при дилатации ПЖ обычно превышает 26 мм. Следует помнить, что нередко при таком способе исследования полость ПЖ и эндокардиальная поверхность его передней стенки видны неотчетливо в связи с наличием большого количества трабекул.

|
| Рис. 2.32. Определение КДР правого желудочка в норме (а) и при дилатации правого желудочка (б). Измерения проводят в конце диастолы, соответствующем зубцу R ЭКГ |
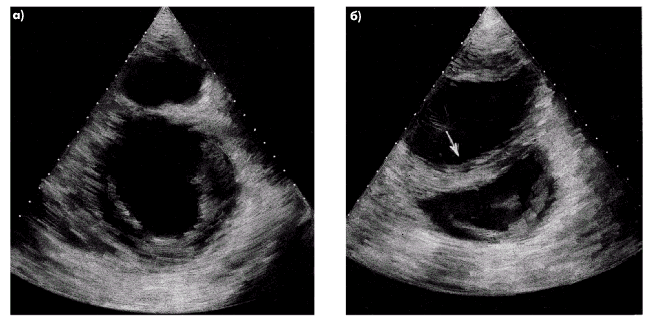
Дилатация ПЖ сравнительно хорошо выявляется при двухмерном исследовании в парастернальной позиции по короткой оси, а также в апикальной позиции четырехкамерного сердца. При диагностически значимом расширении ПЖ его размеры в этих позициях равны или даже превышают размеры ЛЖ (рис. 2.33), тогда как в норме имеют место обратные отношения.
|
| Рис. 2.33. Двухмерные эхокардиограммы, зарегистрированные в парастернальной позиции по короткой оси в норме (а) и при выраженной дилатации правого желудочка (б). Отмечается изменение нормального соотношения размеров ЛЖ и ПЖ, утолщение передней стенки ПЖ и МЖП, а также парадоксальное движение МЖП в сторону левого желудочка (отмечено стрелкой) |
Косвенное определение давления в легочной артерии
Неинвазивное определение давления в малом круге кровообращения и диагностика легочной артериальной гипертензии необходимы для оценки тяжести течения и прогноза многих заболеваний сердца, в том числе сердечной недостаточности. М-модальное, и особенно двухмерное, ультразвуковое исследование позволяет выявить ряд косвенных признаков, характерных для повышения давления в легочной артерии: 1. Гипертрофию и дилатацию ПЖ (см. ниже).
|
|
|
2. Вторичную недостаточность легочного и трехстворчатого клапанов.
3. Изменение характера движения задней створки клапана легочной артерии.
С помощью допплеровского исследования можно выявить наиболее достоверные качественные и количественные признаки гипертензии. Исследование систолического потока через клапан легочной артерии обычно проводят из левого парастернального доступа по короткой оси (рис. 2.34). Основная волна допплеркардиограммы направлена в сторону от ультразвукового датчика и располагается ниже базовой линии спектрограммы. Пик максимальной скорости, как правило, смещен к началу потока и имеет закругленную вершину. По сравнению с аортальным систолическим потоком крови поток в выходном отделе ПЖ и в устье легочной артерии меньшей амплитуды (не более 60–71 см/с) и имеет закругленную вершину.

|
| Рис. 2.34. Допплер-ЭхоКГ потока крови через клапан легочной артерии (PА), зарегистрированная по короткой оси из левого парастернального доступа. а — схема расположения ультразвукового датчика и направления сканирования; б — допплерограмма потока крови. Во время систолы ПЖ определяется систолический пик скорости, направленный вниз |
Качественные критерии легочной гипертензии заключаются в изменении формы потока крови в выносящем тракте ПЖ и в устье клапана легочной артерии. При нормальном давлении в легочной артерии форма потока крови приближается к куполообразной и симметричной (рис. 2.35, а), а при легочной гипертензии становится треугольной или двухпиковой. Треугольный тип формы кривой характеризуется более быстрым формированием пика линейной скорости, который смещается к началу кривой (рис. 2.35, б). Двухпиковый тип кривой также отличается уменьшением времени начального ускорения кровотока в легочной артерии, после чего наблюдается мезосистолическое его замедление, а затем снова — позднесистолическое ускорение (рис. 2.35, в). Кривая линейной скорости при этом приобретает своеобразный W-образный вид.

|
| Рис. 2.35. Изменение формы допплерограммы систолического потока крови в выносящем тракте правого желудочка: а — куполообразная и симметричная форма потока при отсутствии легочной гипертензии, б — треугольная форма потока крови при легочной гипертензии, в — двухпиковый тип кривой при легочной гипертензии. Объяснение в тексте |
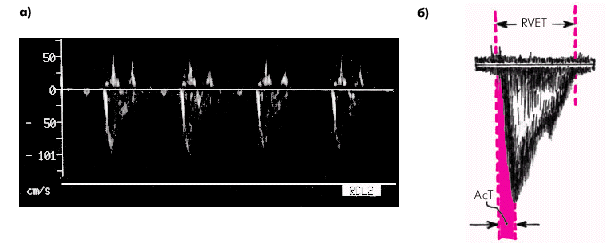
Метод количественного определения среднего давления в легочной артерии (СрДЛА) (по A. Kitabatake с соавт., 1983). Данный метод отличается относительной простотой и в то же время достаточной точностью определения СрДЛА. Он основан на измерении некоторых количественных параметров, характеризующих систолический поток крови в выходном отделе ПЖ (рис. 2.36), и вычислении отношения времени ускорения потока (времени от начала кривой до ее пика — АсТ) к общей длительности изгнания из ПЖ (RVET). Было показано, что это отношение находится в обратной зависимости от величины среднего давления в легочной артерии. В табл. 2.9. представлены значения СрДЛА в зависимости от величины отношения AcT/RVET.
|
| Рис. 2.36. Допплерограмма систолического потока крови в устье легочной артерии у больной с легочной гипертензией (а) и измерение количественных параметров допплерограммы, необходимых для расчета среднего давления в легочной артерии (б). Объяснение в тексте |
Таблица 2.9
Среднее давление в легочной артерии в зависимости от величины отношения
AcT/RVET (по данным импульсной допплер-эхокардиографии)
| AcT/RVET | СрДЛА, мм рт. ст. | AcT/RVET | СрДЛА, мм рт. ст. | AcT/RVET | СрДЛА, мм рт. ст. |
| 0,10 | 131,8 | 0,26 | 47,0 | 0,39 | 20,3 |
| 0,14 | 101,8 | 0,27 | 44,0 | 0,40 | 19,0 |
| 0,15 | 95,4 | 0,28 | 41,3 | 0,41 | 17,8 |
| 0,16 | 89,5 | 0,29 | 38,7 | 0,42 | 16,7 |
| 0,17 | 83,9 | 0,30 | 36,3 | 0,43 | 15,7 |
| 0,18 | 78,7 | 0,31 | 34,0 | 0,44 | 14,7 |
| 0,19 | 73,9 | 0,32 | 31,9 | 0,45 | 13,8 |
| 0,20 | 69,2 | 0,33 | 29,9 | 0,46 | 12,9 |
| 0,21 | 64,8 | 0,34 | 28,5 | 0,47 | 12,1 |
| 0,22 | 60,8 | 0,35 | 26,3 | 0,48 | 11,4 |
| 0,23 | 57,0 | 0,36 | 24,6 | 0,49 | 10,7 |
| 0,24 | 53,4 | 0,37 | 23,1 | 0,50 | 10,0 |
| 0,25 | 50,1 | 0,38 | 21,7 | 0,51 | 9,4 |
Существуют и другие, более точные, способы эхокардиографи ческого определения систолического и диастолического давления в легочной артерии.
| 2.5.6. Ультразвуковая флебография |

|
 Запомните
Ультразвуковыми признаками застоя крови в венозном русле большого круга кровообращения являются: уменьшение коллабирования нижней полой вены во время глубокого вдоха менее чем на 50%; расширение портальных вен (печеночной, воротной, брыжеечной, селезеночной) и уменьшение их опорожнения во время вдоха. Запомните
Ультразвуковыми признаками застоя крови в венозном русле большого круга кровообращения являются: уменьшение коллабирования нижней полой вены во время глубокого вдоха менее чем на 50%; расширение портальных вен (печеночной, воротной, брыжеечной, селезеночной) и уменьшение их опорожнения во время вдоха.
|
| 2.5.7. Дополнительные инструментальные методы исследования |

|
- радионуклидная вентрикулография;
- катетеризация правых отделов сердца плавающим катетером Свана-Ганца с измерением давления в камерах сердца и ЛА, в том числе определение ЦВД и давления “заклинивания” ЛА (ДЗЛА) (см. главу 6);
- нагрузочная сцинтиграфия миокарда с 201Tl для количественной оценки нарушений коронарной перфузии (см. главы 5 и 6);
- коронароангиография (КАГ) для всесторонней оценки состояния коронарного русла.
| 2.6. Лечение хронической систолической сердечной недостаточности |

|
- больные с различными причинами возникновения ХСН;
- больные с явными клиническими симптомами и сниженной систолической функцией ЛЖ (снижением ФВ и СИ по данным эхокардиографического исследования);
- больные с клинической симптоматикой СН, но без признаков систолической дисфункции (диастолическая ХСН);
- больные с бессимптомной дисфункцией ЛЖ (снижение ФВ и СИ без клинических признаков СН) и т.п.
| 2.6.1. Этиологическое лечение |

|
- артериальная гипертензия (нормализация АД);
- бради- и тахиаритмии (коррекция нарушений сердечного ритма и проводимости);
- злоупотребление алкоголем (прекращение приема алкоголя);
- ожирение (снижение массы тела);
- пороки сердца (хирургическая коррекция порока);
- тиреотоксикоз или микседема (адекватная коррекция гормональных нарушений);
- экссудативный или констриктивный перикардит (адекватная терапия или хирургическое лечение);
- ИБС (адекватно подобранная антиангинальная терапия или внутрикоронарная ангиопластика и аортокоронарное шунтирование);
- анемии (восстановление содержания эритроцитов и гемоглобина);
- хронические обструктивные заболевания легких (противовоспалительная терапия, лечение обструктивного синдрома).
| 2.6.2. Устранение факторов, провоцирующих ухудшение состояния больных ХСН |

|
- несоблюдение врачебных рекомендаций (избыточное потребление соли, жидкости, нарушение схемы приема лекарственных средств и др.);
- нарушение индивидуального режима физической активности;
- инфекции;
- употребление алкоголя;
- острый ИМ, нестабильная стенокардия;
- ТЭЛА;
- преходящие расстройства электролитного обмена (гипокалиемия, гипофосфатемия, гипокальциемия и др.);
- беременность и роды;
- возникновение пароксизмов или постоянной формы мерцательной аритмии;
- дисфункция щитовидной железы.
| 2.6.3. Немедикаментозное лечение |

|
 Запомните
При отсутствии признаков обострения заболевания, в частности прогрессирующей левожелудочковой недостаточности или нарастающего отечного синдрома, неоправданно длительное и резкое ограничение физической активности, строгий постельный или полупостельный режим у большинства больных ХСН быстро приводят к развитию синдрома детренированности, значительным структурным изменениям скелетных мышц и прогрессирующему снижению толерантности к нагрузкам. Запомните
При отсутствии признаков обострения заболевания, в частности прогрессирующей левожелудочковой недостаточности или нарастающего отечного синдрома, неоправданно длительное и резкое ограничение физической активности, строгий постельный или полупостельный режим у большинства больных ХСН быстро приводят к развитию синдрома детренированности, значительным структурным изменениям скелетных мышц и прогрессирующему снижению толерантности к нагрузкам.
|
Физическая реабилитация пациентов с ХСН должна учитывать степень функциональных нарушений. Наиболее эффективны физические тренировки, организуемые для больных ХСН в специальных кардиологических и реабилитационных центрах, которые осуществляются под постоянным врачебным контролем за гемодинамикой и другими показателями. Однако более доступны самостоятельные физические упражнения, объем и интенсивность которых индивидуально определяются лечащим врачом.
|
|
|


