 |
Разработка теоретических основ технологии получения экологически чистых нанопокрытий нового поколения с использованием сплавов на основе металлов группы железа
|
|
|
|
Реферат
Тема: «Разработка методов получения и обработки наноматериалов и структур, обладающих улучшенными функциональными свойствами».
подтема 1 «Получение, исследование свойств и определение области рационального применения нанокристаллических электрохимических покрытий из металлов группы железа с тугоплавкими металлами»,
этап 1.4 «Разработка теоретических основ технологии получения экологически чистых нанопокрытий нового поколения с использованием сплавов на основе группы железа»
Отчет на 54 страницах машинописного текста, 18 рисунков, 3 таблицы, список используемых источников содержит 13 наименований.
Ключевые слова: гель-хроматография, электроосаждение, борглюконатный электролит, нанокристаллические кобальт-вольфрамовые сплавы, анодное растворение, микротвердость Co-W покрытий, растворимые аноды.
Сочетанием гель-хроматографического разделения глюконатного электролита для получения нанокристаллических Co-W покрытий, электрохимических методов и результатов электронной микроскопии получены новые данные о механизме индуцированного соосаждения металлов группы железа с вольфрамом (на примере Co-W покрытий, электроосажденных из глюконатного раствора), свидетельствующие в пользу механизма, основанного на определяющей роли поверхностного восстановления интермедиата вольфрама, содержащего глюконат.
Показано, что обнаруженный ранее на примере электроосаждения Сo-W покрытий размерный эффект микротвердости, наблюдается также для Ni-W и Fe-W покрытий.
Показана возможность использования для получения нанокристаллических Co-W покрытий растворимых кобальтового и вольфрамового анодов. Экспериментально установлен факт существенного повышения работоспособности глюконатного электролита при электроосаждении Co-W при использовании растворимого вольфрамового анода.
|
|
|
В рамках сотрудничества между ПГУ им. Т.Г.Шевченко и Технопарка “Сколково” разработан инновационный проект “Технология получения упрочняющих коррозионностойких покрытий из сплавов группы железа с вольфрамом”, который в настоящее время проходит экспертизу.
Содержание
Введение.. 8
Глава 1. Исследование процесса электрохимической нуклеации и создание ее статистической модели. 10
1.1. Расчет термодинамических функций. 11
1.2. Расчет кинетики процесса нуклеации. 19
1.3. Выводы.. 21
Литература. 21
Глава 2. Исследование процессов управления составом и свойствами поверхности обеспечивающих снижение антропогенного воздействия на окружающую среду. 22
2.1. Исследование и разработка методов электроосаждения из экологически чистых электролитов на основе солей кобальта и вольфрама в условиях индуцированного осаждения сплавов 22
2.1.1. Методика исследования микро- и макрораспределение скоростей осаждения нанокристаллических Co-W покрытий из цитратных растворов. 22
2.1.2. Методы анализа поверхности и определения ее механических свойств. 26
2.1.3. Природа кинетических ограничений скорости осаждения. 27
2.1.4. Влияние гидродинамических условий на скорость осаждения. 28
2.1.5. Гидродинамические условия и морфология покрытий. 30
2.1.9. Рассеивающая способность электролита. 34
2.1.10. Микротвердость покрытий. 35
Литература. 37
Глава 3. Разработка методов повышения коррозионной и износостойкости поверхности при локальной электрохимической размерной обработке. 39
3.1. Микрообработка СоW покрытий в нитратных и нитратно-щелочных растворах. 39
3.1.1. Анодное растворение поликристаллических покрытий с малым содержанием вольфрама в нитратном растворе. 39
3.2. Анодное растворение нанокристаллических покрытий с высоким содержанием вольфрама в нитратном растворе. 44
|
|
|
3.3. Анодная обработка в нитратно-щелочном растворе. 50
3.4. Изменение микротвердости поверхности после обработки. 53
3.5. Выводы.. 58
Литература. 59
Глава 4. Разработка методов управления функциональными свойствами электрохимических покрытий, обеспечивающих снижение антропогенного воздействия на окружающую среду. 61
4.1. Микрообработка азотированных поверхностей стали, полученных электрохимико-термической обработкой, в хлоридных растворах. 61
4.1.1 Анодное растворение термообработанной и азотированной поверхностей. 61
4.2. Макрокинетика анодного растворения поверхностей. 74
4.3. Влияние плотности тока на шероховатость поверхности. 79
4.4. Микротвердость поверхности после анодного растворения в хлоридах. 84
4.5. Разработка рекомендаций по применению процессов анодного растворения упрочняющих электрохимических покрытий при их микрообработке в электролитах, обеспечивающих снижение антропогенного воздействия на окружающую среду. 87
4.6. Выводы.. 89
Литература. 92
Глава 5. Прогнозирование направления исследований и инновационной деятельности в области электрохимии и электрохимической технологии, в том числе на территории ПМР. 94
5.1.Наукометрический анализ взаимного влияния процессов социально-экономического и научного (информационного) развития общества. Место исследователей Молдовы и Приднестровья в мировом информационном процессе. 94
5.2. Динамика мирового информационного процесса в области электрохимии. Роль исследователей Молдовы (в том числе. 112
Приднестровья) в этом процессе. 112
5.3. Анализ электрохимических технологий, используемых на предприятиях ПМР. 118
5.4. Выводы.. 121
Литература. 122
Общие выводы... 123
Приложения.. 124
Перечень условных обозначений
ВДЭ - вращающийся дисковый электрод
ВЦЭ - вращающийся цилиндрический электрод
ЦЭ - цилиндрический электрод
i и i ср - соответственно текущая и средняя по поверхности плотности тока
k - электропроводность электролита
L - характерный линейный размер
С0 - концентрация электроактивных частиц
n - кинематическая вязкость
D - коэффициент диффузии
F - константа Фарадея
n - число переносимых электронов в электрохимической реакции
|
|
|
mx - локальное значение толщины покрытия
hx - локальное значение выхода металла по току
С - электрохимический эквивалент
r - плотность
t - время обработки
ix - локальная плотность тока
iv - объёмная плотность тока
Введение
Актуальность и новизна темы. Развитие электрохимических технологий в настоящее время происходит в нескольких направлениях. Одно из них обусловлено необходимостью разработки технологий получения и обработки материалов, обладающих новыми функциональными свойствами (высокой износостойкостью и коррозионностойкостью, электропроводностью, твердостью и т.д.). Второе связано с необходимостью разработки технологий, обеспечивающих уменьшение нагрузки на окружающую среду. Одной из основных целей настоящего исследования было сочетание этих двух направлений, т.е. разработка основ технологических процессов получения материалов и покрытий, обладающих уникальными функциональными свойствами, в условиях обеспечивающих снижение нагрузки на окружающую среду. Одной из классических электрохимических технологий, широко применяемых в настоящее время в промышленности, является технология электролитического хромирования, которая относится к экологически вредным технологиям. В настоящее время ведутся интенсивные попытки разработки технологий обеспечивающих получение покрытий обладающих подобными свойствами, но при существенно меньшей нагрузке на окружающую среду. В настоящем исследовании показаны возможности использования CoW покрытий, получаемых из экологически чистого электролита как альтернативы замены электролитическому хрому. Примечательной особенностью таких покрытий является то, что они нанокристаллические. Конечной целью проводимого исследования является разработка технологии таких покрытий и определение их области рационального использования в промышленности. Настоящий отчет посвящен созданию теоретических основ такой технологии. На базе этой работы разработан инновационный проект технологии электрохимических упрочняющих покрытий металлов группы железа с вольфрамом, который в рамках сотрудничества ПГУ им. Т.Г. Шевченко и технопарка «Сколково» передан на экспертизу для получения дополнительного финансирования.
|
|
|
Разработка теоретических основ технологии получения экологически чистых нанопокрытий нового поколения с использованием сплавов на основе металлов группы железа
Анализ существующих технологий получения экологически чистых электрохимических нанокристаллических покрытий нового поколения с использованием сплавов на основе металлов группы железа с тугоплавкими металлами
Проведенный в отчетном году анализ, показал следующее. Получение упрочняющих и коррозионностойких покрытий является продолжающимся трендом современного материаловедения. Эффективным методом решения подобной задачи является использование электрохимических методов. Электрохимическое материаловедение – один из наиболее развивающихся в настоящее время разделов материаловедения, поскольку, являясь относительно дешевыми, электрохимические методы позволяют управлять не только составом, но и структурой покрытия.
В настоящее время основным процессом, решающим подобного рода задачи (упрочнения поверхности, повышения ее коррозионной стойкости и др.), является процесс электрохимического хромирования. Однако, этот процесс является экологически вредным. Следствием этого были, в частности, несколько директив Европейской комиссии, запрещающих или ограничивающих использование этой технологии на территории Европейского Союза [1, 2]. Также, в США существует программы стратегических исследований в области защиты окружающей среды (Strategic Environmental Research and Development Program (SERDP) and Environmental Security Technology Certification Program (ESTCP)) одной из задач которых является поиск материалов для замены электролитического хрома.
Вследствие этого в различных странах осуществляется поиск электрохимических систем, на основе которых возможно создание промышленной технологии, способной заменить процесс хромирования [3,4].
Одним из вариантов решения задачи является разработка технологии получения упрочняющих коррозионностойких покрытий с использованием сплавов металлов подгруппы железа (Fe,Co,Ni) с вольфрамом. Электроосаждение подобных покрытий относится к категории аномального электроосаждения [5]. Механизм подобных процессов является предметом активных научных дискуссий, что может служить подтверждением актуальности подобной проблемы. Дополнительным стимулом исследований и разработок в этом направлении является то, что электролиты используемые (пока еще в исследовательской практике), являются существенно более экологически чистыми в сравнении с традиционно применяемыми в процессах электроосаждения. Как правило, это цитратные и глюконатные растворы.
|
|
|
Как показано в ряде работ [3,4] микротвердость таких материалов может достигать 1000кГ/мм2, а коэффициент трения быть меньше чем 0,1. Неоднократно отмечалась высокая коррозионная стойкость получаемых покрытий [3-5]. В то же время достигаемые в этих работах значения микротвердости, могут существенно варьировать [4], что объясняется недостаточно контролируемыми условиями проведения эксперимента.
Таким образом, в настоящее время проводится большое количество исследований, посвященных различным аспектам применения технологии получения покрытий из сплавов металлов группы железа с вольфрамом при решении различных задач: получение упрочняющих покрытий, улучшение магнитных свойств, повышение коррозионной стойкости, повышение каталитической способности в реакции получения водорода. Обзору этих исследований посвящены работы [4, 5]. Однако все эти исследования находятся пока на этапе лабораторных технологий и не перешли на уровень промышленных технологий. Одним из главных недостатков этих технологий является плохая воспроизводимость и неопределенность критических параметров процесса.
Плохая же воспроизводимость обусловлена тем, что механизм этих процессов до сих пор является предметом дискуссий. За прошедший год Лабораторией НИЛ ЭХП получены новые данные относительно механизма их получения на основе результатов гель-хроматографического разделения электролита на составляющие и определения их электрохимической активности с использованием циклической вольтамперометрии (CVA).
4.1.1 Гель-хроматографическое разделение глюконатного электролита для получения нанокристаллических Co-W покрытий и определение их электрохимической активности.
4.1.1.1 Методика
Использованная методика гель-хроматографического разделения электролита была близка к описанной в [6,7], однако, по сравнению с описанной ранее, была существенно модифицирована.
Измерение, стабилизация скорости потока и подготовка элюента. Фиксация скорости потока осуществлялась гравиметрическим методом. Емкость с элюентом (водой) взвешивалась на электронных весах BEL M1702l, сопряженных с компьютером, что обеспечивало автоматическую регистрацию изменения массы. Регистрация значений массы пропущенного растворителя осуществлялась по команде компьютера и точно соответствовала значению оптической плотности раствора в текущий момент. Таким образом, мы получили не усредненное значение скорости прокачки носителя, а мгновенное значение количества прошедшего растворителя для каждой измеряемой точки. Такой подход позволил значительно повысить воспроизводимость положения и формы хроматографических пиков. Для стабилизации скорости прокачки элюента через колонку перед ней в систему была включена эластичная трубка из тонкой резины, которая играла роль демпфера и компенсировала пульсации, возникавшие в процессе работы перистальтического насоса. В процессе проведения экспериментов в хроматографической колонке спектрофотометра накапливалось некоторое количество воздуха, выделяющегося из воды, что приводило к формированию воздушных полостей, нарушающих нормальную работу колонки. Резкое падение давления растворителя на выходе из хроматографической колонки воздуха и в кювете приводило к ошибкам при регистрации оптической плотности. Чтобы избежать этих негативных факторов проводили деаэрацию воды, путем ее длительного кипячения непосредственно перед экспериментом с последующим охлаждением, в сосуде с минимальной свободной поверхностью.
Состав сорбента хроматографической колонки также был изменен. Сорбент Bio-Gel P-4 с диаметром гранул 50 – 150 меш и пределом исключения молекул из гранул <3600, использовавшимся в предыдущей работе, был заменен на Bio-Gel P-2 с большим диаметром гранул (200 – 400 меш) и меньшим пределом исключения молекул из гранул (<1600), что позволило улучшить степень деления исследуемого раствора.
Способ измерения оптической плотности раствора, проходящего через колонку, тоже был модифицирован. Спектрофотометр Specord M40 был переоборудован для компьютерной записи результатов измерений. В режиме реального времени хроматограмма записывалась в файл и выводилась на экран монитора в координатах «количество пропущенного элюента (время) – оптическая плотность».
Для контроля воспроизводимости результатов и качества деления хроматографической колонки в каждую вносимую в колонку пробу добавлялось 0,1 мл водного раствора BSA (бычий сывороточный альбумин), не взаимодействующего с компонентами раствора электролита и выполняющего роль репера. Положение пика этого белка соответствует свободному объему колонки и позволяет судить о работоспособности всей системы.
4.1.1.2 Результаты гель-хроматографического разделения
На рис.4.1 представлена типичная хроматограмма бор – глюконатного электролита, использованного для получения Co-W покрытий и состоящего из (моль/л): CoSO4 – 0,053, Na2WO4 – 0,05, глюконат натрия – 0,55, борная кислота – 0,65, хлорид натрия – 0,51

Рис. 4.1 Гель-хроматограмма бор-глюконатного электролита.
Как видно из рис., при использовании данного метода разделения имеет место разделение на 3 фракции в соответствии с различным молекулярным весом отдельных фракции (фракции с более высоким молекулярным весом выходят из колонки раньше).Из результатов, представленных на рис. 4.2, видно, что образуются глюконатные комплексы не только с W и Co, но и комплекс с хлоридом натрия, а также образуется бор – глюконатный комплекс.

Рис.4.2 Гель-хроматограммы составляющих электролита.
Очевидно, что третий пик на гель-хроматограмме рис.4.1 связан с наличием хлорид – глюконатного комплекса, а первый и второй включает бор – глюконатный.

Рис.4.3 Сравнение гель-хроматограмм, содержащих только соль кобальта и только вольфрамат при наличии в растворе также остальных компонентов.
Результаты гель-хроматографического разделения, представленные на рис.4.3, свидетельствуют в пользу того, что первый пик на хроматограмме рис.4.1 соответствует кобальтовому комплексу, а второй – глюконатному комплексу с вольфрамом.
Полученные результаты позволили перейти к препаративному разделению составляющих на три фракции. На рис.4.4 представлены объемы элюирования, из которых отбирались фракции. При препаративном разделении из первой фракции отбирался объем ~ 7 мл, из второй фракции также 7 мл, а из третьей ~ 9мл. Всего было проведено 17 делений. Затем каждая из фракций концентрировалась в роторном испарителе (объем доводился до ~ 50 мл) и полученный раствор подвергался анализу на содержание W и Co (методика определения описана в [6,7]), после чего проводилось исследование электрохимической активности фракций методом СVA.

Рис. 4.4 Разделение электролита на фракции.
Табл.4.1 Содержание W и Co во фракциях после гель – хроматографического разделения
| Фракция | Co, мг | W, мг | Co: W (ат. %) |
| 6.636 | 3.02 | 6.8: 1 | |
| 2.658 | 23.824 | 1: 2.9 | |
| 0.3182 | 4.696 | 1: 4.7 | |
| Сумма, мг: | 9.61 (93%) | 31.54 (98%) | |
| Всего внесено в колонку, мг | 10.325 | 32.2 |
Результаты, представленные в табл. 4.1, показывают, что если первая фракция представляет собой кобальтовый комплекс, “загрязненный” вольфрамом, то вторая и третья фракции - вольфрамовые комплексы, “загрязненные” кобальтом. Данные, представленные в табл., свидетельствуют также о точности анализа (наличие баланса по кобальту и вольфраму). Видно, что с точностью 2-7 % такой баланс между содержанием кобальта и вольфрама, внесенного в колонку, и обнаруженного после фракционного разделения, наблюдается.
4.1.1.3 Результаты исследования электрохимической активности продуктов деления
На рис.4.4 представлены циклические вольтамперограммы исследования электрохимической активности полученных фракций. Использовались следующие циклы: от OCP в катодную сторону до – 1,3 В и затем обратно в анодную до + 1,00 В (нас. Ag/AgCl электрод). Наличие анодных пиков свидетельствует в пользу электроосаждения металла из определенной фракции.
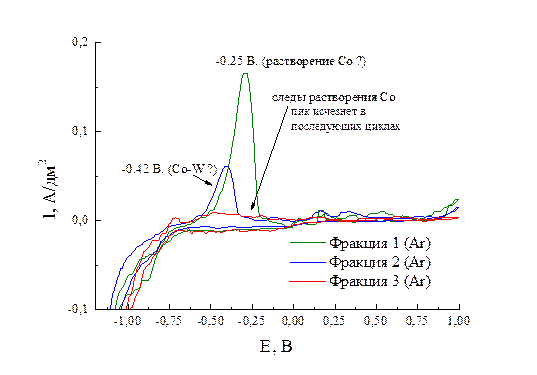
Рис.4.5 Циклические вольтамперограммы фракций.
Видно, что и из первой фракции и из второй (но не из третьей) происходит осаждение покрытия, анодно растворяющегося в анодном цикле. Причем, анодное растворение из второй фракции происходит с меньшим перенапряжением, но количество осажденного вещества из первой фракции больше (рис.4.5). Однако на основе циклических вольтамперограмм нельзя дать ответ на вопрос какая фаза образуется при восстановлении (и соответственно, нельзя дать ответ на вопрос какой фазе соответствуют пики анодного растворения).
С целью ответа на этот вопрос проводили потенциостатическое осаждение при потенциале -0,9 В как из первых двух фракций, так и из полного электролита. При этом, на основе результатов увеличения веса образцов определяли выход по току. В полном соответствии с результатами CVA выход по току при осаждении из первой фракции оказался более чем вчетверо больше, чем при осаждении из второй (соответственно, ~ 37% и ~ 9%). Результаты электронной микроскопии с использованием EDS анализа (рис.4.6-4.8) показали, что в отличие от электроосаждения из полного электролита при электроосаждении из отдельных фракций осаждается только Со.
Этот факт является принципиально важным с точки зрения механизма индуцированного соосаждения металлов группы железа с вольфрамом.
|
|
|


