 |
Альдегидо - кетонная перегруппировка
|
|
|
|
Общие сведения о перегруппировке
Альдегидо- кетонная перегруппировка основана на превращении альдегидов в изомерные кетоны, сопровождающаяся обменом водорода альдегидной группы на соседний углеводородный радикал под действием протонных кислот (кислот Льюиса, серной и т. д.)
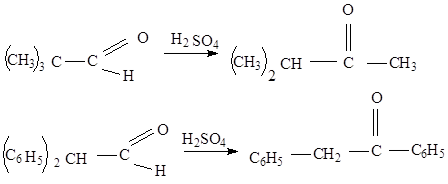
Альдегидо- кетонная перегруппировка является нуклеофильной, интрамолекулярной, стереоспецифической, протекает с миграцией от атома углерода к другому атому улерода (от С-С), с изомеризацией в насыщенных системах.(16)
Механизм перегруппировки.
Механизм превращения альдегидов в кетоны сходен с механизмом ретропинаколиновой перегруппировки и может быть представлен следующей схемой:

1.Благодаря неподеленной паре электронов на атоме кислорода альдегиды обладают основными свойствами и реагируют с кислотами.
При взаимодействии с протонными кислотами альдегиды (I) присоединяют протон, вследствии чего образуется σ – связь ОН(II.) В результате возрастает электрофильность углеродного атома карбонильной группы(17).
2.Т.к. α- углеродный атом в соединении (II) связан с радикалом, который за счет резонансных факторов, эффекта гиперконьюгации, имеет неподеленную пару, то данная пара начинает выступать в качестве нуклеофила. При этом начинает образовываться связь между радикалом, находящимся у α- углеродного атома и карбкатионным углеродом, при этом одновременно происходит разрыхление связи между α- углеродным атомом и радикалом при нем. В результате образуется неустойчивое соединение (III).
3.В результате происходит образование вторичного катиона на α- углеродном атоме (IV).В дальнейшем происходит регенирация протона с образованием соединения (V),которое по правилу Эльтекова- Эйленмеера является неустойчивым, т.к. образуется система, в которой у одного атома углерода находятся двойная связь и гетероатом, несущий неспаренную пару электронов.
|
|
|
4.Таким образом, соединение (V), вследствии своей неустойчивости изомеризуется с образованием кетона.
Пинаколиновая перегруппировка
Общие сведения о пергруппировке.
Катализируемая минеральными кислотами перегруппировка 1, 2- диолов называется пинаколиновой перегруппировкой (18). Данная перегруппировка является нуклеофильной, интрамолекулярной, протекает без изомеризации в алифатическом ряду с миграцией от атома углерода к другому атому углерода. Движущей силой реакции является отщепление молекулярного азота, а содействующим фактором - легкий отрыв протона от кислорода, что в итоге приводит к стабильной молекуле.
Механизм перегруппировки.

Многочисленные исследования различных замещенных гликолей и 1,2- аминоспиртов показали, что мигрирующая группа (Н, алкил, арил, галоген) выполняет роль нуклеофильного реагента, атакуя (+) заряженный атом углерода, возникающий после отщепления одного из протонированных гидроксилов.(19)
При этом установлено, что перескакивающий заместитель подходит к атому углерода всегда со стороны, противоположной положению потерянного гидроксила. Это означает, что в карбкатионе вращение С-С- связи отсутствует, вероятно, вследствии сильного донорно- акцепторного взаимодействия оставшегося –ОН с носителем (+)- заряда. Мигрирующая группа (Н, СН3, С6Н5 и др.) в переходном состоянии связана с обоими атомами углерода трехцентровой связью. Второй гидроксид- ион, сыграв свою активную роль стабилизатора карбкатиона вновь возвращается к своему (С1) атому углерода, но уже в виде протонированой С=О- группы.
Перегруппировка требует энергетических затрат на разрыв одной сигма- связи (С1- R) и перераспределение электроной плотности между химическими связями. Установлено, что результат перегруппировки для несимметрично замещенных гликолей сильно зависит от конформации заместителей и всей молекулы в целом.
|
|
|
На основании выше сказанного можно сделать вывод, что рассмотренная перегруппировка является нуклеофильной, стереоспецифической, внутримолекулярной.
Расчленение на стадии здесь дано искусственно, для ясности.
Подробно изучено, какие радикалы в этой перегруппировке легче мигрируют. В порядке легкости миграции радикалы располагаются в следующий ряд:
п-CH3OC6H4 > п-CH3C6H4 > п-ClC6H4 > Алкилы > H
Общий вывод таков: легче мигрирует радикал, в наибольшей степени рассредоточивающий положительный заряд, появившийся в системе в результате отрыва -ОН, или, другими словами, легче мигрирует радикал, наиболее способный подвергнуться электрофильной атаке. То обстоятельство, что начальным моментом перегруппировки является отрыв гидроксильного аниона и образование карбониевого катиона (в переходном состоянии тотчас рассредоточивающего свой заряд между С, от которого оторван гидроксил, соседним С скелета и ключевым С мигрирующей R'-группы), доказывается следующими аналогиями:
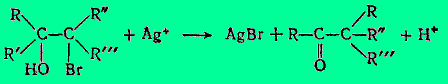
(Здесь даны только исходный бромгидрин и конечный пинаколин; механизм, очевидно, тот же.)
Еще одна аналогичная перегруппировка - «окислительное дезаминирование» Мак-Кензи:

Движущей силой реакции является отщепление молекулярного азота, а содействующим фактором - легкий отрыв протона от кислорода, что в итоге приводит к стабильной молекуле.
Общий механизм реакции можно выразить одной схемой синхронного превращения:
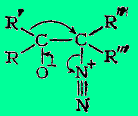
|
|
|


