 |
Общие сведения о перегруппировке.
|
|
|
|
Перегруппировка Демьянова относится к перегруппировке в ненасыщенных системах, основанной на расширении или сужении цикла на один атом углерода при превращении алициклических или гетероциклических первичных аминов в спирты под действием азотистой кислоты (20). Данная перегруппировка является внутримолекулярной (интра-), т.е. разрыв старых связей и образование новых происходит синхронно; является нуклеофильной; протекает с миграцией от атома углерода к другому атому углерода (от С-С); протекает с участием карбкатиона.
При рассмотрении перегруппировки Демьянова следует учитывать устойчивость циклов, то есть то, что шестичленные и пятичленные циклы энергетически наиболее устойчивы чем трехчленные, четырехчленные и т.д. Поэтому при рассмотрении расширения или сужения циклов в результате перегруппировки следует иметь в виду теорию устойчивости циклов.
Так, например, при действии азотистой кислоты на циклогексилметиламин (I) образуется смесь циклогексилкарбинола I(III) и циклогептанола (смесь изоборнеона) (IV).
Эта же смесь спиртов образуется и при действии азотистой кислоты на циклогептиламин (II):

Механизм перегруппировки.
Механизм перегруппировки Демьянова аналогичен механизму пинаколиновой и ретропинаколиновой перегруппировок.
Так, образование циклогексилкарбинола при действии азотистой кислоты на циклогексилметиламин (I) может быть объяснено следующей схемой:

| |
Однако карбониевый ион (V) может претерпевать перегруппировку типа ретропинаколиновой, в результате чего возникает карбониевый катион (VI), а из него- циклогептанол:

|
Т.е. пара электронов как нуклеофил атакует атом углерода, на котором находится недостаток электронной плотности, причем образование новой связи и разрыв старой происходит синхронно, т. е. перегруппировка является внутримолекулярной.
|
|
|
При действии азотистой кислоты на циклогептиламин образуется карбониевый катион (VI), который реагирует с водой, дает циклогептанол:
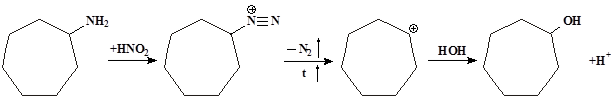
А претерпевая перегруппировку типа пинаколиновой, образует карбониевый ион (V), и из него циклогексилкарбинол:

Побочные реакции.
Перегруппировка Демьянова может сопровождаться образованием олефинов за счет отщепления протона от карбониевых ионов (V), (VI) или (VII):

Реагирует ли азотистая кислота с циклогексилметиламином или циклогептиламином, в реакционной смеси устанавливается равновесие между карбониевыми ионами 5 и 6. Это является причиной образования одинаковой смеси спиртов в обоих случаях. Таким образом, в данной перегруппировке побочная реакция-образование циклических олефинов.
Сужение и расширение циклов наблюдается не только при реакции олефинов с азотистой кислотой, но и в других случаях, когда образуются карбониевые ионы.
Н.Я.Демьянов и Н.М.Кижнер установили, что при действии бромистоводородной кислоты на циклопропилкарбинол образуется циклопропилбромметан и бромциклобутан, из циклобутанола при действии бромистоводородной кислоты получается циклопропилкарбинол:

Перегруппировка Наметкина.
Общие сведения о перегруппировке.
Переход α-метилкамфена в 4-метилизоборнеол в условиях кислотного катализа называется перегруппировкой Наметкина, иначе ее называют камфеновой перегруппировкой второго рода. Данная перегруппировка наблюдается в ряду терпенов.(21)
Механизм перегруппировки.
Камфеновая перегруппировка второго рода была открыта Наметкиным и Брюсовой.

Механизм перегруппировки Наметкина заключается в изомеризации углеродного скелета по типу ретропинаколиновой или, при обратном процессе, - пинаколиновой перегруппировки.
|
|
|
Рассмотрим механизм:
1.К α-метилкамфену (I) идет присоединение воды по двойной связи в соответствии с правилом Марковникова (II).
2.Дальнейшая протонизация дает оксониевый ион (III). Как известно, вода – это хорошо уходящая группа. Вследствие этого, соединение (III) превращается в открытый карбкатион (IV).
3.Затем собственно здесь начинается перегруппировка: атака нуклеофила (пары электронов) по положительному реакционному центру. То есть миграция группы, имеющей избыток электронов (÷СН3) к атому, несущему положительный заряд (карбкатион), стабилизация карбкатиона, одновременный уход ÷СН3 группы и атака его по карбкатиону обуславливает тот факт, что данная перегруппировка является внутримолекулярной (интрамолекулярной).
4. В месте ухода÷СН3 группы появляется новый реакционный центр, который может сразу перейти в конечный продукт (4-метилиззоборнеол), либо сразу при взаимодействии с водой, либо претерпевающий перегруппировку (VII).
Таким образом, перегруппировка Наметкина является нуклеофильной, внутримолекулярной перегруппировкой.
|
|
|


