 |
7.3.2. Задачи для самостоятельной работы.
|
|
|
|
7. 3. 2. Задачи для самостоятельной работы.
Разбор типовой задачи
Найти поверхностное натяжение бутанола при 298оС, если число капель из сталагмометра для этанола составило 76, а для воды 29 капель, s(Н2О)=73× 10-3 Дж/м2.
Решение:
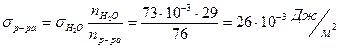
2. Задачи для самостоятельной работы
1. При адсорбции уксусной кислоты из 1л водного раствора 50г угля концентрация кислоты уменьшилась с С0=1, 4 М до С1=1, 25М. Найдите удельную адсорбцию и степень адсорбции в %.
2. Во сколько раз поверхностная активность пентанола больше, чем у этанола?
3. Вычислите длину и площадь молекулы изоамилового спирта (СН3)2СН2СН2СН2ОН, если Г∞ =7· 10-6моль/м2, плотность спирта 0, 81· 106г/м3.
4. Сравните поверхностную активность пропионовой и масляной кислот. Выполняется ли правило Траубе-Дюкло?
| Кислота | С, моль/л | σ, мН/м |
| Пропионовая | 0, 0312 | 69, 5 |
| 0, 0625 | 67, 7 | |
| Масляная | 0, 0312 | 65, 8 |
| 0, 0625 | 60, 4 |
5. При уменьшении концентрации новокаина в растворе с 0, 2 моль/л до 0, 15моль/л поверхностное натяжение возросло с 6, 9∙ 10-2 Дж/м2 до 7, 1∙ 10-2 Дж/м2, а у раствора кокаина с 6, 5∙ 10-2 Дж/м2 до 7, 0∙ 10-2 Дж/м2. Сравните величины адсорбции двух веществ в данном интервале концентраций при 293° К. Для какого вещества она больше?
6. Концентрация кетоновых тел, накапливаемых в крови больных сахарным диабетом в течении суток, достигает 0, 2 моль/л. Какое количество кетоновых тел адсорбируется из крови при гемосорбции, если емкость адсорбента равна Г∞ =3· 10-3моль/г, α =6· 10-2моль/л в уравнении Ленгмюра: Г= Г∞ С/(α +С).
7. Концентрация холестерина в плазме крови после проведения гемосорбции снизилась с 4, 8 до 4, 0 мкмоль/мл. Чему равна емкость данного адсорбента по холестерину (Г∞ в мкмоль/г), если объем плазмы равен 1 л, а масса сорбента = 10г?
|
|
|
7. 4. Контроль усвоения темы занятия.
Образец билета выходного контроля.
1. Межфазное взаимодействие между контактирующими поверхностями конденсированных тел разной природы
1) электрофорез; 2) когезия; 3) диализ;
4) адгезия; 5) коагуляция.
2. Поверхностно – активные вещества
1) NaCl; 2) C17H33COONa; 3) C2H5NH3Cl;
4) H2SO4 5) O2 .
3. Во сколько раз поверхностная активность бутанола больше, поверхностной активности метанола.
1) в 3 раза; 2) в 6 раз; 3) в 9 раз 4) в 27 раз.
4. На поверхности костной ткани Са3(РО4)2 в первую очередь адсорбируютсяионы:
1) Са2+; 2) Na+; 3) HPO42-; 4) Cl- 5) HCO3-.
5. Динамический метод анализа и разделения веществ, в котором имеется 2 фазы: неподвижная и подвижная, фильтрующаяся через неподвижную.
1) ионный обмен; 2) хроматография; 3) кондуктометрия;
4) титрование; 5) диализ.
7. 5. Подведение итогов занятия.
7. 6. Задание на дом: Получение и свойства коллоидных растворов.
Место проведения самоподготовки: читальный зал и др.
Литература. [1], [2].
Занятие №13
Тема: Получение и свойства коллоидных растворов.
1. Актуальностьтемы: Ткани организма- это коллоидно-дисперсныесистемы. Кровь представляет собой систему, состоящую из плазмы и кровяных клеток(в основном, эритроцитов). Кровь можно рассматривать как грубодисперсную свободнодисперсную лиофобную стабилизированную систему типа твердая фаза в жидкой среде. Стабилизаторами являются белки, макроионы которых адсорбируются на поверхности эритроцитов и придают им отрицательный заряд. Кости - это система с твердой дисперсионной средой, в которых газовые, жидкостные или твердые включения распределены в объеме твердой фазы или образуют непрерывную систему взаимных прослоек и каналов в непрерывной твердой фазе.
|
|
|
2. Учебные цели: Научиться получать коллоидные растворы различными методами, эмульсии – методом диспергирования. Ознакомиться методами очистки коллоидных растворов и определением знака заряда коллоидных частиц.
Для формирования профессиональных компетенций обучающийся должен знать
-правила работы в химической лаборатории с реактивами и приборами
-классификацию дисперсных систем, способы их получения, особенности строения коллоидных частиц
уметь
- производить расчеты и оценивать их результаты
-определять заряд гранулы по результатам расчетов
-написать условную формулу коллоидной частицы и определять ее составные частицы
владеть
-самостоятельной работой с учебной и справочной литературой
-безопасной работы в химической лаборатории и обращаться с химической посудой и реактивами
3. Материалы для самоподготовки к усвоению данной темы.
Вопросы для самоподготовки к занятию:
1. Классификация дисперсных систем.
2. Основные способы получения коллоидных дисперсных растворов и эмульсий.
3. Методы очистки дисперсных систем.
4. Основные свойства дисперсных систем: молекулярно-кинетические; оптические и электрические.
5. Строение мицелл.
6. Механизм возникновения электрического заряда коллоидных частиц.
7. Методы определения знака заряда коллоидных частиц.
4. Вид занятия: лабораторное занятие
5. Продолжительность занятия: 3 академических часа.
|
|
|


