 |
Определение содержания фосфатов в почве
|
|
|
|
Теоретическая часть
Фосфор наряду с азотом относится к биогенным элементам. Оба эти элемента являются составной частью всех тканей живых организмов.
Фосфор играет исключительно важную роль в процессах обмена энергии.
Кроме того, фосфат-ион регулирует направленность внутриклеточных процессов окисления. Вследствие этого недостаток в окружающей среде фосфора может быть фактором, лимитирующим процессы жизнедеятельности. Вместе с тем избыточное накопление фосфатов в почве приводит к загрязнению грунтовых вод и природных водоёмов. Цель данной лабораторной работы ознакомить студентов с методикой количественного определения свободных фосфатов в почве.
Фосфор содержится в земной коре в количестве 0,1% в виде химических соединений и минералов, главным образом фосфатных.
Особенностью фосфорной кислоты является её способность вступать в реакции конденсации с отщеплением молекулы воды:

Это процесс эндотермический. Обратная реакция гидролиза является экзотермической. Сочетание этих процессов в биологических системах регулирует внутриклеточное накопление и выделение энергии. Фосфатные группы входят в состав молекул РНК и ДНК, ответственных за биосинтез белков и передачу наследственной информации.
Круговорот фосфора охватывает только литосферу и гидросферу.
В основном происходит одностороннее движение фосфора с суши в воду и далее в донные отложения в форме гидро- и дигидроанионов  и
и  с катионами меди, железа и других тяжелых металлов.
с катионами меди, железа и других тяжелых металлов.
Главным антропогенным источником фосфатов являются фосфорные удобрения: СaHPO4; Сa(H2PO4)2; NH4H2PO4 и (NH4)2HPO4. Поступление фосфатов из почвы в водоёмы с грунтовыми водами и поверхностными стоками является одним из факторов ускоренного эвтрофирования водоёмов.
|
|
|
Нормальное количество фосфатов в почвах нечернозёмной зоны изменяется от 3 до 30мг на 100г почвы. Для определения содержания фосфатов их предварительно извлекают из почвы раствором соляной или уксусной кислоты.
Последующее определение осуществляют фотометрически. В данной работе используется образование в кислом растворе, содержащем фосфат-, молибдат- и ванадатанионы фосфорновонадиевомолибденовой гетерополикислоты с соотношением P:V:Mo = 1:1:11, обладающей ярко-оранжевой окраской. Измеряют поглощение в ультрафиолетовой области при 315нм (максимальная чувствительность) или в видимой области спектра при 400 - 470нм.
Цветная реакция зависит от кислотности раствора и концентрации используемых реагентов. Оптимальная кислотность фотометрируемого раствора 0,5 – 1,0моль-экв/л по HNO3 (или по H2SO4, HCl, HClO4). Если кислотность раствора мала, то жёлтое окрашивание появляется и в отсутствие ионов 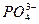 . При слишком высокой кислотности фосфорновонадиевомолибденовая гетерополикислота образуется слишком медленно. Образующаяся окраска устойчива. Концентрация ванадата в конечном растворе должна быть» 0,002моль/л, молибдата» 0,01моль/л.
. При слишком высокой кислотности фосфорновонадиевомолибденовая гетерополикислота образуется слишком медленно. Образующаяся окраска устойчива. Концентрация ванадата в конечном растворе должна быть» 0,002моль/л, молибдата» 0,01моль/л.
Определению фосфора мешает хром (VI), а также Ni2+, Co2+, Cu2+, обладающие собственной окраской. Анализируемый раствор не должен содержать восстановителей.
Экспериментальная часть
Оборудование и реактивы:
1. Метаванадат аммония, 0,25 %-ный раствор. Растворяют 1,25 г NH4VO3 в 250 мл горячей воды. По охлаждении к раствору добавляют 10 мл конц. НNO3. раствор оставляют до следующего дня, фильтруют (в случае необходимости), разбавляют водой до 500 мл и перемешивают. Раствор хранят в полиэтиленовом сосуде.
2. Молибдат аммония, 5 %-ный раствор. Растворяют 25 г (NH4)6Мо7O24×4Н2О в 250 мл воды при температуре около 50° С и оставляют до следующего дня. Раствор фильтруют (в случае необходимости), разбавляют водой до 500 мл и хранят в полиэтиленовом сосуде.
|
|
|
3. Стандартный раствор фосфора (V), содержащий 1мг/мл Р. Растворяют в воде 4,3900 г КН2РО4, высушенного при 110° С, прибавляют 1 мл хлороформа (предупреждает образование плесени). Полученный раствор разбавляют водой до 1 л.
4. Азотная кислота. Разбавляют концентрированную азотную кислоту (r=1,41 г/см3) водой в соотношении 1:1 по объему.
5. 0,1 н соляная кислота или 10 % уксусная кислота.
Ход работы:
|
|
|


