 |
Определение растворенного в воде кислорода
|
|
|
|
Теоретическая часть
Содержание кислорода в воде имеет большое значение при оценке качества поверхностных вод, некоторых сточных вод, при оценке и контроле работы станций биологической очистки и др. Содержание кислорода в воде колеблется от 6 до 10 мг/л, редко превышая 15 мг/л.
Режим растворенного кислорода[38] сильно влияет на жизнь водного объекта. Минимальная концентрация растворенного кислорода, необходимая для нормального развития рыбы, составляет около 5 мг/л. Понижение ее до 2 мг/л вызывает их массовую гибель. Неблагоприятно и пресыщение воды кислородом. ПДК кислорода - не менее 4 мг/л.
Определение растворенного в воде кислорода проводится по йодометрическому методу Винклера, который основан на способности гидроксида марганца (II) окисляться в щелочной среде в соединения высшей степени окисления, количественно связывая растворенный в воде кислород. Процесс связывания кислорода выражается уравнениями:
4MnCl2 + 8NaOH = 8NaCl + 4Mn(OH)2
2Mn(OH)2 + O2 = 2H2MnO3
2H2MnO3 + 2Mn(OH)2 = 2 Mn2O3 + 4H2O
Экспериментальная часть
Оборудование и реактивы:
1. Реактивы Винклера.
Растворяют 210 г хлористого марганца MnCl2•4Η2Ο х.ч. в дистиллированной воде и доводят объем до 500 мл. Если раствор мутный, его следует профильтровать. Можно использовать и MnSO4•4H2O в количестве 200г. Щелочной раствор йодистого калия KI +NaOH готовят так: 75г KI растворяют в 50 мл дистиллированной воды, а затем смешиваютс раствором, состоящим из 250г NaOH и 150-200мл дистиллированной воды, после чегообщий объем доводится водой до 500 мл. При отсутствии NaOH можно применять KOH(350г), а вместо KI можно применять NaI (68г).
2. Серная кислота (1:1) или концентрированная фосфорная кислота (85 %).
3. 0,2 % раствор крахмала (свежеприготовленный).
|
|
|
4. Тиосульфат натрия, Na2S2O3•5 H2O, 0,01н (или 0,002н).
5. K2Cr2O7, 0,01н для установки титра тиосульфата натрия.
Ход работы:
В пикнометры с помощью сифона наливают исследуемую воду. Не закрывая пикнометр пробкой, прибавляют реактивы Винклера - по 1 мл каждого. Пипетку с реактивом опускают на одну треть склянки. Сначала добавляют щелочной раствор иодида калия, затем хлорида марганца. Закрывают пробкой так, чтобы не было пузырьков воздуха, и перемешивают. Пробу ставят в темное место на 1-2 часа или на сутки. После отстаивания открывают пробку и прибавляют 1 мл концентрированной фосфорной или разбавленной (1:1) серной кислоты. Закрывают пробкой. Перемешивают до растворения осадка и титруют тиосульфатом натрия (0,01 н.) до бледно желтого цвета. Прибавляют 0,5 мл крахмала и тируют до полного обесцвечивания. Обмывают оттитрованным раствором стенки склянки и дотитровывают. Рассчитывают по формуле:
Х = n×F×0,08×1000/V–v, где n- объем тиосульфата натрия, пошедшего на титрование, мл;
F- поправка; V - объем склянки; v - объем прибавленных реактивов Винклера.
Определение поправки: к 1 мл 15 % KI добавляют 3 мл 25 % раствора серной кислоты и 20 мл 0,01 н. раствора бихромата калия. Ставят на три минуты в темноту, накрыв часовым стеклом. Титруют раствором тиосульфата натрия. Вычисляют поправку:
F = 20/B, где В - число мл тиосульфата натрия, пошедшее на титрование.
Контрольные вопросы
1. Какова минимальная концентрация растворенного кислорода в водоёме?
2. Охарактеризуйте процессы растворения газов.
(Лурье, 1984)
Лабораторная работа №3
Определение различных форм углекислоты в природных водоемах
Теоретическая часть
Углекислый газ, угольная кислота и её соли – постоянные компоненты природных вод. Содержание свободной угольной кислоты Н2СО3 зависит от концентрации растворенной двуокиси углерода. В форме угольной кислоты находится лишь незначительная часть растворенного углекислого газа (около 1%), поэтому содержание свободной углекислоты в воде характеризуют суммой СО2 + Н2СО3. Существующее между различными формами угольной кислоты равновесие выражается химическими уравнениями:
|
|
|
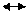
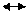
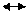 СО2+Н2О Н2СО3 Н+ + НСО3- Н+ + СО32- (Мингулина, 1990).
СО2+Н2О Н2СО3 Н+ + НСО3- Н+ + СО32- (Мингулина, 1990).
Из уравнений диссоциации угольной кислоты следует, что соотношение между её формами зависит от концентрации водородных ионов. При значении рН < 4,3 вся углекислота находится в воде в виде СО2 и Н2СО3; с увеличением значения рН доля СО2 уменьшается при одновременном увеличении доли НСО3- , и при значении рН = 8,35 практически вся углекислота присутствует в форме бикарбонат-ионов. При значении рН > 12 она представлена только ионами СО32- (рис 2).

Рис.2. Зависимость содержания отдельных компонентов карбонатной системы от рН раствора.
Воду с фактическим содержанием СО2, равным её расчетной по уравнению равновесной концентрации, называют стабильной. При содержании СО2, большем равновесной концетрации, возможно растворение СаСО3 при контакте воды, например, с доломитовыми или известняковыми породами, бетонными сооружениями, поэтому такую воду называют агрессивной.
Наоборот, при недостатке СО2 будет наблюдатся распад бикарбонатов с образованием дополнительного количества твердой фазы карбоната кальция. Такую воду называют нестабильной:
 Са2+(водн) + 2НСО3-(водн) СаСО3(тв) + СО2(г) + Н2О(ж)
Са2+(водн) + 2НСО3-(водн) СаСО3(тв) + СО2(г) + Н2О(ж)
Фактические значения рН, определенные экспериментально, могут быть больше или меньше равновесного значения рН. Разность между экспериментально найденным и равновесным значением рН называется индексом стабильности воды (U). При U=0 вода стабильна, при U>0 она нестабильна и способна к образованию отложений, при U<0 вода агрессивна (Мешалкин, 2007).
Экспериментальная часть
Оборудование и реактивы:
Коническая колба; пипетка; бюретка; спиртовой раствор фенолфталеина; метиловый оранжевый; гидроксид натрия (0,1М); соляная кислота (0,05М)
|
|
|


