 |
Пиролиз метана (нагревание)
|
|
|
|
CH4 àC2H2+3H2
2) ГИДРОЛИЗ КАРБИДА КАЛЬЦИЯ(СаС2) ПРОМЫШЛЕННЫЙ СПОСОБ:
CaC2+2H2O=Ca(OH)2+C2H2
Лабораторный способ:
CaC2+2HCIà CaCI2+C2H2
Спирты, их роль в обмене веществ.
СПИРТЫ CnH2n+1OH
Спирты-это производные углеводороды у которых 1 или несколько атомов водорода,замещены на гидрокси группу(ОН)
Классификация спиртов:
По характеру углеводородного радикала
*предельные спирты CH3-CH2-OH этанол (этиловый спирт)
*непредельные спирты CH2=CH-CH2-OH ПРОПЕНОЛ(АКРИЛОВЫЙ СПИРТ)
*ароматические спирты бензиловый спирт
2. по кол-во гидроксогрупп:
*одноатомные CH3-CH2-OH
* многоатомные CH2OH-CH2OH этандиол-1,2
CH2OH-CH2OH-CH2OH пропантриол (глицерин)
Хим.св-ва спиртов
Взаимодействие с активным металлом (кислотное св-во спирта)
CH3-CH2-OH+Na àCH3-CH2-ONa (этилат натрия,алкоголят натрия) 3,5+ H2
CH3-CH2-ONa + H2O à CH3-CH2-OH+ NaOH
CH3-CH2-ONa + HCI à CH3-CH2-OH+ NaCI
Взаимодействие с галогенными водородами. Замещение гидроксогруппами
CH3-CH2-OH+ HCIà CH3-CH2-CI+ H2O
Дегидратация (отщипление воды)
*Внутримолекулярная образуется алкены(температура больше 140)
H2SO4 T>140
CH3-CHOH-CH2-CH3 à CH3-CH=CH-CH3 + H2O
*МЕЖМОЛЕКУЛЯРНАЯ (T<140) ОБРАЗУЮТСЯ ПРОСТЫЕ ЭФИРЫ
C2H5OH+ C2H5OHà H2O+ C2H5OC2H5 ДИЭТИЛОВЫЙ ЭФИР
Окисление
*горение
CH3-CH2-OH+3O2à2CO2 +3 H2O
*окисление оксида меди (2) при нагревании,при окислении первичных спиртов образуются альдегиды:
R-CH2-OH+CuOà R-COH+Cu+H2O
ПРИ ОКИСЛЕНИИ ВТОРИЧНЫХ СПИРТОВ ОБРАЗ.КЕТОНЫ:
R-CH2-OH-R’+CuOàR-C=O-R’+Cu+H2O
· При окислении более сильными окислителями (перманаганатом калия) спирты окисляются до карбоновых кислот (COOH). Окисление вторичных и третичных спиртов идет с разрывом углеродной цепи.
5CH3-CH2-OH+4KMnO4 +6 H2SO4à 5CH3-COOH+2K2SO4+4MnSO4+11H2O
ПОЛУЧЕНИЕ СПИРТОВ:
ДЕЙСТВИЕ ВОДНОГО Р-РА ЩЕЛОЧИ НА МОНОГОЛОГЕНОПРОИЗВОДНЫЕ (ЩЕЛОЧНОЙ ГИДРОЛИЗ)
|
|
|
CH3-CHCI-CH3+ NaOH(водн.) à NaCI+ CH3-CHOH-CH3
Гидратация алкенов
CH2=CH-CH3 + HOH → CH3-CHOH-CH3
Многоатомные спирты CnH2n+2Oх
CH2OH-CH2OH- этандиол или этиленгликоль
CH2OH-CHOH -CH2OH - глицерин или пропантриол
Способы получения:
1) щелочной гидролиз галогенопроизводных:
CH2CI-CH2CI+2KOH(H2O)→ CH2OH-CH2OH
Хим. Св-ва
1) взаимод. С активными металлом.
CH2ОН-CH2OH+Na → CH2ОNa -CH2ONa+ 0.5 Н2(стрелка вверх)
CH2ОН-CH2OH -CH2OH+ Cu(OH)2 → H2O+ 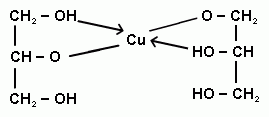
Это кач.реакция на многатомные спирты. Признак: образование василькового цвета
14. Теория химического строения органических веществ, понятие об изомерии и гомологии.
Крупнейшим событием в развитии органической химии было создание в 1961 г. великим русским ученым А.М. Бутлеровым теории химического строения органических соединений.
До А.М. Бутлерова считалось невозможным познать строение молекулы, т. е. порядок химической связи между атомами. Многие ученые даже отрицали реальность атомов и молекул.
А.М. Бутлеров опроверг это мнение. Он исходил из правильных материалистических и философских представлений о реальности существования атомов и молекул, о возможности познания химической связи атомов в молекуле. Он показал, что строение молекулы можно установить опытным путем, изучая химические превращения вещества. И наоборот, зная строение молекулы, можно вывести химические свойства соединения.
Теория химического строения объясняет многообразие органических соединений. Оно обусловлено способностью четырехвалентного углерода образовывать углеродные цепи и кольца, соединяться с атомами других элементов и наличием изомерии химического строения органических соединений. Эта теория заложила научные основы органической химии и объяснила ее важнейшие закономерности. Основные принципы своей теории А.М. Бутлеров изложил в докладе «О теории химического строения».
Основные положения теории строения сводятся к следующему:
|
|
|
Основные положения теории химического строения А.М.Бутлерова можно свести к следующему.
1. Все атомы в молекуле органического соединения связаны друг с другом в определенной последовательности в соответствии с их валентностью. Изменение последовательности расположения атомов приводит к образованию нового вещества с новыми свойствами. Например, составу вещества С2Н6О отвечают два разных соединения: диметиловый эфир (СН3-О-СН3) и этиловый спирт (С2Н5ОН).
2. Свойства веществ зависят от их химического строения. Химическое строение - это определенный порядок в чередовании атомов в молекуле, во взаимодействии и взаимном влиянии атомов друг на друга - как соседних, так и через другие атомы. В результате каждое вещество имеет свои особые физические и химические свойства. Например, диметиловый эфир - это газ без запаха, нерастворимый в воде, t°пл. = -138°C, t°кип. = 23,6°C; этиловый спирт - жидкость с запахом, растворимая в воде, t°пл. = -114,5°C, t°кип. = 78,3°C.Данное положение теории строения органических веществ объяснило явление изомерии, широко распространенное в органической химии. Приведенная пара соединений - диметиловый эфир и этиловый спирт - один из примеров, иллюстрирующих явление изомерии.
3. Изучение свойств веществ позволяет определить их химическое строение, а химическое строение веществ определяет их физические и химические свойства.
4. Атомы углерода способны соединятся между собой, образовывая углеродные цепи различного вида. Они могут быть как открытыми, так и замкнутыми (циклическими), как прямыми, так и разветвленными. В зависимости от числа связей, затрачиваемых атомами углерода на соединение друг с другом, цепи могут быть насыщенными (с одинарными связями) или ненасыщенными (с двойными и тройными связями).
5. Каждое органическое соединение имеет одну определенную формулу строения или структурную формулу, которую строят, основываясь на положении о четырехвалентном углероде и способности его атомов образовывать цепи и циклы. Строение молекулы как реального объекта можно изучить экспериментально химическими и физическими методами.
Значение теории химического строения А.М. Бутлерова:
1) является важнейшей частью теоретического фундамента органической химии;
|
|
|
2) по значимости ее можно сопоставить с Периодической системой элементов Д.И. Менделеева;
3) она дала возможность систематизировать огромный практический материал;
4) дала возможность заранее предсказать существование новых веществ, а также указать пути их получения.
Теория химического строения служит руководящей основой во всех исследованиях по органической химии.
Карбоновые кислоты
Это органические соединения,в составе которых имеется одна или несколько карбоксильных групп. COOH
Классификация кислот:
1. кол-во карбоксильных групп:
*одноосновные CH3-COOH (уксусная кислота,этановая кислота) С6Н5СООН(БЕНЗОЙНАЯ КИСЛОТА)
2. МНОГООСНОВНАЯ
|
|
|


