 |
Реакции, сопровождающиеся разрушением комплексных ионов.
|
|
|
|
Опыт 12. Образование и разрушение амминокомплекса никеля. Налить в пробирку 3−4 капли раствора сульфата никеля (II) и добавить 2−3 капли концентрированного раствора аммиака до полного растворения образующегося в первый момент осадка сульфата гидроксоникеля. Отметить окраску раствора, обусловленную катионом гексаамминоникеля (2+). Добавить несколько капель раствора соляной кислоты концентрацией 15 % до изменения окраски. Записать уравнения реакций. Объяснить изменение окраски при переходе от аквакомплекса никеля к амминокомплексу и затем к хлорокомплексу с точки зрения теории кристаллического поля и спектрохимического ряда лигандов.
Опыт 13. Разрушение комплекса при разбавлении раствора. Выполнение работы. Внести в пробирку 2 капли раствора нитрата серебра и добавлять 0,1 н. раствор иодида калия по каплям, встряхивая пробирку после каждого добавления. Почему растворяется выпавший вначале осадок иодида серебра? К получившемуся раствору добавить 4−5 капель воды. Что наблюдается?
Описать наблюдаемые процессы. Написать уравнения реакций: образования иодида серебра, его перехода в комплексное соединение, диссоциации комплексного иона, выражение константы нестойкости. Какое влияние оказывает разбавление раствора на диссоциацию комплексного иона?
Опыт 14. Разрушение комплекса при осаждении комплексообразователя. В две пробирки с раствором сульфата меди добавить: в одну раствор оксалата аммония, в другую − сульфида натрия. Написать уравнения реакций и отметить цвета выпавших осадков. В двух других пробирках получить комплексное соединение меди, добавив к 4−5 каплям раствора CuSO4 раствор аммиака до растворения выпадающего вначале осадка основной соли меди. Отметить цвет полученного комплексного соединения. Написать уравнение реакции взаимодействия сульфата меди с аммиаком, учитывая, что координационное число меди равно четырем.
|
|
|
Испытать действие растворов оксалата аммония и сульфида аммония на полученный раствор комплексной соли меди. От действия какого реактива выпадает осадок? На присутствие каких ионов в растворе комплексной соли указывает появление этого осадка? Добавить в пробирку, где выпал осадок, еще 6−7 капель того же реактива и для ускорения коагуляции поместить пробирку в водяную баню, нагретую до кипения. Сохранилась ли в растворе окраска комплекса меди?
Описать наблюдаемые явления. Ответить на поставленные по ходу работы вопросы. Написать уравнения проделанных реакций, уравнение электролитической диссоциации комплексной соли меди и ее комплексного иона. Как влияет добавление (NH4)2S на диссоциацию комплексного иона?
Сравнить произведения растворимости соответствующих солей меди и объяснить, почему одна из них не выпадает в осадок из комплексного соединения.
Опыт 15. Гидратная изомерия аквакомплексов хрома (III). Хлорид хрома СrСl3·6Н2О образует изомеры различного цвета: сине-фиолетовый [Сr(Н2О)6]Сl3; темно-зеленый [Сr(Н2О)5С1]С12·Н2О и светло-зеленый [Сr(Н2О)3Сl3]·3Н2О. В растворах все три изомера находятся в равновесии, состояние которого зависит от различных факторов, в частности, сильно зависит от температуры.
В две пробирки поместить по несколько кристалликов хлорида хрома СrСl3·6Н2О и по 10 капель воды. Одну пробирку оставить в качестве контрольной, вторую нагреть на кипящей водяной бане и наблюдать изменение окраски. Какой изомер аквакомплекса хрома (III) преимущественно устойчив при комнатной температуре? При высокой температуре?
Дать рациональные названия всех трех приведенных изомеров.
Опыт 16. Комплексные соединения в окислительно-восстановительных реакциях.
|
|
|
А. Восстановление серебра из его комплексного соединения. Добавить в пробирку к 5−6 каплям раствора нитрата серебра раствор хлорида натрия. Полученный осадок растворить в концентрированном растворе аммиака. Опустить в раствор кусочек гранулированного цинка. Что наблюдается?
Написать уравнения: получения осадка хлорида серебра, его растворения в аммиаке с образованием комплекса серебра и взаимодействия полученного комплексного соединения с цинком. Какой ион является окислителем в последней реакции? Написать уравнение электролитической диссоциации комплексного иона и ионное уравнение окислительно-восстановительной реакции.
Б. Восстановление гексацианоферрата (III) калия. В пробирку внести 4−5 капель раствора иодида калия, 3−4 капли 2 н. раствора хлороводородной кислоты и 2−3 капли бензола. Отметить, что бензол остается бесцветным. Добавить один микрошпатель кристаллов комплексной соли железа (III) K3[Fe(CN)6] и перемешать раствор стеклянной палочкой. По изменению окраски бензола убедиться в выделении свободного иода.
Написать уравнение реакции взаимодействия гексацианоферрата (III) калия с иодидом калия, учитывая, что K3[Fe(CN)6] переходит при этом в K4[Fe(CN)6]. (Кислоту в уравнение реакции не вводить). Указать окислитель и восстановитель.
В. Окисление гексацианоферрата (II) калия. Поместить в пробирку 4−5 капель раствора перманганата калия, подкислить 2 н. серной кислотой и добавить по каплям раствор гексацианоферрата (II) калия до обесцвечивания раствора.
Написать уравнение реакции, учитывая, что комплекс железа (II) переходит в комплекс железа (III) с тем же координационным числом, а перманганат калия в кислой среде восстанавливается до сульфата марганца (II).
Протокол лабораторной работы
По каждому опыту записать используемые при проведении эксперимента реактивы и результаты проведения реакций: образование осадка, выделение газа, изменение цвета раствора и т.д.
Содержание отчета по лабораторной работе
1. Название работы.
2. Цель работы.
3. Уравнения реакций в молекулярной и ионной форме, результаты проведения реакций, ответы на вопросы.
Лабораторная работа № 11. Определение энтальпии реакции нейтрализации
|
|
|
Цель работы: ознакомиться с принципами и практическими приемами определения теплового эффекта реакции нейтрализации. Измерение теплового эффекта реакции основано на первом начале термодинамики. Для определения теплового эффекта реакции необходимо знать теплоемкость системы Сcal и вызванное реакцией изменение температуры D Т.
Общие сведения
Реакция нейтрализации представляет взаимодействие оснований с кислотами, например, NaOH + HCl = NaCl + H2O. В ионной форме должна быть выражена уравнением H+ + OH− = H2O. Образование из ионов Н+ и OH− молекул воды сопровождается выделением значительного количества тепла.
Сильные кислоты и сильные основания в достаточно разбавленных растворах диссоциированы полностью, поэтому общий тепловой эффект реакции нейтрализации для них обусловлен образованием молекул воды из ионов и теплота процесса должна быть близка к стандартной теплоте нейтрализации, вычисленной по закону Гесса.
Слабые кислоты и основания в растворе представлены преимущественно молекулами. Значение теплоты нейтрализации может существенно отличаться от стандартного значения. В этом случае процесс можно разделить на стадии: диссоциация слабого электролита, гидратация ионов  и собственно нейтрализация
и собственно нейтрализация 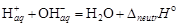 . Тепловой эффект реакции является суммой перечисленных процессов и к теплоте нейтрализации сильного электролита
. Тепловой эффект реакции является суммой перечисленных процессов и к теплоте нейтрализации сильного электролита  следует добавить эндотермический эффект диссоциации слабого электролита
следует добавить эндотермический эффект диссоциации слабого электролита  и экзотермический эффект гидратации катиона и аниона
и экзотермический эффект гидратации катиона и аниона 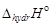 :
:
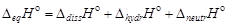 .
.
Контрольные вопросы
1. На каком законе термодинамики основано измерение теплового эффекта реакции?
2. Какие величины надо знать или экспериментально определить для установления теплового эффекта реакции?
3. Какие составляющие входят в величину теплового эффекта реакции нейтрализации слабого электролита?
4. Что представляет собой реакция нейтрализации?
5. В каком случае величина теплового эффекта реакции взаимодействия кислоты и щелочи близка к справочному значению?
|
|
|
6. Почему тепловой эффект взаимодействия слабой кислоты и щелочи будет отличаться от справочного значения?
7. Какие стадии можно выделить при реакции слабой кислоты со щелочью?
8. Какие стадии реакции слабой кислоты со щелочью являются экзотермическими процессами?
9. Из каких составляющих складывается тепловой эффект реакции слабой кислоты со щелочью?
Оборудование и реактивы
Весы лабораторные. Стеклянный химический стакан объемом 100–150 мл. Стеклянный химический стакан объемом 300–400 мл. Стеклянный химический стакан объемом 50 мл. Корковая пробка. Стеклянная палочка. Термометр с ценой деления 0,1°С. Мерный цилиндр объемом 50 мл. Раствор сильной кислоты (0,5 н.). Раствор щелочи (0,5 н.).
Выполнение работы
1. Собрать упрощенный калориметр из двух вложенных друг в друга стаканов: внутренний стакан (емкостью 100-150 мл) поставить на пористую пробку на дне наружного (емкостью 300-400 мл). Поместить во внутренний стакан стеклянную палочку и термометр с ценой деления 0,1°С.
2. Во внутренний стакан калориметра налить мерным цилиндром 25 мл раствора исследуемой кислоты V K концентрацией 0,5 М.
3. Поставить внутренний стакан в калориметр.
4. Поместить в раствор кислоты термометр с ценой деления 0,1°С.
5. Измерить температуру кислоты с точностью до 0,1 °С.
6. Мерным цилиндром отмерить 25 мл щелочи.
7. Вылить щелочь в кислоту и осторожно, но быстро перемешать раствор.
8. Измерить температуру полученного раствора с точностью до 0,1 °С.
Содержание протокола лабораторной работы
1. Название кислоты и ее химическая формула
2. Объем раствора кислоты, взятый для опыта V К = ………….мл
3. Концентрация раствора кислоты С К = ………………….экв/л
4. Название сильного основания и его химическая формула
5. Объем раствора щелочи, взятый для опыта V Щ = ………….мл
6. Концентрация раствора щелочи С Щ = ………………..экв/л
7. Температура раствора начальная Т 1 = ……………°С
8. Температура раствора конечная Т 2 = …………..°С
|
|
|


