кислой среде HCl) относятся: PbS, HgS, CuS, Ag2S, SnS, SnS2, Bi2S3, As2S3, As2S5, Sb2S3, Sb2S5, CdS. При действии конц. кислот - окислителей они окисляются:
Bi2S3 + 8HNO3 (конц) ® 2Bi(NO3)3 + 2NO + 3S¯ +4H2O
Bi2S3 + 25HNO3 (конц.) 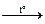 Bi2(SO4)3 + 24NO + 12H2O Bi2(SO4)3 + 24NO + 12H2O
CuS + 10HNO3 (конц) 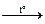 Cu(NO3)2 + H2SO4 + 8NO2 + 4H2O Cu(NO3)2 + H2SO4 + 8NO2 + 4H2O
SnS2 + HNO3 (конц) ® H2SnO3¯ + H2SO4 + NO2
3As2S5 + 40HNO3 (конц) + 4H2O ® 6H3AsO4 + 15H2SO4 + 40NO
Кислотные сульфиды (SnS2, As2S3, As2S5, Sb2S3, Sb2S5) растворяются в избытке основных сульфидов (Na2S, (NH4)2S) с образованием тиосолей:
Э2S3 + 3(NH4)2S ® 2(NH4)3ЭS3
Э2S5 + 3(NH4)2S ® 2(NH4)3ЭS4
Помимо сульфидов известны гидросульфиды (NaHS, KHS, Ca(HS)2 и др.) - хорошо растворимые в воде вещества, подвергающиеся гидролизу, но в меньшей степени, чем сульфиды.
HS- + H2O «H2S + OH-, рН>7
Сульфиды имеют различный цвет, что связано со степенью поляризации сульфид-ионов: более высокая степень поляризации приводит к углублению цвета.
Например: Na2S – бесцветный As2S3 и As2S5 - желтый
ZnS – белый
CdS – желтый Sb2S3 и Sb2S5 - оранжевый
MnS – телесный
HgS – черный Bi2S3 - коричневый
В лаборатории получают сероводород из сульфида железа (II), или сульфида кальция:
FeS + 2HCl ® FeCl2 + H2S
H2S – горит голубым пламенем:
2H2S + 3O2 ® 2SO2 + 2H2O
2H2S + O2 ® 2S + 2H2O (при недостатке O2).
H2S можно обнаружить по почернению "свинцовой бумаги" - фильтровальной бумаги, пропитанной солями Pb (II):
H2S + Pb2+ ® PbS¯ + 2H+.
Качественной реакцией на H2S и сульфид ион в растворе является | 


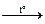 Bi2(SO4)3 + 24NO + 12H2O
Bi2(SO4)3 + 24NO + 12H2O