 |
Недостаточность печени. Этиология, патогенез, основные проявления. Роль алкоголя в этиологии заболевания печени.
|
|
|
|
Вопрос 12.
Общая этиология и патогенез заболеваний печени. Экспериментальное изучение функции печени (прямая и обратная фистула, полное и частичное удаление печени, ангиостомия, функциональные пробы печени)
Печеночная недостаточность (ПН) характеризуется снижением одной, нескольких или всех функций печени ниже уровня, необходимого для обеспечения нормальной жизнедеятельности организма. ПН делится на виды по следующим признакам:
1) по числу нарушенных функций - на парциальную и тотальную,
2) по течению - на острую и хроническую,
3) по исходу - летальную и нелетальную.
Причины печеночной недостаточности. Можно выделить две группы причин печеночной недостаточности.
К первой группе относятся патологические процессы, локализующиеся в печени и в желчевыделительных путях, а именно:
а) гепатиты - вирусные, бактериальные, токсогенные;
б) дистрофии (гепатозы);
в) циррозы;
г) опухоли печени;
д) паразитарные поражения ее;
е) генетические дефекты гепатоцитов;
ж) камни, опухоли, воспаления желчевыделительных путей с выраженным холестазом.
Ко второй группе причин относятся патологические процессы вне печени, а именно:
а) шок, в том числе послеоперационный;
б) сердечная недостаточность;
в) общая гипоксия;
г) почечная недостаточность;
д) белковое голодание;
е) гипоавитаминоз E;
ж) дефицит селена;
з) эндокринопатии - в частности, острая недостаточность надпочечников;
и) метастазы опухолей в печень.
Патогенез печеночной недостаточности. Общий патогенез ПН может быть представлен в виде следующей цепи изменений: действие повреждающего фактора → 1) изменение молекулярной архитектоники мембран гепатоцитов → 2) усиление свободнорадикального перекисного окисления липидов (ПОЛ) → 3) частичная или полная деструкция мембран + повышение их проницаемости → 4) выход из лизосом их гидролаз, что потенцирует повреждение мембран клеток → 5) освобождение поврежденными макрофагами некрозогенного фактора и интерлейкина 1, способствующих развитию воспалительной и иммунной реакции в печени → 6) образование аутоантител и аутосенсибилизированных T-киллеров, вызывающих дополнительное аутоаллергическое повреждение гепатоцитов.
|
|
|
Каждое из перечисленных патогенетических звеньев может стать на определенной стадии развитием печеночной недостаточности доминирующим, что должно быть учтено при выборе ее терапии.
Проявления и механизмы печеночной недостаточности:
1. Нарушение участия печени в углеводном обмене. Оно заключается в снижении способности гепатоцитов, с одной стороны, превращать глюкозу в гликоген, а с другой - расщеплять гликоген до глюкозы. Это обусловливает характерный признак ПН - неустойчивый уровень сахара крови. После приема пищи развивается гипергликемия, а натощак - гипогликемия.
2. Нарушение участия печени в липидном обмене. Оно характеризуется снижением способности гепатоцитов:
а) превращать более атерогенную форму холестерина (свободный холестерин) в менее атерогенный холестерин-эстер и б) образовывать фосфолипиды, обладающие антиатерогенным действием.
Оба эти изменения ведут к увеличению в крови уровня свободного холестерина и к снижению антиатерогенных фосфолипидов, что способствует отложению холестерина в стенках сосудов и развитию атеросклероза.
3. Нарушение участия печени в белковом обмене. Включает три вида изменений:
а) снижение синтеза гепатоцитами альбуминов, что ведет к гипоальбуминемии и гипоонкии крови, а на стадии развития портальной гипертензии способствует развитию асцита;
|
|
|
б) уменьшение биосинтеза ферментов и белков - прокоагулянтов (протромбина, проакцелерина, проконвертина), что обусловливает развитие коагулопатий, характеризующихся склонностью к кровоточивости. Этому способствует также уменьшение всасывания в кишечнике жирорастворимого витамина K, поскольку ПН сочетается с нарушением желчеобразовательной и желчевыделительной функций печени;
в) снижение активности процесса дезаминирования аминокислот и синтеза мочевины из аминогрупп и аммиака, что ведет к снижению в крови содержания мочевины.
4. Нарушение биосинтеза гепатоцитами ферментов. Заключается в уменьшении секреции гепатоцитами образуемых ими ферментов (холинэстеразы, НАД и др. ) в кровь. Кроме того, повреждение гепатоцитов сопровождается увеличением выхода из них в кровь внутриклеточных ферментов: аланинаминотрансферазы и глютаматаминотрансферазы.
5. Расстройство обмена витаминов. Состоит в:
а) снижение всасывания в кишечнике жирорастворимых витаминов A, D, E, K;
б) уменьшении способности гепатоцитов превращать провитамины в активные витамины (например, каротин в витамин A);
в) торможении процесса образования из витаминов коферментов (например, из пантотеновой кислоты - ацетил коэнзим A, из витамина B1 - кокарбоксилазы пирувата).
Все перечисленные изменения ведут к развитию эндогенных (печеночных) гиповитаминозов.
6. Нарушение антитоксической (" барьерной" ) функции печени. Оно характеризуется снижением обезвреживания печенью: а) кишечных ядов - фенольных ароматических соединений (фенола, индола, скатола), биогенных аминов (кадаверина, путресцина, тирамина), аммиака;
б) ядовитых метаболитов: низкомолекулярных жирных кислот (валериановой, капроновой), метилированных и аминных производных серусодержащих аминокислот (тауриновой, цистамина, метионина), токсического производного пирувата - ацетонина;
в) экзогенных ядов (грибкового, микробного, паразитарного происхождения, ядохимикатов и др. ); снижается также инактивация купферовскими (зведчатыми) клетками коллоидальных частиц и микробов.
7. Нарушение образования и секреции печенью желчи, что ведет к развитию желтух.
Финалом нарастающей печеночной недостаточности является печеночная кома.
|
|
|
Эксперименты на печени.
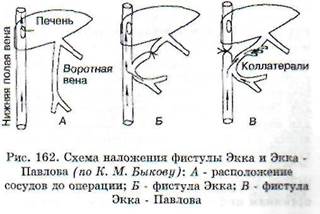
Наложение фистулы Экка - метод, примененный в 1877 г. русским исследователем Экком в лаборатории Н. В. Тарханова. Он заключается в следующем: между нижней полой и воротной венами у собак создается анастомоз. Воротная вена выше соустья перевязывается и вся кровь, оттекающая из органов брюшной полости, поступает непосредственно в нижнюю полую вену, минуя печень (рис. 162). Этот эксперимент позволил изучить обезвреживающую, а также мочевинообразовательную функции печени.
После операции Экка у животных уже через 3-4 дня при кормлении мясной пищей или через 10-12 дней при использовании молочно-растительной диеты, появлялись атаксия, манежные движения, периодически клонические и тонические судороги. В крови нарастало содержание аммиака, который в норме обезвреживается в печени, уменьшался синтез белков, нарушался обмен холестерина и образование желчи.
Обратная фистула Экка - Павлова. В 1893 г. И. П. Павлов предложил после наложения соустья на воротную и нижнюю полую вены перевязывать выше соустья не воротную, а нижнюю полую вену. При этом в печень устремляется кровь не только из пищеварительного тракта по воротной вене, но и из задней половины туловища. Животные с такой фистулой живут годами. На этой экспериментальной моделе изучается функциональное состояние печени в разных условиях пищевой нагрузки.
Полное удаление печени. Производится в два приема. Вначале воспроизводится обратная фистула Экка - Павлова. Последствием этой опера- ции является развитие коллатерального кровообращения. В результате часть венозной крови из задней части тела через v. azygos и внутренние грудные вены отводится в верхнюю полую вену, минуя печень. Через 3-4 недели после первой операции проводят вторую: воротная вена перевязывается и печень удаляется. В ближайшие часы после удаления печени у собак появляется мышечная слабость, адинамия, резко понижается содержание сахара в крови и при снижении его ниже 2, 5 ммоль/л возможно развитие гипогликемической комы с последующей гибелью животного. Введением глюкозы можно несколько продлить жизнь животного. Одновременно в крови нарастает количество аммиачных соединений и понижается содержание мочевины. Собаки после такой операции живут не более 12-15 часов. Удаление печени является, по существу, экспериментальной моделью печеночной комы.
|
|
|
После частичного удаления печени (до 3/4 органа) очень резких нарушений обмена не происходит ввиду того, что оставшаяся
часть печени сохраняет свои функции и реализует компенсаторные возможности.
При изучении функциональной роли печени в норме и при патологии применяется также ангиостомический метод Е. С. Лондона, предложенный в 1919 г. К стенкам крупных кровеносных сосудов (воротная и печеночная вены) пришиваются металлические канюли (нержавеющие или серебряные), свободные концы которых выводятся через покровы брюшной стенки наружу. Канюли позволяют систематически брать кровь из сосудов и вводить в них различные вещества. Метод ангиостомии дал много ценного в изучении роли печени в билирубино-образовании, углеводном, белковом, жировом и солевом обменах.
Экспериментальной моделью является и метод перфузии изолированной печени. Донорами печени являются преимущественно лабораторные животные: крысы, кролики, кошки. В настоящее время для этих целей используется и печень крупных животных: собак, свиней и телят. Эта экспериментальная модель применима для изучения роли печени в процессах метаболизма, а также в решении вопросов трансплантации органа.
Для экспериментального воспроизведения заболеваний печени пользуются введением в организм инфекционных и токсических агентов. Сильным гепатотропным ядом является СС14 (четыреххлористый углерод). Парентеральное введение 0, 2 мл/100 г 80% масляного раствора этого вещества вызывает альтерацию и некробиоз гепатоцитов в центральных зонах печеночных долек. Для указанных целей используют также хлороформ, семена гелиотропа. Жировой гепатит воспроизводится путем введения сернокислого гидразина и алкоголя. Токсическое действие алкоголя на печень выражается в сосудистых расстройствах и очаговых дистрофически-деструктивных изменениях паренхимы.
Вопрос 13.
Недостаточность печени. Этиология, патогенез, основные проявления. Роль алкоголя в этиологии заболевания печени.
|
|
|


