 |
Общие указания к лабораторным работам по электрохимическим методам анализа
|
|
|
|
1. Прежде чем приступить к выполнению практических работ необходимо прочитать:
а) описание прибора и методику измерений на нем по соответствующей инструкции, прилагаемой к прибору;
б) описание выполнения конкретной работы.
2. При выполнении работы следует четко представлять себе механизм соответствующих химических и электрохимических реакций.
3. В процессе выполнения работы проводить запись в лабораторном журнале.
4. По полученным экспериментальным данным начертить соответствующие кривые.
5. Обратить особое внимание на правила обращения и очистки индикаторных электродов.
Черезвычайно осторожно обращаться со стеклянным электродом, так как стенки шарообразного конца его очень тонки (0,03 мм), электрод легко повредить. Поэтому при опускании его в раствор необходимо проследить, чтобы нижний конец полуэлемента сравнения был на несколько мм ниже, чем у стеклянного электрода во избежание удара.
6. При работе с соединительным мостиком необходимо следить, чтобы в нем не было пузырьков воздуха. В тех случаях, когда нельзя применять соединительные мостики, заполненные раствором хлорида калия (титрование галогенидов, присутствие веществ, реагирующих с ионами хлорида), их заменяют мостиками с раствором нитрата калия. Соблюдать при этом правила включения мостика в цепь.
7. По окончании работы привести в порядок и сдать рабочее место лаборанту.
8. Электроды оставить погруженными в дистиллированную воду.
Лабораторная работа №1
Разделение и обнаружение ионов методом бумажной хроматографии
Цель работы: Определение водородного показателя среды потенциометром ЭВ-74.
Для определения рН растворов составляют ячейку из стеклянного индикаторного электрода и хлор-серебрянного электрода сравнения, погруженного в один и тот же раствор. ЭДС такой ячейки состоит из алгебраической суммы потенциалов, возникающих на отдельных поверхностях раздела фаз:
|
|
|
испытуемый раствор – внешняя поверхность стекла (Е1), внутренняя поверхность стекла – стандартный раствор (Е2);
стандартный раствор – индикаторный электрод (Е3) и потенциал электрода сравнения, погруженного в раствор (Е4):
э.д.с.=Е1+Е2+Е3+Е4 (2)
Так как переменным является лишь Е1, зависящий от рН раствора, то э.д.с. является практически функцией рН испытуемого раствора:
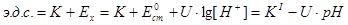 , (3)
, (3)
где  - стандартный потенциал стеклянного электрода.
- стандартный потенциал стеклянного электрода.
Надо полагать, что если внешняя и внутренняя поверхности шарика стеклянного электрода соприкасаются с одним и тем же раствором и применены два одинаковых индикаторных электрода, то из-за равенства E1=E2 и E3=E4 э.д.с. цепи должна оказаться равной нулю. На практике, однако, у каждого стеклянного электрода наблюдается при указанных условиях небольшая величина э.д.с., называемая «потенциал ассиметрии», связанная с некоторым расхождением между величинами E1и E2.
Хотя точная причина такого явления еще окончательно не установлена, принято считать ее следствием различия в степени поверхностного натяжения внешней и внутренней стенок стекла. Приборы, с помощью которых измеряют рН растворов стеклянным электродом, снабжены необходимым приспособлением, позволяющим корректировать потенциал асимметрии.
Современные рН-метры позволяют непосредственно измерять значение рН, отсчитываемое по положению стрелки измерительного прибора на шкале рН.
Из-за большого омического сопротивления измерительной цепи (стекло-диэлектрик) все подобные рН-метры сконструированы с расчетом усиления силы тока, протекающего через цепь (ламповые усилители).
Аппаратура и реактивы
|
|
|
Лабораторный рН-метр, милливольтметр рН-340 (ЭВ-74);
Электрод сравнения – хлоридсеребрянный;
Индикаторный электрод – стеклянный;
Буферные растворы с различными значениями рН.
Порядок выполнения работы
1. Ознакомление с порядком работы на ЭВ-74.
2. Определение рН раствора.
До начала измерения переключатель иономера установите в положение “t” и “-1-19”. Включите иономер в сеть и прогрейте его 30 мин. Слегка приподнимите стаканчик с электродами, отодвиньте столик, промойте электроды дистиллированной водой из промывалки. Остатки воды с электродов удалите кусочками фильтровальной бумаги.
Проверку и настройку рН-метра проводят по одному из стандартных буферных растворов (например, с рН 1,68; 3,56; 4,06; 6,86; 9,22). Рекомендуется применять стандартный буферный раствор, величина которого находится в том же диапазоне измерения, что и рН испытуемого раствора. Перед каждым погружением в стандартный или испытуемый раствор электроды тщательно промывают дистиллированной водой и осторожно удаляют избыток воды с их поверхности фильтровальной бумагой. В стакан наливают стандартный буферный раствор с соответствующим значением рН и опускают в него электроды. Ручкой потенциометра устанавливают стрелку прибора на деление шкалы, отвечающее значению рН стандартного раствора.
Получите у преподавателя испытуемый раствор, налейте его в стаканчик иономера (до половины объема) и погрузите в него электроды. После этого последовательно нажмите кнопки прибора «Катионы, анионы», «рХ» и «-1-19».
Заметьте положение стрелки на шкале «-1-19» показывающего прибора и нажмите кнопку соответствующего диапазона. Если показание по шкале «-1-19» оказалось между цифрами 8 – 9, то следует нажать кнопку диапазона 4-9.
Запишите показание стрелки иономера по шкале «0-5» и прибавьте к нему начальную цифру выбранного диапазона. На этом определение рН испытуемого раствора закончено.
Электроды до следующего определения оставьте в дистиллированной воде. Выключите иономер из сети.
Контрольные вопросы
- Принципы потенциометрического определения рН растворов.
- Индикаторные электроды в рН метре. Принципы действия. Устройство.
- Какой электрод применяют в качестве электрода сравнения?
|
|
|
Литература
1. Методическое пособие по физико-химическим методам анализа. Орел ГТУ, 2001.
2. Цитович И.К. Курс аналитической химии. – М.: Высшая школа, 1994.
3. Васильев В.П. Аналитическая химия, ч.2. Физико-химические методы анализа. М.: Высшая школа, 1994.
4. Дорохова Е.П., Прохорова Г.В. Аналитическая химия. Физико-химические методы анализа/ Под ред. О.М. Петрухина. – М.: Химия, 1987.
5. Практикум по физико-химическим методам анализа/ Под ред. О.М. Петрухина. – М.: Химия, 1987.
Лабораторная работа №2
|
|
|


