 |
Глава 9. Заболевания задней доли гипофиза
|
|
|
|
Г. Л. РОБЕРТСОН (G. L. ROBERTSON)
ГОРМОНЫ ЗАДНЕЙ ДОЛИ ГИПОФИЗА
АНАТОМИЯ
Нейрогипофиз представляет собой удлиненное выпячивание вентрального гипоталамуса, непосредственно контактирующее с задней и дистальной частью аденогипофиза [I]. У взрослых мужчин и женщин масса нейрогипофиза составляет приблизительно 100 мг, и его можно разделить на две части, соединенные короткой ножкой, проходящей сквозь диафрагму турецкого седла. Верхнюю часть называют по-разному: воронкой или срединным возвышением, а нижнюю — инфундибулярным отростком или pars nervosa. Обе части снабжаются кровью из ветвей верхней и нижней гипофизарных артерий, отходящих от задней коммуникантной и внутрикавернозной части внутренних сонных артерий. В pars nervosa артериолы распадаются на местные капиллярные сети, которые дренируются непосредственно в яремную вену через венозные синусы (турецкого седла, кавернозные и боковые). В воронке первичные капиллярные сети сливаются в другую си-

Рис. 9—1. Нейрогипофиз и его основные нервные связи.
НГ — нейрогипофиз; АГ — аденогипофиз: ДТС — диафрагма турецкого седла; ПЗН — перекрест зрительных нервов: СОЯ — супраоптическое ядро: ПВЯ — паравентрикулярное ядро ОР — осморецептор; БР — волюм- и барорецептор ЯСТ — ядро солитарного тракта: РЦ — рвотный центр.
стему — воротные вены, которые перед впадением в системную циркуляцию перфузируют аденогипофиз.
Под микроскопом нейрогипофиз выглядит как густо переплетенная сеть капилляров, питуицитов и безмякотных нервных во-лолон, содержащих большое число электронно-плотных гранул. Эти нейросекреторные нейроны берут начало главным образом в крупноклеточных ядрах супраоптической и паравентрикулярной областей гипоталамуса [2]. Большинство аксонов направляется отсюда вентрально и каудально и оканчивается луковицеобразными расширениями на капиллярных сетях, пронизывающих все части нейрогипофиза, в том числе ножку и воронку (рис. 9—1). Последняя служит местом окончания и других нейросекреторных нейронов, влияющих на переднюю долю гипофиза, путем высвобождения стимулирующих или тормозящих факторов в воротные вены. Играют ли аналогичную роль нейрогипофизарные нейроны воронки — неизвестно. Существует и особый еще меньший отдел нейрогипофиза, который проецируется на III и, вероятно, боковые желудочки мозга [1, З]. По-видимому, из него секрет, выделяется непосредственно в СМЖ, но окончательно его функция не установлена [4].
|
|
|
ХИМИЯ
Единственно известными гормонами, секретируемыми нейрогипофизом взрослого человека, являются вазопрессин и окситоцин. Их структура впервые была расшифрована du Vigneaud с сотр. более 20 лет назад [5]. Каждый из этих гормонов представляет собой нонапептид, состоящий из шестичленного кольца, замкнутого дисульфидным мостиком, и трехчленной концевой части, терминальная карбоксильная группа в которой амидирована (рис. 9—2). Вазопрессин отличается от окситоцина только присутствием фенилаланина на месте изолейцина в кольце и аргинина на месте лейцина в концевой части молекулы. Эти два гормона обнаружены у всех млекопитающих, за исключением подотряда Suina, у некоторых видов которого образуется вариант вазопрессина, содержащий в 8-й позиции лизин вместо аргинина [6]. Окситоцин обнаружен также у многих видов птиц, пресмыкающихся, амфибий и костистых рыб. Однако вместо вазопрессина гипофиз позвоночных, не относящихся к классу млекопитающих, содержит аргининвазотоцин. Его структура отличается от структуры вазопрессина только присутствием в 3-й позиции изолейцина, а биологические эффекты обоих соединений одинаковы. Поскольку вазотоцин — это единственный нонапептидный гормон, находимый у некоторых филюмов древних позвоночных, его считают предшественником, из которого в процессе эволюции вследствие мутации и удвоения генов образовались окситоцин и вазопрессин.
|
|
|
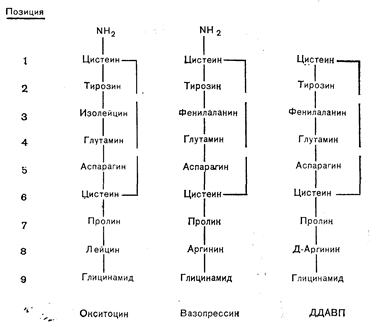
Рис. 9—2. Аминокислотная последовательность окситоцина, вазопрессина и синтетического аналога— 1-дезамино-8-D-аргинин-вазопрессина (ДДАВП).
Синтез большого числа структурных аналогов вазопрессина и окситоцина позволил точнее выяснить зависимость между их конформацией и биологической активностью [7]. Хотя изменение почти любой части молекулы может сказываться на трехмерной структуре и биологической активности, наиболее важными для узнавания и связывания гормона его рецептором считают боковые цепи в 3, 4, 7 и 8-й позиции, тогда как замещения в 5-й позиции влияют на собственную активность молекулы. При замене в 8-й позиции L-аргинина на D-аргинин отношение антидиуретического эффекта вазопрессина к его прессорной активности резко увеличивается. Эта модификация наряду с удалением терминальной аминогруппы цистеина образует 1-дезамино-8-D-аргинин-вазопрессин (ДДАВП) (см. рис. 9—2) — клинически применяемый аналог, обладающий более длительной и сильной антидиуретической активностью [8].
Вазопрессин и окситоцин откладываются в нейрогипофизе в виде нерастворимых комплексов с белками-носителями, получившими название нейрофизинов. Acher и сотр. [9] впервые отделили эти нейрофизины от активных гормонов более 20 лет назад. Однако лишь недавно удалось получить отдельные нейрофизины в достаточно чистом виде, чтобы определить их физикохимические свойства [10]. У человека и большинства млекопитающих иммунологически и хроматографически выделены нейрофизины двух основных типов. Один из них находится исключительно в гранулах, содержащих окситоцин, а второй — только в гранулах, содержащих вазопрессин. Оба представляют собой, по-видимому, одноцепочечные полипептиды с исходной молекулярной массой примерно 10000, но в концентрированных растворах легко образуют димеры и тетрамеры. Нейрофизин каждого типа одинаково хорошо связывает окситоцин и вазопрессин. Это свидетельствует о том, что специфические связи с гормонами, обнаруживаемые in vivo, обусловлены анатомической компартментализацией. Оптимум рН для связывания гормонов с нейрофизином составляет 5, 2—5, 8,. а К—приблизительно 2-105. Такие параметры обеспечивают полную диссоциацию комплекса нейрофизин — гормон в плазме. Частично определена аминокислотная последовательность ряда нейрофизинов, причем выявлена значительная внутренняя гомология той части молекулы, которую считают местом связывания гормонов.
|
|
|
БИОСИНТЕЗ И СЕКРЕЦИЯ
Вазопрессин и окситоцин синтезируются в клеточным телах супраоптических и паравентрикулярных ядер, упаковываются в гранулы с соответствующими нейрофизинами и транспортируются по аксонам к их конечным расширениям, где и хранятся до своего высвобождения [2, 11]. Хотя каждый гормон продуцируется особой популяцией нейронов [12], механизмы биосинтеза того и другого, по-видимому, одинаковы. Включение аминокислот в вазопрессин требует участия рибосом и проходит, вероятно, через-этап синтеза макромолекулярного предшественника или прогормона, который в процессе транспорта расщепляется с образованием активного нонапептида [11]. Синтез гормонов как механически, так и анатомически тесно связан, по-видимому, с синтезом соответствующего нейрофизина. Так, крысы линии Brattleboro с наследственным отсутствием способности к синтезу вазопрессина лишены также соответствующего нейрофизина [12]. И наоборот, многие злокачественные опухоли, которые в процессе дедифференцировки приобретают способность к синтезу вазопрессина и/или окситоцина, содержат и соответствующие нейрофизины [13]. Скорость синтеза гормонов увеличивается под действием стимулов, усиливающих их секрецию, таких, как дегидратация. Однако по крайней мере у крыс эта компенсаторная реакция развивается лишь постепенно и часто выражена не в той степени, чтобы полностью компенсировать повышенную скорость секреции. Запасы вазопрессина в нейрогипофизе при хронической стимуляции его секреции, что наблюдается в условиях длительного воздержания от питья, обычно резко истощаются.
|
|
|
Процесс упаковки гормона со своим нейрофизином в гранулы и транспорта их по аксону выяснен не полностью. Гранулы окружены мембраной и у некоторых видов животных образуются, по-видимому, из пластинчатого комплекса в перикарионе. Транспорт может осуществляться с помощью особого феномена аксонального тока, наблюдаемого в других нервных структурах, или какого-то более быстрого механизма с участием микротрубочек.
Секреция гормона и связанного с ним нейрофизина осуществляется, очевидно, с помощью зависимого от кальция процесса экзоцитоза, аналогичного описанному для других нейросекреторных систем [14]. Согласно этой точке зрения, процесс «запускается» распространением по нейрону электрического импульса, который вызывает деполяризацию клеточной мембраны, приток кальция, слияние секреторных гранул с мембраной и выталкивание их содержимого.
РЕГУЛЯЦИЯ СЕКРЕЦИИ
Известно, что на секрецию вазопрессина влияют многие факторы [15—17]. Наиболее важным из них в физиологических условиях является, вероятно, осмотическое давление жидких сред организма. Влияние этого фактора на секрецию вазопрессина опосредуется осморецептором, расположенным в переднем гипоталамусе вблизи, но отдельно от супраоптических и паравентрикулярных, ядер [18] (см. рис. 9—1). Функциональные свойства осморецептора напоминают таковые дискретного или «установочного» рецептора (рис. 9—3). Когда осмоляльность плазмы удерживается ниже определенного минимума или пороговой величины, содержание вазопрессина в ней постоянно находится на минимальном или неопределимом уровне. Если осмоляльность превышает этот порог, то уровень вазопрессина в плазме круто повышается прямо пропорционально ее осмоляльности. Наклон линии, отражающей

Рис. 9—3. Зависимость содержания вазопрессина (ВП) в плазме от ее осмоляльности у здорового взрослого человека и больного с полиурией различной этиологии (перепечатано с разрешения из публикации Robertson и соавт. [18]).
Черные кружки — здоровые лица (25 человек) черные квадраты — 2 больных первичной полидипсией: черные треугольники— 2 больных нефрогенным несахарным диабетом; кружки с точкой — 8 больных гипофизарным несахарным диабетом.
связь этих двух переменных, указывает на чрезвычайную чувствительность системы осморегуляции. Он свидетельствует о том, что изменения осмоляльности плазмы в среднем на 1 % достаточно, чтобы вызвать существенные сдвиги в секреции вазопрессина.
|
|
|
Система осморегуляции способна реагировать не только чутко, но и весьма точно [18]. При обследовании некоторых взрослых лиц в тщательно контролируемых условиях положения тела и физической активности уровень вазопрессина в плазме и ее осмоляльность почти всегда обнаруживают тесную корреляцию. Сравнительно широкий разброс, который характеризует зависимость между уровнем вазопрессина в плазме и ее осмоляльностью в популяции здоровых взрослых лиц (см., рис. 9—3), обусловлен в основном индивидуальными особенностями настройки и чувствительности системы. Причины таких индивидуальных различий осморегуляторной функции во многом не известны. На «установочную» точку осморецептора влияют гемодинамические параметры (см. ниже), но нормальные колебания объема или давления крови, вероятно, не столь велики, чтобы на их счет можно было отнести различие в порогах, варьирующих от 270 до 290 мосмоль/кг. Некоторое увеличение чувствительности системы может быть связано с возрастом, но опять-таки возрастной фактор не единственный, поскольку даже у молодых лиц чувствительность может различаться в 5 раз. Роль пола и/или половых гормонов неизвестна. В одном из исследований не было найдено-разницы в осморегуляторной функции между мужчинами и нормально менструирующими женщинами, тогда как в другом у женщин и получавших эстрогены мужчин чувствительность системы оказалась более высокой [16].
Осморецептор неодинаково чувствителен к различным растворенным в плазме веществам [15, 16, 18]. Натрий и его анионы, в норме определяющие более 95% общего осмотического давления плазмы, наиболее сильные из известных веществ, стимулирующих секрецию вазопрессина. Весьма эффективны и некоторые сахара, такие, как маннитол и сахароза, по крайней мере при внутривенном введении. В отношении этих веществ, таким образом, механизм регуляции обладает свойствами истинного осморецептора. С другой стороны, повышение осмоляльности плазмы за счет мочевины или глюкозы практически не стимулирует секрецию вазопрессина. Все еще не известно, каким образом и почему осморецептор столь эффективно различает разные виды растворенных в плазме веществ. Согласно современным представлениям, сигналом, стимулирующим осморецептор, служит снижение содержания внутриклеточной жидкости под действием осмотических сил. Если эта гипотеза верна, то способность данного растворенного вещества стимулировать секрецию вазопрессина должна была бы находиться в обратной зависимости от скорости, с которой оно попадает из плазмы в осморецептор [15]. В течение длительного времени считали, что эта скорость проникновения определяется проницаемостью мембраны клеток самого осморецептора, но недавно проведенные исследования указывают на важную роль и гематоэнцефалического барьера [19].
Какова бы ни была функциональная или анатомическая основа специфичности осморецептора, она имеет важное практическое значение, так как ограничивает диагностическую ценность номограмм (см. рис. 9—3) теми клиническими ситуациями, в которых уровень мочевины и глюкозы в плазме находится в пределах нормы. Это означает также, что ни осмоляльность плазмы, ни концентрация в ней натрия порознь не может служить универсальной точкой отсчета при.оценке осморегуляции секреции вазопрессина. Пока не будет проверена способность других присутствующих в плазме растворенных веществ (глицерин, ацетон или аминокислоты) влиять на секрецию вазопрессина, наиболее надежным подходом как в клинических, так и в экспериментальных исследованиях должно быть определение осмоляльности плазмы и концентрации в ней натрия.
На секрецию вазопрессина могут влиять также изменения объема или давления крови. Эти гемодинамические влияния опосредуются в основном афферентными волокнами, идущими от барорецепторов предсердий и дуги аорты и достигающими ствола мозга в составе блуждающего и языкоглоточного нервов (см. рис. 9—1). Точная локализация, число и характер связей, которыми эти сигналы передаются в нейрогипофиз, неизвестны, но в них, вероятно, принимают участие первичные синапсы в ядре солитарного тракта продолговатого мозга с вторичными проекциями на ядра медиодорсальной области заднего гипоталамуса [20].
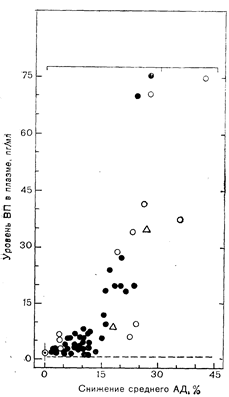
Рис. 9—4. Зависимость уровня вазопрессина в плазме от процента снижения артериального давления (АД) у здоровых взрослых лиц и больных с идиопатической постуральной гипотензией. У здоровых взрослых лиц АД снижали с помощью инфузии триметафана (арфонада) [21] или ортостаза сразу же после кровопускания [22].
Светлые кружки — ортостаз после кровопускания; черные кружки — инфузия триметафана: светлые треугольники — идиопатическая ортостатическая гипотензия.
Здесь сигналы, по-видимому, интегрируются и в составе дорсального продольного пучка достигают нейросекреторных нейронов переднего гипоталамуса.
Функциональные свойства этой гемодинамической системы регуляции представлены зависимостью между уровнем вазопрессина в плазме и изменениями артериального давления (рис. 9—4). У здоровых взрослых лиц резкое снижение артериального давления любым из нескольких способов приводило к повышению уровня вазопрессина в плазме на величину, примерно соответствующую степени достигаемой гипотензии. В отличие от того что наблюдается в системе осморегуляции, эта зависимость между стимулом и реакцией носит отчетливый двухфазный или криволинейный характер. Так, хотя эпизоды умеренно тяжелой гипотензии почти всегда сопровождаются очень значительным повышением уровня вазопрессина в плазме, снижение артериального давления даже на 10% обычно не оказывает такого эффекта. Регуляция секреции вазопрессина у человека изменением объема крови изучена недостаточно, но разные данные, полученные при обследовании человека и в эксперименте у животных, единогласно указывают на то, что регулируемые объемом механизмы реагируют двухфазным, или криволинейным образом, точно так же, как барорегуляторная система [1б]. Так, кровопускание в количестве 500 мл, или примерно 7% от общего объема крови, никогда не приводит к изменению уровня вазопрессина в плазме у здоровых взрослых лиц, находящихся в положении лежа. Вертикальное положение, при котором центральный или эффективный объем крови уменьшается на 8—15%, обычно вызывает 2—3-кратное повышение содержания вазопрессина в плазме. Сочетание кровопускания с ортостазом, которое обычно снижает центральный объем крови настолько, что это сопровождается некоторым снижением артериального давления, почти всегда увеличивается уровень вазопрессина в плазме в 2—3 раза. Относительно малая чувствительность секреции вазопрессина к небольшим колебаниям общего объема крови отчетливо отличается от очень высокой эффективности осмотических стимулов (рис. 9—5). Эту разницу необходимо учитывать при анализе регуляции водного баланса и интерпретации результатов ряда широко применяемых диагностических проб на секрецию вазопрессина.
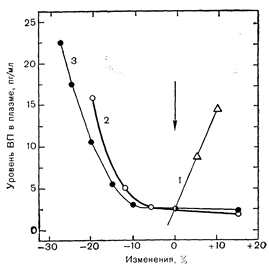
Рис. 9—5. Схематическое изображение зависимости стимул—реакция в отношении уровня вазопрессина (ВП) в плазме и процента изменения осмоляльности плазмы (1) общего объема крови (2) и артериального давления (3) у здоровых взрослых лиц. У экспериментальных животных получены в принципе такие же, но более детализированные кривые в отношении всех трех стимулов [15].
Стрелкой указаны исходные показатели.
Изменения объема или давления крови достаточно значительные, чтобы сказаться на секреции вазопрессина, не обязательно ограничивают влияние осморегуляторной системы [16, 18]. Их эффект, по-видимому, сводится лишь к изменению «настройки» этой системы, что увеличивает или снижает действие данного осмотического стимула (рис. 9—6). Так, даже в условиях значительной гиповолемии и/или гипотензии уровень вазопрессина в плазме все еще может снижаться или повышаться при соответствующих изменениях осмоляльности плазмы. Этот вид взаимодействия между осмотическими и гемодинамическими стимулами может иметь важные физиологические и патофизиологические последствия. Он свидетельствует также о том, что эти две системы регуляции, хотя и различаются по локализации и функции, но в конце концов

Рис. 9—6. Схематическое изображение зависимости между уровнем вазопрессина (ВП) в плазме и ее осмоляльностью в условиях различного объема крови и/или давления. Жирная линия — нормоволемическое и нормотензивное состояние. Цифры со знаком «минус» указывают на процент снижения, а со знаком «плюс» — процент повышения объема и давления крови. замыкаются на одной и той же популяции нейросекреторных нейронов. Как и где происходит такая интеграция — совершенно неизвестно, но, вероятно, в ее осуществлении участвует один или несколько интернейронов, связывающих осморецептор с нейросекреторными клетками [18].
Секрецию вазопрессина могут стимулировать и разнообразные факторы, не связанные с осмотическим давлением или гемодинамикой. Одним из наиболее действенных факторов, по крайней мере у человека, является тошнота [16]. Путь опосредования этого эффекта не полностью ясен, но, вероятно, включает хеморецепторную триггерную зону в area postrema продолговатого мозга (см. рис. 9—1). Он может активироваться различными веществами и процедурами (апоморфин, никотин, алкоголь и рвотный позыв). Их эффект на секрецию вазопрессина проявляется немедленно и крайне интенсивен. Даже при преходящей тошноте, не сопровождающейся рвотой или изменениями артериального давления, нередко можно наблюдать повышение уровня вазопрессина в 100—1000 раз. Предварительное введение флуфеназина (фторфеназин), галоперидола или прометазина (дипразин) [23] в дозах, достаточных для предотвращения тошноты, полностью снимает реакцию вазопрессина. У грызунов, конституционально не способных к рвоте, резко снижена и реакция вазопрессина на апоморфин и другие рвотные стимулы.
Менее эффективным, но столь же постоянным стимулом секреции вазопрессина, является острая гипогликемия [15, 24]. Рецепторы и пути, опосредующие этот эффект, неизвестны, но, по-видимому, отличаются от таковых для осмотических, гемодинамических и рвотных воздействий [25]. Чувствительность этой реакции оценена не точно, но, вероятно, аналогична таковой в отношении гормонов передней доли гипофиза. Снижение уровня глюкозы в плазме натощак на 50% У здоровых взрослых лиц, как правило, повышает содержание вазопрессина в плазме в 2—4 раза, а у крыс — даже в 10 раз. Величина реакции может зависеть также от скорости снижения уровня глюкозы в плазме, поскольку, несмотря на сохранение гипогликемии в течение 1 ч и более, уровень вазопрессина обычно быстро нормализуется. Фактором, «запускающим» секрецию вазопрессина, может быть внутриклеточное содержание глюкозы или одного из ее метаболитов, так как 2-дезоксиглюкоза также является мощным стимулом секреции этого гормона [26, 27].
К регуляции секреции вазопрессина причастна и система ренин — ангиотензин [17, 18, 28]. Ангиотензин, вероятно, действует на одну или несколько областей в ЦНС, поскольку он оказывается наиболее эффективным при инъекции непосредственно в желудочки мозга или мозговые артерии. Уровень ренина и/или ангиотензина в плазме, необходимый для стимуляции секреции вазопрессина, не установлен, но, вероятно, достаточно высок. Практически во всех опубликованных до сих пор работах ангиотензин вводили в дозах, повышающих давление, но тем не менее уровень вазопрессина в плазме повышался лишь в 2—4 раза. Неизвестно, активируется ли когда-либо эндогенная система ренин— ангиотензин в такой степени, чтобы это могло стимулировать секрецию вазопрессина. Та же неопределенность существует в отношении изоренинов, обнаруженных в мозге и СМЖ.
Давно считают, что неспецифический стресс, вызываемый такими факторами, как боль, эмоции или физическая нагрузка, усиливает секрецию вазопрессина [29]. Однако не было показано, опосредуется ли этот эффект особым путем или он является следствием какого-то вторичного стимула, например гипотензии и/или тошноты, которые могут обусловливаться вазовагальным рефлексом на боль или сильную эмоцию. По крайней мере у крыс разнообразные стрессоры, активирующие гипофизарно-надпочечниковую систему, не влияют на уровень вазопрессина в плазме, если они в то же время не снижают артериального давления [16]. Неизвестно, обладают ли животные других видов большей чувствительностью к повреждающим факторам как таковым. Резкое повышение уровня вазопрессина, вызываемое манипуляциями на брюшной полости у человека и собак, находящихся под наркозом, считают результатом раздражения ноцицептивных путей [30, 31], но столь же вероятным объяснением могло бы служить опосредование этого эффекта рвотным рефлексом [16]. Решение этих вопросов важно для понимания регуляции секреции вазопрессина особенно у больных с неадекватной секрецией его в сочетании с тяжелыми болевыми ощущениями.
Секреция вазопрессина изменяется и под действием различных лекарственных средств и гормонов (табл. 9—1) [17, 32]. Многие стимуляторы, например изопротеренол (изадрин), никотин и апоморфин, действуют, вероятно (по крайней мере отчасти), через снижение артериального давления и/или тошноту [16, 17, 23]. Другие, например гистамин, брадикинин, простагландины, b-эндорфин, большие дозы морфина и внутривенное введение цикло-
Таблица 9—1. Лекарственные вещества и гормоны, влияющие на секрецию и эффект вазопрессина
I. Влияние на секрецию А. Стимулирующее
1. Ацетилхолин
2. Никотин
3. Апоморфин
4. Морфин (высокие дозы)
5. Адреналин
6. Изопротеренол (изадрин)
7. Гистамин
8. Брадикинин
9. Простагландины
10. бета-Эндорфин
11. Циклофосфамид (циклофосфан) внутривенно
12. Винкристин
13. Инсулин
14. 2-Дезоксиглюкоза
15. Ангиотензин 16; Хлорпропамид? 17. Клофибрейт? 18. Карбамазепин?
Б. Тормозное
1. Алкоголь
2. Норадреналин
3. Флуфеназин (фторфеназин)
4. Галоперидол
5. Прометазин (дипразин)
6. Оксилорфан, буторфанол, морфин (низкие дозы)
7. Фенитоин (дифенин) внутривенно?
8. Глюкокортикоиды?
II. Влияние на почки А. Потенцирующее
1. Хлоряропамид
2. Индометацин
3. Ацетилсалициловая кислота
4. Тиазиды
5. Клофибрейт?
6. Карбамазепин?
Б. Ингибирующее
1. Барбитураты
2. Литий
3. Тетрациклины
4. Метоксифлуран
5. Глибурид
6. Изофосфамид
7. Алкалоиды барвинка
8. Вазопрессиновая кислота
9. Глюкокортикоиды?
фосфамида (циклофосфан), изучены недостаточно полно, чтобы можно было очертить механизм их действия, но также могли бы влиять с помощью одного или того и другого механизмов. Как уже отмечалось, инсулин и 2-дезоксиглюкоза действуют, по-видимому, вызывая внутриклеточную глюкопению, тогда как ангиотензин обладает неизученным центральным эффектом. Винкристин может действовать путем разрушения микротрубочек в нейрогипофизе и/или периферических нейронах, участвующих в регуляции секреции вазопрессина. По поводу стимулирующего эффекта хлорпропамида, клофибрата и карбамазепина все еще имеются разногласия, и механизм их действия, если он существует, остается неясным.
Вазоактивные вещества, подобные норадреналину, тормозят секрецию вазопрессина путем повышения артериального давления [17]. Дофаминергические антагонисты, подобные флуфеназину (фторфеназин), галоперидолу и прометазину, действуют, вероятно, подавляя активность хеморецепторной триггерной зоны, поскольку они специфически тормозят секрецию вазопрессина только на рвотные, а не осмотические или гемодинамические стимулы. Глюкокортикоиды у здоровых лиц и больных с недостаточностью функции надпочечников, по-видимому, оказывают тормозное действие, но все еще не ясно, действуют они центрально или за счет повышения объема и давления крови. Ингибиторный эффект внутривенного введения фенитоина в лучшем случае непостоянен, и механизм его действия неизвестен. Опиаты, такие, как оксилорфан, буторфанол или низкие дозы морфина, постоянно угнетают секрецию вазопрессина у крыс и обладают, вероятно, аналогичным действием у человека. Механизм их действия пока не установлен, но связан, по-видимому, с их агонистическим, а не антагонистическим влиянием на рецепторы, поскольку тормозное действие всех трех соединений блокируется налоксоном.
Вместе с тем неясно, влияют ли факторы, модулирующие секрецию вазопрессина в плазму из pars nervosa, на его секрецию из двух других отделов нейрогипофизарной системы. Эта неопределенность особенно велика применительно к тубероинфундибулярному тракту, который, как отмечалось, по-видимому, секретирует свои продукты в аденогипофиз по воротным венам. Плазма крови из этих сосудов содержит чрезвычайно высокие концентрации вазопрессина при стрессе, сопровождающем крупные операции и наркоз [З], но неизмененный исходный уровень вазопрессина в этих сосудах и влияние на него более физиологических стимулов остаются неизвестными. Соответствующие сведения имели бы очевидное значение для понимания роли (если таковая имеет место) вазопрессинсодержащих нейронов воронки в регуляции функции передней доли гипофиза. Регуляция секреции вазопрессина в III желудочек и СМЖ изучена не намного лучше, Как у человека, так и у экспериментальных животных концентрация вазопрессина в СМЖ всегда ниже, чем в плазме крови, но при изменениях гидратации или объема циркулирующей крови она повышается или снижается так же, как в плазме.
ОКСИТОЦИН
Отсутствие прямого и специфического метода определения окситоцина в жидких средах организма является значительным препятствием для понимания регуляции его секреции. Существуют биологические методы, как прямые, так и косвенные, но в их специфичности можно сомневаться, поскольку свойствами окситоцина в существенной степени обладает и вазопрессин. Именно эти перекрестные эффекты могут (по крайней мере отчасти) обусловливать представление о реакции окситоцина и вазопрессина на одни и те же стимулы. Недавно удалось разработать более специфический радиоиммунологический метод определения окситоцина, который должен способствовать уточнению и расширению современных представлений о регуляции секреции этого гормона.
Одним из стимулов секреции окситоцина, который уже в настоящее время представляется вполне определенным, является кормление грудью. Эффект опосредуется, по-видимому, чувствительными волокнами, идущими от соска молочной железы в гипоталамус через спинной мозг, ретикулярную формацию и медиальный продольный пучок. По не совсем понятным причинам активация этого пути вызывает вспышкообразную секрецию окситоцина. Аналогичное действие оказывает, по-видимому, расширение шейки матки и/или влагалища. Последнее может определять очень резкое повышение уровня окситоцина, наблюдаемое в родах. Эстрогены, по-видимому, усиливают эффекты многих из этих стимулов, а также увеличивают секрецию окситоцина в исходном состоянии.
НЕЙРОФИЗИН
Каждый из нейрофизинов выделяется, по-видимому, в сопровождении своего гормона [3]. Например, никотин специфически повышает концентрацию в плазме нейрофизина, связанного с вазопрессином, а эстрогены специфически повышают уровень другого нейрофизина, который, как принято считать, связан с окситоцином. Эта зависимость подтверждает экзоцитарную теорию гормональной секреции и в какой-то степени позволяет судить о секреции гормона по результатам определения нейрофизинов в плазме. Однако концентрация нейрофизинов в плазме не всегда изменяется параллельно изменению концентрации гормона. Это расхождение чаще всего наблюдается при действии таких физиологических стимулов, как гипертония, или дегидратация, под влиянием которых уровень вазопрессина в плазме нередко повышается при отсутствии заметного повышения уровня соответствующего нейрофизина. Это может быть следствием чисто методических трудностей определения небольшого прироста содержания нейрофизина из-за малой чувствительности метода определения и/или относительно высокого исходного уровня иммунореактивности нейрофизина в плазме. В исходном состоянии молярное отношение вазопрессина к своему нейрофизину в плазме составляет приблизительно 1:40, что резко отличается от отношения 1: 1, которое следует из результатов опытов по связыванию, а также прямых определений содержания вазопрессина и его нейрофизина в гипофизе. Таким образом, эти два вещества, очевидно, либо совершенно по-разному распределяются и подвергаются клиренсу, либо в каких-то условиях секреции попадают в периферическую кровь в разных количествах.
РАСПРЕДЕЛЕНИЕ И КЛИРЕНС
Попадая в системный кровоток, вазопрессин быстро распределяется по внеклеточной жидкости [16]. У здоровых взрослых лиц равновесие между внутри- и внесосудистым пространствами достигается в основном в течение 10—15 мин. Скорость, с которой вазопрессин диффундирует через капиллярную мембрану, вполне соответствует небольшим размерам его молекул и отсутствию комплексирования с нейрофизином или другими макромолекулярными компонентами плазмы [10, 35]. После уравновешивания концентрация вазопрессина в плазме продолжает снижаться, но уже с меньшей скоростью. Полупериод второй фазы, который предположительно характеризует необратимый или метаболический клиренс, у здоровых лиц значительно варьирует, но в популяции в целом составляет в среднем около 20 мин. Скорость метаболического клиренса, определяемая как в постоянных условиях, так и с помощью метода импульсного введения гормона, также значительно колеблется, но, по данным обоих методов, составляет в среднем около 10 мл/кг в минуту [15, 35]. У мелких животных, например у крыс, для которых характерен сравнительно высокий минутный объем сердца, клиренс вазопрессина обычно протекает гораздо быстрее.
Хотя in vitro многие ткани обладают способностью инактивировать вазопрессин, основной клиренс его in vivo осуществляется, по-видимому, в печени и почках [35]. Это справедливо, очевидно, даже в отношении беременных, в плазме крови которых содержится фермент, способный in vitro быстро разрушать гормон. Ферментативные процессы, с помощью которых печень и почки инактивируют вазопрессин, выяснены недостаточно точно, но, по-видимому, включают начальное восстановление дисульфидного мостика, а затем расщепление связи между 1-м и 2-м остатком аминопептидазой. Дальнейшее разрушение, а также продукты пептида, попадающие в плазму и/или мочу, в настоящее время неизвестны.
Какая-то часть вазопрессина не разрушается и экскретируется с мочой в интактном виде [16, 35]. Это количество может значительно варьировать, но обычно весьма мало по сравнению с метаболизируемой фракцией. У нормально гидратированных здоровых взрослых лиц, например, мочевой клиренс вазопрессина колеблется от 0,1 до 0,6 мл/кг в минуту или составляет примерно от 1 до 5% от скорости общего клиренса. Механизм экскреции вазопрессина изучен недостаточно. По всей вероятности, гормон фильтруется в почечном клубочке, а затем с вариабельной скоростью реабсорбируется в одном или нескольких участках канальца. Этот процесс каким-то образом сопряжен с динамикой натрия в почках, поскольку показано, что мочевой клиренс вазопрессина резко изменяется в тесной зависимости от изменения клиренса растворенных веществ [16]. Определение экскреции вазопрессина не всегда дает надежные указания на изменения его уровня в плазме и результаты таких определений в условиях значительных изменений клубочковой фильтрации и/или экскреции растворенных веществ необходимо трактовать с осторожностью.
Распределение и клиренс окситоцина во многих отношениях аналогичны таковым вазопрессина. О судьбе нейрофизинов в настоящее время почти ничего не известно, за тем исключением, что они также могут обнаруживаться в моче.
ДЕЙСТВИЕ
Наиболее важным биологическим эффектом вазопрессина является сохранение воды в организме путем снижения выделения мочи. Этот антидиуретический эффект осуществляется за счет усиления реабсорбции не содержащей растворенных веществ в дистальных и/или собирательных канальцах почки [36] (рис. 9—7). В отсутствие вазопрессина мембраны, выстилающие эту часть нефрона, формируют непреодолимое препятствие для диффузии воды и растворенных веществ. Гипотонический фильтрат, образующийся в более проксимальных отделах нефрона, без изменения проходит через дистальный каналец и собирательный проток. В таких условиях, называемых водным диурезом, осмоляльность и ток мочи у здорового взрослого человека обычно составляют примерно 60—70 мосммоль/кг и 15—20 мл/мин соответственно.
В присутствии вазопрессина гидроосмотическая проницаемость дистальных и собирательных канальцев увеличивается, что создает возможность диффузии воды по осмотическому градиенту,. существующему в норме между канальцевой жидкостью и изотонической или гипертонической средой коркового и мозгового слоя почки (см. рис. 9—7). Поскольку вода реабсорбируется без растворенных веществ, осмотическое давление оставшейся мочи повышается, а ее объем и скорость тока уменьшаются. Количество воды, реабсорбируе
|
|
|


