 |
Синтез жирных кислот и триглицеридов
|
|
|
|
Исходным предшественником для синтеза жирных кислот является ацетил-СоА, образующийся из глюкозы через пируват в ходе пируватдегидрогеназной реакции (см. ранее) или при окислении амино- или жирных кислот (см. далее). Первой стадией синтеза жирных кислот в цитозоле является карбоксилирование ацетил-СоА с образованием малонил-СоА. Фермент, катализирующий эту реакцию — ацетил-СоА-карбоксилаза, представляет собой ограничивающий скорость пункт биосинтеза жира. Этот фермент требует присутствия биотина в качестве кофактора и аллостерически активируется цитратом. Он ингибируется свободными жирными кислотами и производными жирокислотного ацил-СоА и стимулируется инсулином. Уровень фермента снижается при голодании и диабете и повышается после потребления пищи. Малонил-СоА в свою очередь является мощным ингибитором окисления жирных кислот и кетогенеза [15]. Тем самым избегается «бесполезный» цикл одновременной стимуляции синтеза и окисления жирных кислот.
Для накопления жирных кислот в виде капелек жира в клетках необходима их эстерификация с a-глицерофосфатом, образующая триглицерид. Глицерин-3-фосфат может образовываться при гликолитическом распаде глюкозы до диоксиацетона, который затем в присутствии НАД•Н восстанавливается. Глицерин-3-фосфат может образовываться и из свободного глицерина (высвобождаемого при распаде триглицеридов) в присутствии АТФ и глицерокиназы. Последняя присутствует в печени, но отсутствует в жировой ткани. Синтез триглицеридов в жировой ткани требует не только производных жирокислотного ацил-СоА (либо синтезированных in situ, либо извлекаемых из липопротеинов крови), но и поглощения глюкозы и ее утилизации по пути гликолиза с тем, чтобы получить глицерин-3-фосфат.
|
|
|
Ферменты, необходимые для синтеза жира, присутствуют в разных тканях, особенно в печени, жировой ткани и кишечнике. Однако исследования жировой ткани человека обнаружили относительно низкую скорость включения глюкозы в жирные кислоты [16]. Синтез жирных кислот у человека происходит в основном в печени, откуда они высвобождаются в виде триглицеридов в составе липопротеинов очень низкой плотности (ЛПОНП). Последние служат средством транспорта триглицеридов в жировую ткань, где липопротеиновая липаза катализирует их гидролиз до свободных жирных кислот и глицерина, проникающих в клетку. В жировых клетках протекает реакция реэстерификации между образованным из глюкозы глицерин-3-фосфатом и приносимыми липопротеинами жирными кислотами. Таким образом, синтетическая функция жировой ткани заключается прежде всего в образовании глицерин-3-фосфата, тогда как превращение ацетил-СоА в длинноцепочечные жирные кислоты происходит в печени (рис. 10-6)
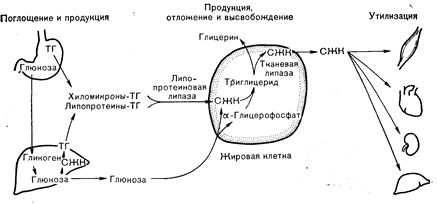
Рис. 10—6. Гомеостаз жира у человека. Жирные кислоты либо поступают в организм в виде триглицеридов (ТГ) с пищей, либо синтезируются из глюкозы в печени. Они транспортируются из кишечника и печени в виде хиломикронов и липопротеинов очень низкой плотности соответственно. Поглощение жировыми клетками прежде всего требует действия липопротеиновой липазы, которая высвобождает свободные жирные кислоты (СЖК), подвергающиеся реэстерификации внутри жировой клетки. Высвобождение из жировой клетки регулируется гормончувствительной тканевой липазой. Затем СЖК могут поглощаться мышцами, сердцем и другими тканями.
МОБИЛИЗАЦИЯ ЖИРНЫХ КИСЛОТ
Хотя жир накапливается в виде триглицеридов, его поглощение и окисление тканями (сердце, мышца, печень) требует высвобождения этих запасов из депо в виде свободных жирных кислот (СЖК), переносящихся с кровью (см. рис. 10—6). Распад триглицеридов в жировой ткани регулируется тканевой липазой, катализирующей следующую реакцию триглицерид + 3Н2О ® 3СЖК + глицерин
|
|
|
Этот процесс, называемый липолизом, находится под регулирующим влиянием различных гормонов (адреналин, гормон роста, инсулин). Фермент получил название гормончувствительной липазы. Адреналин, глюкагон, гормон роста, АКТГ и тиреоидные гормоны повышают его активность, а инсулин снижает ее. Как правило, гормональная активация липазы сопровождается увеличением уровня цАМФ (что и может быть механизмом изменения активности фермента), тогда как инактивация липазы связана со снижением уровня цАМФ. Наиболее важным с физиологической точки зрения активатором гормончувствительной липазы является адреналин, а наиболее важным ингибитором ее инсулин. Маловероятно, чтобы АКТГ или глюкагон играли роль в физиологической модуляции липолиза, поскольку для повышения активности липазы требуются чрезвычайно высокие концентрации этих гормонов.
На скорость липолиза влияет также утилизация глюкозы жировой тканью. Как показано на рис. 10—6, ресинтез триглицеридов может продолжаться до тех пор, пока имеющийся глицерин-3-фосфат обеспечивает возможность эстерификации СЖК. Поскольку в жировой ткани отсутствует глицерокиназа, количество-глицерин-3-фосфата определяется скоростью гликолиза. В условиях повышения утилизации глюкозы мобилизация жирных кислот снижается из-за увеличения количества субстрата их эстерификации независимо от изменений активности гормончувствительной липазы.
ОКИСЛЕНИЕ ЖИРНЫХ КИСЛОТ
Процесс, с помощью которого жирные кислоты окисляются и обеспечивают продукцию макроэргического фосфата в виде АТФ, называется b-окислением, поскольку в нем происходит окисление b-углеродного атома с образованием b-кетокислоты, подвергающейся расщеплению с выходом ацетил-СоА и укороченной на два углеродных атома жирной кислоты. Этот процесс повторяется до тех пор, пока вся жирная кислота не окислится до ацетил-СоА, который поступает в цикл ТКК для последующего окисления до COs.
Начальной стадией окисления жирных кислот является их активация в цитозоле путем образования ацил-СоА-производного. Однако длинноцепочечные ацил-СоА-производные (12 углеродных атомов или более) не в состоянии проникнуть через митохондриальную мембрану. Для этого необходима молекула-переносчик, которой служит карнитин. Ацилкарнитинтрансфераза I катализирует образование жирного ацилкарнитинового производного, пересекающего внутреннюю мембрану митохондрий. Жирная ацильная группа переносится на внутримитохондриальный СоА под действием ацилкарнитинтрансферазы II. Карнитин высвобождается и тем самым становится доступным для переноса других ацильных остатков жирных кислот в митохондрии. Недавно полученные данные свидетельствуют о том, что именно это является лимитирующим скорость ферментативным этапом процесса b-окисления [15]. Кроме того, ацилкарнитинтрансфераза I ингибируется малонил-СоА — первым интермедиатом на пути биосинтеза жирных кислот (см. ранее).
|
|
|
|
|
|


