 |
Патогенез осложнений диабета
|
|
|
|
Один из наиболее важных и нерешенных вопросов диабетологии касается патогенеза хронических микрососудистых и неврологических осложнений [180]. Вообще говоря, существует два главных представления в этой области. Одно из них исходит из того, что микроангиопатиями нейропатия являются следствием гипергликемии и/или других метаболических нарушений, обусловленных недостаточностью инсулина («метаболическая» гипотеза [181]. Согласно второму представлению, эти повреждения генетически обусловлены, возникают независимо от гипергликемии или недостаточности инсулина и в действительности могут опережать любые метаболические сдвиги («генетическая» гипотеза) [182]. Эта проблема имеет не только теоретическое значение, поскольку она тесно связана с вопросами лечения диабета. Сторонники «метаболической» гипотезы обычно считают, что нормализация уровня глюкозы в крови должна предотвратить или свести к минимуму осложнения диабета и поэтому ратуют за «жесткий контроль» инсулинозависимого диабета. В противоположность этому сторонники «генетической» гипотезы пропагандируют «свободный контроль», поскольку (по их представлениям) степень гипергликемии не влияет на развитие осложнений. Указанные разногласия сохраняются и по сей день, когда накоплено много данных, свидетельствующих в пользу как той, так и иной точки зрения. Для решения этой проблемы исследователи используют различные подходы, включающие биопсию тканей, изучение метаболизма в пораженных тканях и оценку влияния лечения на развитие осложнений (табл. 10—15).
Таблица 10—15. Данные, подтверждающие две основные теории патогенеза осложнений диабета
|
|
|
| Метод исследования | «Метаболическая» гипотеза | «Генетическая» гипотеза |
| Изучение биоптатов | Отсутствие изменений в клубочках в первые 2 года заболевания диабетом Сосудистые изменения в интактных почках, пересаженных больным диабетом Гломерулопатия при вторичном диабете | Утолщение базальной мембраны у лиц с предиабетом Повреждения в трансплантированной почке могут быть неспецифическими Гломерулопатии при вторичном диабете развиваются редко |
| Изучение обмена веществ | Повышенное содержание глюкозы в базальной мембране клубочков Повышение уровня гликозилированного гемоглобина Повышение уровня сорбитола в нервной ткани Снижение содержания миоинозитола в нервной ткани | Нормальное содержание глюкозы в базальной мембране клубочков Причинно-следственная связь между метаболическими нарушениями и функциональными и гистологическими нарушениями в пораженных тканях не установлена |
| Эффект лечения | Меньшая выраженность ретинопатии у больных, получающих дробные дозы инсулина Предотвращение ретинопатии у леченных инсулином собак, больных диабетом Регрессия клубочковых повреждений у крыс после трансплантации островков | Данные клинических исследований недостаточно отчетливы Сосудистые повреждения у животных, больных диабетом, могут быть несравнимыми с таковыми у человека |
ИССЛЕДОВАНИЕ БИОПСИЙНОГО МАТЕРИАЛА
Как уже отмечалось, у больных диабетом утолщается базальная мембрана в коже и мышцах, а также в органах, в которых проявляются осложнения диабета — почечных клубочках и сетчатке (см. рис. 10—38). Доступность мышечной ткани для игольчатой биопсии позволила исследовать базальную мембрану капилляров у здоровых людей, у лиц, предрасположенных к заболеванию диабетом, но имеющих нормальную толерантность к глюкозе, и у больных диабетом при различной продолжительности явной гипергликемии. С помощью такого подхода Sipperstein и соавт. [183] обнаружили электронно-микроскопические признаки утолщения базальной мембраны у потомства обоих больных диабетом родителей (т. е. у лиц с предиабетом), хотя у обследуемых не было выявлено нарушений глюкозотолерантности. В отличие от этого William-son и соавт. [184] показали, что утолщение базальной мембраны капилляров в мышцах у лиц с явным диабетом зависит от продолжительности гипергликемии. Кроме того, при исследовании пары однояйцевых близнецов, дискордантных по диабету, базальная мембрана оказалась утолщенной у больного близнеца, но не была изменена у здорового [152]. Результаты обследования индейцев Пима также свидетельствуют в пользу той точки зрения, что утолщение базальной мембраны мышечных капилляров появляется после развития явного диабета, а не опережает его [185].
|
|
|
Хорошо известно, что независимо от состояния базальной мембраны мышечных капилляров клинические признаки поражения капилляров сетчатки и почечных клубочков зависят от длительности течения диабета. Изучение биоптатов показало также, что гистологические изменения в почках отсутствуют в течение не менее 2 лет после развития инсулинозависимого диабета [153, 161]. Важные данные в пользу «метаболической» гипотезы получены и при обследовании больных вторичным диабетом (хронический панкреатит), а также больных первичным диабетом, которым была пересажена почка здорового донора, У больных хроническим панкреатитом и вторичным диабетом наблюдали узелковый и диффузный гломерулосклероз [186], а в здоровых почках, трансплантированных больным диабетом, гиалиноз артериол развивается чаще, чем в почках, трансплантированных лицам, не страдающим диабетом [165]. Аргументы, выдвигаемые против этих наблюдений, заключаются в том, что гломерулопатия при вторичном диабете встречается достаточно редко, чтобы ее можно было уподоблять той, которая сопровождает первичный диабет [187], и что гиалиноз артериол в трансплантированных почках не идентичен диабетическому гломерулосклерозу.
ИЗУЧЕНИЕ МЕТАБОЛИЗМА
Вторым подходом к решению вопроса о патогенезе осложнений диабета является изучение метаболизма в пораженных тканях (базальной мембране, периферических нервах). Такие исследования направлены на поиски метаболического звена, связывающего инсулиновую недостаточность и/или гипергликемию с осложнениями диабета [188]. Beisswenger и Spiro [189] сообщили о большем содержании оксилизина и оксипролина, а также глюкозы и галактозы в базальной мембране капилляров у больных диабетом (аутопсийный материал) по сравнению с таковым у лиц, не страдающих этим заболеванием. Поскольку повышенное содержание глюкозы в гликопротеинах может изменять их форму и ха-
|
|
|

Рис. 10—44. Схематическое изображение предполагаемого механизма, с помощью которого гипергликемия приводит к развитию диабетической нейропатии. а — шванновская клетка при нормальном уровне глюкозы и миоинозитола в плазме: б — то же при гипергликемии, которая обусловливает высокий уровень глюкозы в клетке, в силу чего накапливаются сорбитол и фруктоза. В ответ на осмотический эффект накопления сорбитола в клетку поступает вода. что приводит к ее набуханию. Показано также предполагаемое конкурентное ингибирование (гипергликемией) транспорта миоинозитола в шванновскую клетку, что.приводит к ее обеднению миоинозитолом (по Clements R. С. «Гг., Diabetes, 1979, 28, 604).
рактер упаковки, было выдвинуто предположение, согласно которому избыточное отложение глюкозы может также изменять проницаемость мембраны и играть роль в патогенезе протеинурии. Кроме того, известно, что отложение глюкозы в базальной мембране не зависит от инсулина, в силу чего можно было бы ожидать, что оно увеличивается по мере повышения уровня глюкозы в крови. Несмотря на привлекательность таких представлений, в ряде последующих работ не удалось подтвердить факт увеличения содержания глюкозы или оксилизина в базальной мембране почечных клубочков у больных диабетом [153]. Причина такого расхождения результатов неясна.
Изучали также химический состав и синтез миелина в ткани периферических нервов у животных с экспериментально вызванным диабетом. Gabby и соавт. [13] обнаружили повышенное содержание сорбитола в нервной ткани крыс с диабетом. Сорбитол представляет собой полигидроксилированный спирт (полиол), образующийся из глюкозы под действием фермента альдозоредуктазы (см. выше раздел «Углеводный обмен»). Этот фермент присутствует в нервной ткани и его активность не зависит от инсулина и не насыщается при повышенной концентрации глюкозы в крови. Осмотическая теория, предложенная Gabbay и соавт., заключается в том, что накопление сорбитола приводит к набуханию леммоцитов, в силу чего клетки погибают и демиелинизируются (рис. 10—44). Эту гипотезу подтверждают данные, свидетельствующие о снижении содержания сорбитола в нервной ткани под действием инсулинотерапии, а также о том, что ингибиторы альдозоредуктазы могут предупреждать накопление полиолов, как и замедление нервной проводимости у крыс, которым скармливают галактозу.
|
|
|
Однако предположение о набухании леммоцитов не нашло подтверждения при изучении содержания воды в цитоплазматических элементах нервной ткани [155].
В отличие от сорбитола, количество которого увеличивалось, содержание миоинозитола (полиоловое производное циклогексана) у крыс с экспериментальным диабетом снижалось (см. рис. 10— 44). Потенциальное значение этих данных определяется тем, что восстановление содержания миоинозитола путем его добавления к диете восстанавливало скорость проведения возбуждения по нервам у животных с тяжелым диабетом до нормы [190]. Однако при легкой форме диабета у животных содержание миоинозитола в нервах оставалось нормальным, а его добавка к корму не улучшала нервной проводимости. Кроме того, ограниченные данные в отношении человека не подтверждают ни уменьшения содержания миоинозитола в нервной ткани (материал аутопсии), ни закономерного клинического эффекта миоинозитола, получаемого с продуктами питания больными с нейропатией [155]. Интересно, что данные о повышении тканевого уровня миоинозитола привлекались для объяснения патогенеза и уремической нейропатии.
При диабете в нервах отмечались также изменения в содержании и синтезе миелина. Хотя химический состав миелина остается неизмененным, его общее количество у животных с экспериментальным диабетом снижено. Кроме того, уменьшается и включение лейцина в белки миелина, причем при добавлении инсулина in vitro оно увеличивается [191].
К патогенезу осложнений диабета может иметь отношение и тот факт, что у больных диабетом увеличивается количество гликозилированного гемоглобина (см. выше) [147]. Гликозилированные гемоглобины (гемоглобины A1а, A1b и A1c) представляют собой отрицательно заряженные минорные компоненты гемоглобина. Они отличаются от гемоглобина А присутствием глюкозы или глюкозофосфата, присоединенных к валину на аминоконце b-цeпи так, что появляется основание Шиффа, которое подвергается перегруппировке Амадори с образованием более стабильной кетоаминной связи (Рис. 10—45). Реакция конденсации глюкозы с остатком валина протекает без участия ферментов и зависит от окружающей концентрации глюкозы. Так, при недостаточно компенсированном. диабете общее содержание гемоглобина A1 превышает 12%, тогда как у здоровых лиц и у больных диабетом с менее выраженной гипергликемией его урвень обычно не достигает 6% [148, 149].. Особого упоминания заслуживают данные, свидетельствующие о том, что гликозилирование гемоглобина не ограничивается аминоконцом b-цепи, а захватывает и эпсилон-аминогруппу нескольких лизиновых остатков как a-, так и b-цепи [149]. Кроме того, лизиновые остатки в хрусталике при инкубации его с повышенными концентрациями глюкозы или глюкозо-6-фосфата также подвергаются, неферментативному гликозилированию [192а]. Таким образом, относительная неспецифичность мест гликозилирования позволяет предположить существование более общего феномена, который заключается в том, что гипергликемия обусловливает постсинте-
|
|
|
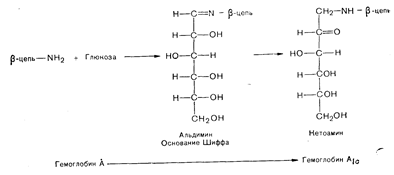
Рис. 10—45. Химические реакции, приводящие к неферментативному превращению гемоглобина А (НbА) в гликозилированный HbA1c. В первой реакции аминоконцевая (валин) аминогруппа b-цепи НbА конденсируется с глюкозой, образуя основание Шиффа. Затем оно подвергается перегруппировке Амадори с образованием более стабильного кетоамина HbA1с. тическую модификацию различных белков, включающих, возможно, белки базальной мембраны и миелина периферических нервов.
Против этих многочисленныхданных, свидетельствующих о химических изменениях в инсулинонезависимых тканях, говорит отсутствие прямых доказательств причинно-следственной связи между этими нарушениями и развитием микроангиопатии или нейропатии [182].
Еще одним метаболическим механизмом, с помощью которого дефицит инсулина мог бы обусловливать развитие осложнений диабета, является нарушение секреции гормона роста. У больных при недостаточной компенсации диабета в покое и даже при средней степени компенсации при физической нагрузке наблюдается гиперсекреция гормона роста. При нормализации гомеостаза глюкозы с помощью инсулина эти изменения исчезают [130]. Merimee [192b] обнаружил, что у карликов с дефицитом гормона роста и сосуществующим диабетом не развивается ни микроангиопатия,. ни нейропатия, несмотря на гипергликемию. Учитывая, однако, этиологическую гетерогенность диабета [110—112], неясно, сам ли по себе дефицит гормона роста или какие-либо другие генетические факторы оказывают у больных диабетом карликов защитное действие в отношении хронических осложнений этого заболевания.
ВЛИЯНИЕ ЛЕЧЕНИЯ
Главный вывод из «метаболической» гипотезы заключается в том, что лечение диабета, приводящее к нормализации содержания глюкозы в крови, должно предотвращать сосудистые и неврологические осложнения. К сожалению, данные, полученные при обследовании больных диабетом, недостаточно четки. Обзор ретроспективных исследований зависимости между «контролем» гликемии и осложнениями диабета не сумел выявить четкого положительного эффекта «жесткого контроля» [193]. Более позднее проспективное исследование, имеющее целью показать положительный эффект дробных инъекций суточной дозы инсулина в отношении профилактики ретинопатии, не успело завершиться, как уже было подвергнуто критике со стороны других исследователей [194].
Однако невозможность обнаружить постоянный положительный эффект «жесткого контроля» гликемии в отношении профилактики осложнений диабета еще не обязательно говорит против существования причинно-следственной связи между гипергликемией и этими осложнениями. В настоящее время известно, что уровень глюкозы в плазме здоровых лиц крайне жестко регулируемый параметр, колебания которого в течение суток редко выходят за пределы 700—1200 мг/л [195]. В то же время даже в самых лучших условиях обычное или даже дробное введение инсулина не снижает среднюю суточную концентрацию глюкозы в плазме или ее колебания до нормальных значений [196, 197]. В связи с этим невозможность предупредить развитие осложнений при диабете может отражать неадекватность принятого в настоящее время лечения, а не неотвратимость прогрессирования генетически обусловленных нарушений в кровеносных сосудах и нервах.
При изучении влияния инсулинотерапии на осложнения у экспериментальных животных с диабетом получают более постоянные результаты, но соответствие этих осложнений микроангиопатии и нейропатии у человека не доказано. У собак с аллоксановым диабетом инсулинотерапия уменьшает частоту ретинопатии [198]. Кроме того, поражения почечных клубочков у крыс со стрептозотоциновым диабетом подвергаются обратному развитию после трансплантации островковых клеток [199]. Однако исходные изменения (до трансплантации) заключаются главным образом в отложении иммуноглобулинов, а не в специфическом утолщении базальной мембраны, наблюдаемом при диабетической нефропатии у человека. После инсулинотерапии у животных с диабетом улучшается и нервная проводимость [155]. Однако поскольку у таких животных отсутствуют неврологические нарушения, сравнимые с диабетической полинейропатией у человека, значение этих данных остается неясным.
РЕЗЮМЕ
Подводя итог, можно считать, что микрососудистые изменения в сетчатке и почках развиваются после (по меньшей мере, через 2 года), а не до развития явного сахарного диабета. Аналогичные изменения появляются при вторичном диабете и, возможно, в нормальных почках, пересаженных больным диабетом. Разнообразные биохимические изменения, в том числе неферментативное гликозилирование и изменение обмена полиолов, могут являться метаболическим звеном, связывающим инсулиновую недостаточность и/или гипергликемию, с одной стороны, и вторичное развитие осложнений диабета, с другой. Тем не менее окончательное доказательство роли именно метаболических, а не генетических факторов в патогенезе осложнений диабета отсутствует. Действительно, обе гипотезы, вероятно, не исключают друг друга. При инсулинозависимом диабете (I тип), продолжающемся в течение 25— 30 лет, Knowles [200] обнаружил прогрессивное увеличение числа случаев микроангиопатии, достигающее максимума распространенности в 80%. Те 20% больных, у которых это осложнение отсутствовало, не отличались от остальных по степени компенсации диабета, но могли отличаться от них по гаплотипу HLA [110, 114]. У этих больных, вероятно, отсутствует какой-то генетический компонент, необходимый для развития осложнений, или, наоборот, присутствует какой-то генетический компонент, обусловливающий «защиту» от этих осложнений. У остальных же 80% больных метаболические изменения, такие, как гипергликемия и/или другие последствия инсулиновой недостаточности, могут играть роль необходимого 1-го этапа клинической экспрессии их генетической предрасположенности к развитию микроангиопатии и нейропатии. К сожалению, нельзя заранее определить больных, обладающих «защитой» от осложнений. В свете современных знаний позиция в отношении лечения должна заключаться в стремлении к максимально возможному восстановлению нормальной метаболической среды без риска развития гипогликемии или нарушения психосоциальной адаптации.
СМЕРТНОСТЬ
За последние 50—60 лет произошло резкое изменение ожидаемой продолжительности жизни, а также причин смерти у больных диабетом. В доинсулиновую эру больные с инсулинозависимым диабетом редко жили больше нескольких месяцев или лет после установления диагноза, а смерть более чем в 40% случаев наступала от диабетического кетоацидоза. В настоящее время на долю кетоацидоза и гиперосмолярной комы приходится только 1 % случаев смерти больных диабетом. Главной причиной смерти является почечная недостаточность (особенно при инсулинозависимом диабете I типа) и. поражение коронарных артерий (особенно при инсулинонезависимом диабете II типа).
ЛЕЧЕНИЕ
Лечение больных диабетом имеет целью: 1) нормализовать углеводный, жировой и белковый обмен; 2) профилактику хронических осложнений (например, микроангиопатии, нейропатии); 3) обеспечить нормальную психосоциальную адаптацию больного; 4) исключить гипогликемию или другие осложнения лечения. Несмотря на то что опыт применения инсулинотерапии насчитывает 60 лет, эти цели в своем полном объеме остаются недостижимыми и в настоящее время. Тем не менее правильное применение инсулина, диеты, физической нагрузки и, когда необходимо, сульфонилмочевинных препаратов может облегчить симптоматику и значительно улучшать метаболическую среду у большинства больных.
В основе всех видов лечения диабета лежит представление о нарушении равновесия между содержанием эндогенного инсулина (т. е. секрецией b-клеток) и количеством инсулина, которое необходимо тканям-мишеням для поддержания нормальной утилизации и мобилизации глюкозы, жира и белка. Нормализация этих метаболических процессов требует приведения в соответствие-«предложения и спроса» инсулина. У больных с инсулинонезависимым диабетом (II тип), из которых у 80% (или более) отмечаются ожирение и инсулинорезистентность, потребность в инсулине-увеличивается на фоне сниженной (но неисчерпанной) секреторной способности b-клеток. Лечение в этих случаях направлено-на снижение потребности в инсулине путем назначения низкокалорийной диеты для уменьшения массы тела. Если диетические-мероприятия не приводят к успеху или недостаточны, в ограниченном числе случаев может оказаться полезной стимуляция эндогенной секреции инсулина с помощью препаратов сульфонилмочевины. В отличие от этого у больных с инсулинозависимым,. склонным к кетозу, диабетом I типа без ожирения отмечается абсолютная недостаточность инсулина, не поддающаяся коррекции при введении сульфонилмочевины или существенно не смягчаю щаяся диетическими мероприятиями. У таких больных краеугольным камнем лечения служит инсулинотерапия.
Лечение различных осложнений диабета (например, фотокоагуляция при ретинопатии, гемодиализ при почечной недостаточности) рассматривалось выше.
ИНСУЛИНОТЕРАПИЯ
Из всех больных диабетом только 15—25% нуждаются в инсулинотерапии. К этой категории относятся: 1) больные инсулинозависимым, склонным к кетозу, диабетом (I тип) независимо от возраста начала заболевания; 2) больные инсулинонезависимым диабетом взрослых (II тип) с гипергликемией, не поддающейся коррекции при соблюдении диеты и/или при введении препаратов сульфонилмочевины; 3) больные инсулинонезависимым диабетом в периоды интеркуррентных «стрессов» (например, хирургическое вмешательство, острые воспалительные заболевания и др.), при которых наблюдается транзиторное снижение метаболизма. Правильное лечение всех этих больных требует детального знания имеющихся препаратов инсулина, а также индивидуального подхода, соответствующего метаболическим, психическим и социальным нуждам больного.
Препараты инсулина
Наиболее широко применяющимися препаратами инсулина являются препараты промежуточного срока действия — изофан (NPH) и инсулин-ленте, а также быстродействующие — обычный
Таблица 10—16. Препараты инсулина
| Препарат инсулина | Действие | Максимум активности, ч | Длительность действия, ч | Буфер | Белок |
| Обычный (нейтральный) | Быстрое | 1—3 | 5—7 | — | — |
| Семиленте | То же | 3—4 | 10—16 | Ацетатный | — |
| NPH | Промежуточное | 6—14 | 18—28 | Фосфатный | Протамин |
| Ленте | То же | 6—14 | 18—28 | Ацетатный | — |
| Ультраленте | Пролонгированное | 18—24 | 30—4С | То же |
и семиленте (табл. 10—16). Кроме того, для продления эффекта инсулина-ленте иногда применяют длительно действующий препарат — ультраленте. Эти препараты инсулина, применяемые порознь или в комбинации, обычно обеспечивают нужды практически всех больных инсулинозависимым диабетом. Протамин-цинк-инсулин и глобин-инсулин, которые все еще имеются в продаже, в современной клинической практике используются реже. Каждый из этих препаратов инсулина представляет собой смесь свиного и бычьего инсулина, хотя для применения в определенных случаях (см. ниже, разделы «Аллергия к инсулину», «Инсулинорезистентность») имеются также инсулины одного биологического вида (например, чистый свиной или чистый бычий инсулин).
Совершенствование промышленного производства инсулина за последние 10 лет увеличило чистоту различных его препаратов [201]. «Монопиковым» инсулином называют инсулин, который при гель-хроматографии дает в основном один пик. Такой инсулин имеет 98% чистоту и содержит меньшее количество макромолекулярных соединений (например, проинсулин), чем препараты, поступавшие в продажу раньше. В настоящее время достигается еще большая степень чистоты препаратов инсулина, имеющихся в продаже. Монокомпонентный инсулин — это инсулин, подвергшийся дальнейшей очистке с помощью хроматографии на DEAE-целлюлозе, обеспечивающей удаление всех, за исключением лишь мельчайших, количеств макромолекулярного материала, что позволяет достичь 99% чистоты и более. Преимущества монокомпонентного инсулина проявляются обычно только у больных с аллергией к инсулину или липоатрофией (см. ниже).
Приблизительные данные о проявлении активности применяемых в настоящее время препаратов инсулина приведены в табл. 10—16. Хотя эти данные характерны для большинства больных диабетом, у некоторых из них нередко отмечаются более медленное начало и большая продолжительность действия того или иного препарата, чем следовало бы ожидать. Отчасти это объясняется появлением антител к инсулину. Таким образом, показатели активности отдельного препарата во времени следует оценивать индивидуально. Кроме того, продолжительность действия инсулина должна зависеть от вводимой дозы. Чем большие количества инсулина вводят, тем длительнее поддерживается его критический уровень, необходимый для стимуляции метаболизма глюкозы в области рецепторов.
Быстродействующую форму инсулина — обычный инсулин (кристаллы цинк-инсулина в прозрачном растворе) до недавнего времени готовили в виде кислого раствора (рН 2,8—3,5), обеспечивающего стабильность гормона. Однако усовершенствование технологии производства позволило получить нейтральный обычный инсулин (обычный инсулин без буфера с нейтральным рН), обладающий повышенной стабильностью и обеспечивающий большую гибкость применения смесей с инсулинами промежуточного срока действия. После подкожной инъекции нейтрального обычного инсулина максимальный гипогликемический эффект (и максимальный уровень иммунореактивного инсулина в сыворотке) наблюдают через 1—3 ч, а возраст уровня глюкозы в крови к исходному—через 5—7 ч. Динамика активности инсулина-семиленте сходна с таковой обычного инсулина, хотя срок наступления его максимального действия (через 3—4 ч) и продолжительность действия несколько больше. Инсулин-семиленте состоит из микрокристаллов цинк-инсулина в ацетатном буфере. Именно микрокристаллическая структура определяет быстрое всасывание этого препарата. Поскольку поддержание компенсации метаболизма при применении только инсулина короткого действия требует частых инъекций в течение суток, инсулинотерапию почти всегда проводят с использованием препаратов более длительного действия.
Потребность в практических равномерно поступающих в организм препаратах инсулина привела Хагедорна к созданию смесей обычного и протамин-цинк-инсулина в стехиометрических соотношениях, что обеспечивает присутствие инсулина в крови но только в течение дня, но и достаточную его концентрацию ночью, т. е. профилактику развития тяжелой гипергликемии натощак в ранние утренние часы. Этот препарат — NPH-инсулин обнаруживает максимальную активность через 6—14 ч после введения. В отличие от протамин-цинк-инсулина его можно смешивать с обычным инсулином без замедления эффекта последнего.
Общей особенностью препаратов группы ленте служит то, что их готовят на ацетатном (а не фосфатном) буфере. Инсулин-ленте обладает точно такой же временной динамикой действия, что и NPH-инсулин, и аналогичными преимуществами в плане возможности смешивания с быстро действующим инсулином. Инсулин-ленте представляет собой смесь быстродействующего инсулина-семиленте (30%) и длительно действующего инсулина-ультраленте (70%). Замедленное всасывание и действие инсулина-ультраленте определяются его крупнокристаллической природой, обусловленной тщательной «подгонкой» рН при изготовлении. Реакцию на инсулин-ленте можно сделать более длительной, добавив к нему препарат ультраленте; можно также усилить его ранний эффект, добавив обычный инсулин или инсулин-семиленте. Хотя инсулин-ленте теоретически обладает преимуществом, поскольку не содержит чужеродного белка (протамин), практическое значение этого не доказано.
Хотя инсулины промежуточного срока действия обычно могут предотвращать выраженную гипергликемию на протяжении боль-щей части дня, максимум их активности не совпадает с увеличением содержания глюкозы в крови, наступающим после еды, и тем самым у большинства больных они не обеспечивают полной ликвидации гипергликемии после еды. У некоторых больных регуляцию уровня глюкозы в крови можно улучшить с помощью.смесей инсулинов (быстродействующий инсулин с инсулином промежуточного срока действия) или дробления доз комбинированных препаратов (утренняя и вечерняя дозы, каждая из которых содержит смесь инсулинов промежуточного и быстрого действия). Несмотря на все эти возможные комбинации, достичь нормализации уровня глюкозы в крови на всем протяжении суток удается редко, разве только у больных с минимальными проявлениями диабета.
|
|
|


