 |
Иммунная тромбоцитопения потребления
|
|
|
|
Иммунная тромбоцитопеническая пурпура взрослых (хроническая ИТП). Аутоиммунная тромбоцитопения является типичной формой тромбоцитопении потребления у взрослых, а ИТП — наиболее характерной формой аутоиммунной тромбоцитопении. Как правило, ИТП поражает женщин в возрасте 20-30 лет (соотношение женщины:мужчины составляет 3:1) и представляет чаще всего изолированную тромбоцитопению умеренной или тяжелой степени. Однако при наличии других гематологических аномалий необходимо учитывать возможность развития системного нарушения, компонентом которого может быть ИТП. Обычно ИТП ассоциируется с системным аутоиммунным заболеванием, например системной красной волчанкой, и лимфопролиферативными нарушениями, особенно хроническим лимфоцитарным лейкозом и болезнью Ходжкина. Сочетание ИТП с аутоиммунной гемолитической анемией получило название синдрома Эванса; в этом случае следует предположить наличие первичного лимфопролиферативного нарушения.
Как и у больных с тромбоцитопенией, у пациентов с ИТП чаще всего наблюдаются петехии, пурпура, кровоточивость десен, меноррагия. Начало симптомов может быть острым или подострым. В противоположность ИТП детского возраста (см. далее), у взрослых в анамнезе нет эпизодов инфекции. Наличие геморрагических пузырьков на слизистой оболочке, носовые и желудочно-кишечные кровотечения менее характерны и являются предвестниками возможного возникновения сильного кровотечения. Селезенка может чрезвычайно активно элиминировать тромбоциты, покрытые антителами, однако развитие спленомегалии не типично для ИТП, поэтому при ее обнаружении врач должен задуматься о правильности поставленного диагноза.
|
|
|
ИТП возникает в результате сенсибилизации аутореактивными антитромбоцитарными антителами, обычно класса IgG, против компонентов тромбоцитарной мембраны. Наиболее часто поражается мембранный гликопротеиновый IIb-IIIa комплекс, хотя могут быть задействованы и другие мембранные гликопротеины. Сенсибилизация аутоантителами к тромбоцитам определяется у 90 % больных с ИТП (на основании выявления у них повышенного количества тромбоцитарного IgG). Однако при измерении уровня связанного с тромбоцитами IgG нередки артефакты, что затрудняет постановку диагноза. Так, содержание связанного с тромбоцитами IgG повышается независимо от уровня циркулирующих в плазме иммуноглобулинов и объема тромбоцитов. Концентрация тромбоцитарного IgG увеличивается также в присутствии циркулирующих иммунных комплексов.
Взрослых больных с ИТП госпитализируют только в случае активного кровотечения или при количестве тромбоцитов менее 10 000-20 000/мкл. С помощью аспирации и биопсии костного мозга подтверждают предполагаемый диагноз, после чего можно начинать лечение. В большинстве случаев ежедневный пероральный прием умеренных доз преднизолона дает положительные результаты. Однако при кровотечении или повышенном риске его развития клиническая реакция наступает значительно быстрее после внутривенного введения иммуноглобулина, высокой дозы метилпреднизолона или их сочетания. При сильном кровотечении в комплекс неотложной терапии следует включить переливание тромбоцитарной массы.
Считают, что эффект кортикостероидов заключается в ингибировании взаимодействия между тромбоцитами, покрытыми IgG, и Fc-рецепторами макрофагов селезенки, что нарушает фагоцитоз. При длительном применении кортикостероиды подавляют, по-видимому, и образование антитромбоцитарных аутоантител. Вводимый внутривенно иммуноглобулин, насыщая Fc-рецепторы селезеночных макрофагов, также эффективен, что связано со снижением скорости фагоцитоза тромбоцитов.
|
|
|
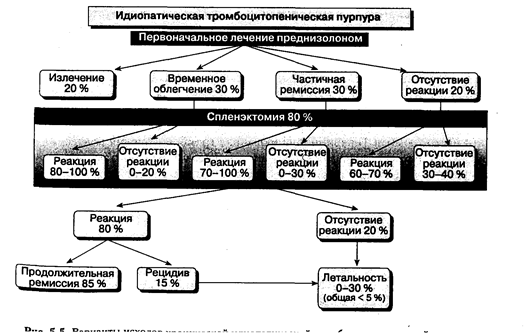
Реакция на эти методы лечения наблюдается обычно в пределах нескольких дней или 1-3 недель. При ее отсутствии следует прибегнуть к альтернативному методу терапии — спленэктомии. Ответ на внутривенно введенный иммуноглобулин может быть временным, и фактически во всех случаях для поддержания необходимого количества тромбоцитов требуется постоянный пероральный прием преднизолона. Стероиды, как правило, продолжают применять в течение 2-3 месяцев, постепенно уменьшая дозу, поддерживая при этом количество тромбоцитов на уровне 30 000-50 000/мкл. У 10-20 % больных таким образом достигается ремиссия и лечение стероидами прекращают. Даже при умеренной хронической тромбоцитопении можно не принимать стероиды, если течение заболевания бессимптомно и функция тромбоцитов нормальна. К сожалению, примерно у 80 % взрослых больных с ИТП возникают рецидивы при уменьшении дозы стероидов и в конце концов требуется выполнение спленэктомии.
Иммунная тромбоцитопеническая пурпура детей (острая ИТП). Хотя клинические проявления ИТП у детей такие же, как у взрослых, патогенез и течение болезни существенно отличаются, что обусловливает разный подход к лечению. Острая ИТП, как правило, наблюдается у детей в возрасте 2-9 лет с максимальной частотой в 3-5 лет. Заболеванию в равной степени подвержены мальчики и девочки. Обычно нарушение возникает после вирусной инфекции (через 1—3 нед). Чаще всего на фоне хорошего самочувствия внезапно возникают петехии и пурпура. Как и у взрослых, у детей ИТП проявляется характерной картиной крови (тромбоцитопения, отсутствие других цитопений или аномальных циркулирующих клеток крови). При физикальном обследовании не обнаруживаются ни лимфаденопатия, ни гепатоспленомегалия. Дифференциальная диагностика изолированной тромбоцитопении у детей значительно проще, чем у взрослых: ИТП составляет более 95 %. Поэтому необходимость исследования костного мозга для подтверждения диагноза является предметом дискуссии. При тромбоцитопении у детей следует также учитывать возможность ВИЧ-инфекции, системной красной волчанки, врожденного гуморального иммунодефицита (особенно IgA). Однако при отсутствии характерных клинических признаков этих заболеваний обычное исследование периферической крови позволяет установить лишь гуморальный иммунодефицит.
|
|
|
В противоположность ИТП у взрослых, когда основной патогенетический процесс — выработка антитромбоцитарных аутоантител, острая ИТП у детей вызвана, как полагают, антителами, направленными против антигенов вирусных белков. Процесс сенситизации циркулирующих тромбоцитов происходит за счет адсорбции на их мембране или вирусного антигена (который впоследствии связывается с антителом), или иммунных комплексов вирус-антитело. Поскольку антигены вируса непременно элиминируются, острая ИТП является самоограниченным заболеванием, которое у 80 % пациентов проходит спонтанно в течение 2 месяцев. Спленэктомия показана редко, так как у 95 % больных количество тромбоцитов достигает приемлемых величин в пределах нескольких месяцев. У детей по сравнению со взрослыми несколько чаще возникает внутричерепное кровоизлияние, нередко без признаков кровотечения, что оправдывает лечение практически всех заболевших с количеством тромбоцитов менее 20 000/мкл. Рекомендуется парентеральная терапия большими дозами стероидов и/или внутривенное введение иммуноглобулина. Из-за высокого риска постспленэктомического сепсиса удаление селезенки у детей относят как можно на более поздний срок.
Иммунная тромбоцитопения, вызванная лекарственными препаратами. Развитие этого вида тромбоцитопении обусловлено взаимодействием принимаемого лекарственного препарата, антител к этому препарату и мембраны тромбоцита. В результате возникает опсонизация и/или активация тромбоцитов. Поэтому индуцированная лекарственным средством тромбоцитопения развивается через 2-3 недели после первичного его приема, т. е. во время пика гуморального иммунного ответа. При повторном воздействии препарата тромбоцитопения может развиться значительно быстрее из-за присутствия уже наработанных антител к лекарственному препарату или мобилизации иммунной памяти. Поскольку для связывания антител с мембраной тромбоцита необходимо наличие препарата то время купирования тромбоцитопении определено кинетикой выведения этого лекарства из организма. Практически в большинстве случаев тромбоцитопения сохраняется еще несколько дней после элиминации вызвавшего ее препарата.
|
|
|
Наиболее часто тромбоцитопения индуцируется гепарином (нарушение развивается у 3-5 % пациентов, получавших гепарин в терапевтической дозе). Обычно это слабая или умеренная тромбоцитопения со средним содержанием тромбоцитов 50 000/мкл. Однако в отдельных случаях количество тромбоцитов снижается до 20 000/мкл, а иногда вызываемая гепарином тромбоцитопения приводит к образованию у больных венозных и артериальных тромбов. Хотя степень риска возникновения связанного с гепарином тромбоза точно не определена, очевидно, что фактически у всех пациентов первым признаком этого грозного осложнения является тромбоцитопения. Учитывая тяжесть течения и высокую летальность при индуцированной гепарином тромбоцитопении, осложнившейся тромбозом, рекомендуется мониторинг количества тромбоцитов у всех больных, получающих гепарин, а при выявлении тромбоцитопении — немедленное прекращение использования этого лекарственного препарата.
В основе механизма развития гепарининдуцированной тромбоцитопении лежит связывание специфических антител с комплексом гепарина и одного из компонентов тромбоцита, который, согласно последним данным, идентифицирован как тромбоцитарный фактор 4. В результате Fc-участок молекулы IgG приближается к Fc-peцептору мембраны тромбоцита и как следствие возникают активация и агрегация тромбоцитов и наблюдается прокоагулянтный эффект. Агрегированные тромбоциты удаляются ретикулоэндотелиальной системой, что приводит к тромбоцитопении. Но если активация и агрегация тромбоцитов выражены достаточно сильно, может иметь место тромбоз. Гепарининдуцированная тромбоцитопения подтверждается при лабораторном исследовании, когда антитела плазмы больного активируют нормальные тромбоциты при терапевтической концентрации гепарина.
Тромбоцитопению вызывают и другие лекарственные препараты за счет связывания мембраны тромбоцита со специфическими антителами, обычно класса IgG.
Хинин и хинидин — типичные лекарственные препараты, индуцирующие тромбоцитопению (вероятность возникновения — 1 на 1000 случаев приема). Клиническое начало тромбоцитопении, вызванной хинином, может быть резким, а сама тромбоцитопения тяжелой. Из-за того, что многие лекарственные средства содержат хинин, необходим тщательный сбор анамнеза, чтобы дифференцировать хинининдуцированную тромбоцитопению от ИТП. Довольно часто наблюдается тромбоцитопения, вызванная препаратами золота (примерно у 2 % больных). Предполагается, что существует генетическая предрасположенность к этому осложнению, так как у большинства пациентов с этим видом тромбоцитопении выявляется антиген гистосовместимости HLA-DR3. Заболевание протекает вяло и проходит в пределах нескольких недель, что, возможно, обусловлено продолжительным периодом полураспада золота, а также тем, что золото стимулирует образование аутоантител к тромбоцитам. Тромбоцитопению могут также вызвать дигоксин, рифампицин, сульфаниламиды.
|
|
|
При лечении прежде всего необходимо идентифицировать и удалить этиологический фактор. Если больной получает лекарства нескольких наименований, необходимо прекратить прием всех препаратов или заменить их, за исключением наиболее важных. Особое внимание следует обратить на перечисленные выше лекарственные средства, вызывающие тромбоцитопению. Большинство клиницистов полагает, что тяжелую тромбоцитопению, индуцированную лекарственными препаратами, следует лечить умеренными дозами кортикостероидов. Рациональной альтернативой может служить и внутривенное введение иммуноглобулина. При тромбоцитопении, возникшей вследствие приема гепарина, переливание тромбоцитарной массы не рекомендуется.
Другие причины иммунной тромбоцитопении. Посттрансфузионная пурпура представляет собой редкую, но тяжелую форму иммунной тромбоцитопении в результате аллоиммунизации. Обычно это нарушение развивается через 1 неделю после гемотрансфузии и проявляется тяжелой рефракторной тромбоцитопенией и кровотечением. Высокая летальность при посттрансфузионной пурпуре обусловлена внутричерепными кровоизлияниями. В связи с этим большое значение имеют ранняя диагностика и рациональная терапия. Как правило, заболевают повторно родящие женщины или те пациенты, которым ранее переливали кровь или ее компоненты. Это редкое нарушение встречается у людей с отсутствием тромбоцитарного антигена PlА1 (приблизительно 2 % населения) после переливания продуктов крови, положительных по PlА1. Происходит выработка эндогенных антител к Р1А1-антигену, которые разрушают не только аллогенные тромбоциты, но и собственные тромбоциты больного, отрицательные по Р1А1. Причина аутореактивности этих анти- Р1А1антител неясна. По последним данным, эффективным оказывается раннее лечение внутривенным введением иммуноглобулина, которое может спасти жизнь больного.
Аутоиммунная тромбоцитопения новорожденного. Заболевание может развиваться у младенцев в результате трансплацентарной передачи материнских антител, вступающих в реакцию с тромбоцитами плода. Полагают, что наиболее вероятный патогенез заболевания – иммунизация Р1А1 – отрицательной матери тромбоцитами плода, несущими этот антиген. Возможна несовместимость и по другим антигенам тромбоцита. В противоположность посттрансфузионной пурпуре данный процесс обычно не затрагивает мать. Ребенок при рождении имеет слабую тромбоцитопению, которая усиливается в 1-2 недели жизни и исчезает к 4-й неделе. Лечение рекомендуется только при тяжелой форме нарушения и сводится к переливанию отмытых тромбоцитов матери и/или к введению иммуноглобулина внутривенно.
|
|
|


