 |
Радикальная полимеризация. Основные мономеры и инициаторы. Элементарные реакции радикальной полимеризации. Приведите примеры.
|
|
|
|
Радикальная полимеризация – полимеризация, инициированная свободными радикалами, генерируемыми в реакционной среде.
Радикальная полимеризация — процесс получения ВМС из низкомолекулярных соединений без выделения побочных продуктов, где активный центр — свободно-радикальная частица (частица с неспаренным электроном). Данный процесс осуществляется за счет кратных связей (С=С, С=О и др.) или раскрытия циклов, содержащих гетероатомы (N, S, O). Продукты полимеризации имеют тот же элементный состав, что и исходные мономеры.
Элементарные реакции радикальной полимеризации:
1. Инициирование радикалов (образование активных центров)
2. Рост цепи (последовательное присоединение мономеров к активному центру)
3. Бимолекулярный обрыв цепи (гибель активного центра)
4. Передача цепи (передача активного центра на другую молекулу)
5. Ингибирование
Мономеры, способные вступать в реакции радикальной полимеризации
В реакции радикальной полимеризации способны вступать мономеры винилового ряда (идет раскрытие связи С=С):
1)  - этилен
- этилен
2) монозамещенные этилена:

в качестве радикала R могут быть различные группировки:
-Cl, -Br, -F, -Ph, -CN, -COOH, COOR, -CНO, 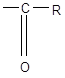
-C(O)NH2 и некоторые другие группы.
3) дизамещенные этилена:

в качестве R1 и R2 могут быть те же группы атомов, что и в случае (2)
4) тризамещенные этилена:

радикальная полимеризация данных мономеров обычно происходит сложно из-за возникающих стерических затруднений
5) четырехзамещенные этилена:

полимеризация затруднена, она может и не происходить.
К гомополимеризации способны мономеры с малыми по размерам заместителями (например, тетрафторэтилен полимеризуется хорошо).
|
|
|
Кроме того, все, в том числе трех- и четырехзамещенные, мономеры в реакциях сополимеризации могут вступать как сомономеры.
6) некоторые циклические структуры:
обычно вступают в реакции как сомономеры, гомополимеризации обычно не происходит.
Пример:
 - ангидрид малеиновой кислоты не способен к гомополимеризации, но легко сополимеризуется.
- ангидрид малеиновой кислоты не способен к гомополимеризации, но легко сополимеризуется.
7) мономеры диенового ряда (бутадиен и его производные):
 -бутадиен
-бутадиен
Может происходить 1,2-, 3,4- и 1,4-присоединение мономера.
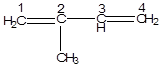 -изопрен
-изопрен
1,2- и 3,4- связи в этом случае неравноценны.
Кроме этого, возможно 1,4-присоединение. В этом случае образуются 2 типа структур – цис- и транс-структуры. Существенно расширяются возможности синтеза разнообразных соединений, селективность реакции невысока.
8) некоторые соединения, содержащие несопряженные двойные связи:
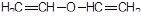 - дивиниловый эфир
- дивиниловый эфир
Полимеризация диметилаллиламмоний хлорида идет с образованием цикла:

9) раскрытие радикалами связей С=О, C=S,  не происходит.
не происходит.
10) в процессах радикальной полимеризации также редко происходит раскрытие циклов, исключение составляют системы:
а) в циклах, где двойная связь сопряжена со связью в напряженном цикле:


идет разрыв связи, сопряженной с фенильной группой в цикле, образовавшийся радикал атакует далее следующий мономер по концевой CH2- группе.
б) с очень неустойчивыми циклами:

11) соединения ацетиленового ряда практически не участвуют в реакциях радикальной полимеризации.
Инициирование (образование свободных радикалов)
Принцип заключается в использовании веществ-инициаторов (перекиси, азосоединения, red-ox системы), у которых энергия обрыва химической связи значительно меньше, чем у мономеров. При этом процесс происходит в две стадии: сначала генерируются радикалы инициатора, которые затем присоединяются к молекуле мономера, образуя первичный мономерный радикал.
|
|
|
Стадия

Стадия

Инициатор очень похож по свойствам на катализатор, но его отличие состоит в том, что инициатор расходуется в процессе химической реакции, а катализатор - нет.
Стадия инициирования – это стадия образования свободных радикалов.
В общем виде стадию инициирования представляют следующим образом:

Соединения, способные образовывать свободные радикалы:
1. Перекисные соединения (пероксиды):

т.е. имеющие в своем составе пероксидную группу
Примеры инициаторов этого класса:
 - пероксид водорода
- пероксид водорода
Распад идет при температурах выше 60˚С.

- третбутилпероксид
распад идет при температурах, больших 100˚С.

-перекись бензоила
распад идет при 60˚С
Бензоильный радикал может дальше распадаться с образованием фенильного радикала.

- дициклогексилпероксодикарбонат
распад идет выше 30˚С
сложный радикал циклогексилпероксокарбоната распадается далее с выделением CO2

- гидроперекись бензойной кислоты
далее идет распад образовавшегося радикала:
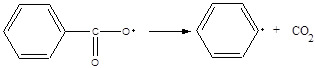
|
|
|


