 |
10.Дезаминирование аминокилот. Катаболизм аминокислот начинается с дезаминирования. Прямое окислительное дезаминирование
|
|
|
|
10. Дезаминирование аминокилот
Катаболизм аминокислот начинается с дезаминирования
У человека основным способом дезаминирования является окислительное дезаминирование. Выделяют два варианта окислительного дезаминирования: прямое и непрямое.
В природе известны четыре основных типа дезаминирования.
Восстановительное дезаминирование:

Гидролитическое дезаминирование:

Внутримолекулярное дезаминирование:

Окислительное дезаминирование:

Прямое окислительное дезаминирование
Прямое дезаминирование катализируется одним ферментом, в результате образуется NH3 и кетокислота. Прямое окислительное дезаминирование может идти в присутствии кислорода ( аэробное ) и не нуждаться в кислороде ( анаэробное ).
1. Аэробное прямое окислительное дезаминирование катализируется оксидазами D-аминокислот ( D-оксидазы ) в качестве кофермента использующими ФАД, и оксидазами L-аминокислот ( L-оксидазы ) с коферментом ФМН.

2. Анаэробное прямое окислительное дезаминирование существует только для глутаминовой кислоты, катализируется только глутаматдегидрогеназой, превращающей глутамат в α -кетоглутарат. Фермент глутаматдегидрогеназа имеется в митохондриях всех клеток организма (кроме мышечных). Этот тип дезаминирования теснейшим образом связан с трансаминированием аминокислот и формирует с ним процесс трансдезаминирования (см ниже).

В печени реакция используется для получения аммиака из его транспортной формы глутаминовой кислоты. Далее аммиак входит в реакции синтеза мочевины.
10. Трансаминирование и декарбоксилирование.
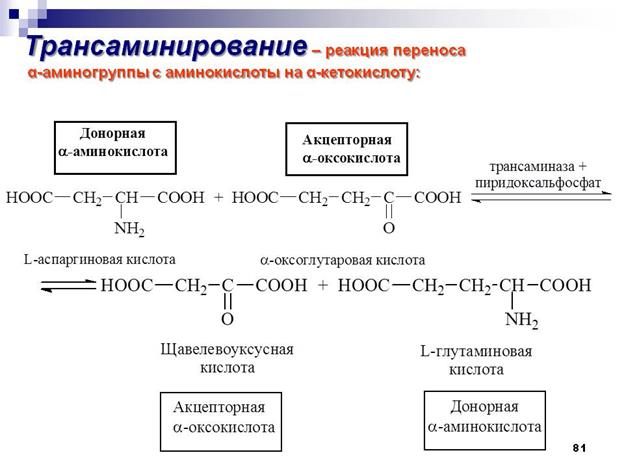
Трансаминирование
Реакции трансаминирования протекают в 2 стадии. На первой стадии к пиридоксальфосфату в активном центре фермента присоединяется аминогруппа от первого субстрата – аминокислоты. Образуется комплекс фермент- пиридоксаминфосфат и кетокислота – первый продукт реакции. Этот процесс включает промежуточное образование 2 шиффовых оснований (альдимин и кетимин).
|
|
|
На второй стадии пиридоксаминфосфат соединяется с новой кетокислотой (второй субстрат) и снова через промежуточное образование 2 шиффовых оснований передает аминогруппу на кетокислоту. В результате фермент возвращается в свою нативную форму, и образуется новая аминокислота – второй продукт реакции.
Чаще всего в реакциях трансаминирования участвуют аминокислоты, содержание которых в тканях значительно выше остальных – глутамат, аланин, аспартат. Наиболее распространенными в большинстве тканей являются аланинаминотрансфераза (АлАТ) и аспартатаминотрансфераза (АсАТ).
Наибольшая активность АсАТ обнаруживается в клетках сердечной мышцы и печени, в то время как в крови обнаруживается только фоновая активность АлАТ и АсАТ. Поэтому можно говорить об органоспецифичности этих ферментов, что позволяет их широко примененятьих с диагностической целью (при инфарктах миокарда и гепатитах).
Роль трансаминирования и трансдезаминирования
Реакции трансаминирования:
· активируются в печени, мышцах и других органах при поступлении в клетку избыточного количества тех или иных аминокислот – с целью оптимизации их соотношения,
· обеспечивают синтез заменимых аминокислот в клетке при наличии их углеродного скелета (кетоаналога),
· начинаются при прекращении использования аминокислот на синтез азотсодержащих соединений (белков, креатина, фосфолипидов, пуриновых и пиримидиновых оснований) – с целью дальнейшего катаболизма их безазотистого остатка и выработки энергии,
|
|
|
· необходимы при внутриклеточном голодании, например, при гипогликемиях различного генеза – для использования безазотистого остатка аминокислот в печени для кетогенеза и глюконеогенеза, в других органах – для его прямого вовлечения в реакции цикла трикарбоновых кислот.
При патологиях (сахарный диабет 1 типа, гиперкортицизм) реакции трансаминирования обусловливают появление субстратов для глюконеогенеза и способствуют патологической гипергликемии.
Продукт трансаминирования глутаминовая кислота:
· является одной из транспортных форм аминного азота в гепатоциты,
· способна реагировать со свободным аммиаком, обезвреживая его (синтез глутамина).
Процесс трансдезаминирования идет в организме непрерывно, потому что:
· сопряженные реакции трансаминирования и дезаминирования создают поток лишнего аминного азота из периферических клеток в печень для синтеза мочевины и в почки для синтеза аммонийных солей.
|
|
|


