|
Описание микроскопа и работы с ним. 4 страница
|
|
|
|
Морских свинок берут из клетки одной рукой, обхватывая туловище позади передних конечностей. Морских свинок фиксируют двумя руками — одной зажимают задние ноги, другой — передние ноги и голову (б).
Белых крыс захватывают рукой вокруг туловища позади передних конечностец. Большой палец должен находиться под нижней челюстью. Частая ошибка в обращении с крысами — слишком крепкий захват животного. Это вызывает у крыс тревогу и она может укусить. Если крыса проявляет агрессивность, то следует пользоваться корнцангом.
Белых мышей из клетки извлекают корнцангам или берут за хвост »и быстро придают мышке висячее положение вниз головой. Затем пускают мышь к себе на халат или на стол, быстрым движением схватывают ее за кожную складку в области затылка и фиксируют мышь, растягивая ее двумя руками. Все, манипуляции следует делать быстро во избежание покусов. Если не удается схватить мышь за кожу в области затылка, можно предварительно, держа мышь за хвост, проделать несколько вращательных движений.
При работе без помощника мышь фиксируют двумя длособами. 1. Захватывают ее кровоостанавливающим пинцетом (Пеана или Кохера) за кожную складку в области затылка и одевают пинцет кольцами для пальцев на какой-либо предмет (например, на стержень штатива для бюретки). Одной рукой удерживают мышь за хвост, а другой — производят инъекцию. 2. Большим и указательным пальцами быстро схватывают мышь за кожную складку в области затылка, переворачивают ее брюшком кверху, захватив при этом хвост и левую заднюю конечность мизинцем и безымянным пальцем этой же руки. Инъекцию производят другой рукой (в, г).
Голубей фиксируют одной рукой, обхватывая туловище и прижимая одновременно оба крыла и обе конечности к телу.
|
|
|
При фиксации лабораторных животных следует соблюдать осторожность, чтобы обезопасить себя и не причинить вреда животным грубой фиксацией.
Способы заражения лабораторных животных. Лабораторных животных чаще всего заражают подкожно, внутримышечно, внутрибрюшинно, внутривенно. Иногда прибегают к внутрикожному, внутримозговому способам «заражения; заражают жиротных через пищеварительный тракт, а также путем аппликации материала на коньюнктиву или на скарифицированную поверхность кожи. На месте инъекции шерсть выстригают, кожу обрабатывают спиртом или 2%-ным раствором карболовой кислоты. Подкожно материал вводят кроликам в области спины или живота; морским свинкам в области живота; белым'мышам— в области спины у корня хвоста. Чтобы предупредить обратное вытекание. материала, место укола захватывают пинцетом и сжимают; можно заклеить его кусочком ваты, смоченным коллодием. Объем вводимого подкожно материала обычно для кролика 0, 5—2 мл; для морской свинки — 0, 5—1 мл; для белой мыши 0, 2—0, 5 мл.
При внутримышечном способе заражения материал вводят кроликам, морским свинкам и белым мышам в толщу мышц с внутренней стороны бедра; голубям — в грудную мышцу после предварительного выщипывания перьев на месте инъекции, при этом иглу следует направлять в сторону головы, а не в сторону туловища, т. к. в последнем случае можно повредить брюшину.
При внутрибрюшинном способе заражения животное фиксируют вниз головой (во избежание ранения кишечника). Применяют короткие, с тупым жалом иглы. Инъекцию производят в левую нижнюю треть живота. Сначала иглу направляют горизонтально, прокалывая одновременно кожу, мускулатуру и брюшину. Затем переводят шприц в вертикальное положение и медленно вводят материал.
Внутривенный способ заражения применяют чаще всего у кроликов. Инъекцию делают в краевую вену уха. Шерсть на месте введения выщипывают, место инъекции дезинфицируют. У основания уха сосуд передавливают пальцами для лучшего наполнения его кровью. Можно предварительно протереть ухо ксиолом или пощелкать по нему. Это вызывает наполнение сосудов кровью и облегчает введение иглы в вену. Левой рукой берут ухо кролика так, чтобы указательный палец был снизу, а большим пальцем прижимают ухо сверху. Для удобства ухо слегка перегибают на указательном пальце. Правой рукой берут шприц, снабженный тонкой иглой, и вводят иглу в вену по ходу тока крови (по направлению к голове) (рис. 13). При правильном введении иглы в вену материал поступает свободно при легком нажатии на поршень. При неправильном положении игль? на месте инъекции образуется вздутие; в этом случае инъекцию повторяют ближе к основанию уха.
|
|
|
Материал внутривенно следует вводить медленно. Доза для кролика составляет обычно 1—5 мл. После инъекции на место укола накладывают кусочек ваты.
После заражения животных помещают в отдельные клетки (мышей можно содержать в стеклянных банках, закрытых сверху металлической сеткой). На клетки или банки наклеивают, этикетки с указанием номера клетки или банки, фамилии ответственного за опыт сотрудника (учащегося), даты, числа и вида животных, чем заражены животные, способа заражения, введенной дозы, как помечены животные.
Зараженных животных содержат в отдельных помещениях, изолированно от здоровых; их обслуживает отдельный персонал.
Вскрытие трупов лабораторных животных. Павших лабораторных животных вскрывают и проводят патоло- гоанато. мические и микробиологические исследования.
Вскрытие трупов следует производить тотчас после смерти животного. Трупы вскрывают на столах, обитых оцинкованным железом или в металлических ванночках. Д«ця удобства их укрепляют булавками, кнопками или гвоздями на деревянной или пробковой доске, которую" затем помещают в ванночку. Можно залить ванночку расплавленным воском. На застывшем воске труп фиксируют булавками. После вскрытия воск обеззараживают перетапливанием.
Перед вскрытием приготавливают инструменты (скальпели, ножницы, пинцеты), а также все необходимое для производства посевов и изготовления мазков: предметные стекла, пастеровские пипетки и бактериологические петли, шпатель для прижигания, спиртовку, питательные среды, карандаш по стеклу, сосуд с дезинфицирующей жидкостью, тетрадь для записи.
|
|
|
Для дезинфекции внешних покровов и для уничтожения накожных паразитов трупы на несколько минут погружают в 2%-ный раствор карболовой кислоты. Можно овлажнить шерсть спиртом и затем обжечь ее.
Вскрытие начинают разрезом по белой линии живота от лобка до шеи. Кожу отпрепаровывают по сторонам. Грудную полость вскрывают ножницами, разрезая сначала диафрагму, затем ребра с обеих сторон по месту прикрепления их к грудной кости, последнюю отделяют от трупа. Для лучшего осмотра органов брюшной полости разрезают брюшную стенку перпендикулярно первому разрезу в обе стороны до поясничных позвонков. При необходимости вскрывают черепно-мозговую по- ЛЬсть и исследуют головной мозг.
. После беглого осмотра органов делают посевы из внутренних органов и крови сердца (см. занятие 6), изготавливают мазки-отпечатки из органов (см. занятие 3) и после этого производят тщательное патологоанато- мическое исследование. Результаты осмотра трупа и па- тологоанатомического исследования вносят в бланк лабораторной экспертизы.
Инструменты после работы стерилизуют кипячением;
труп животного сжигают или автоклавируют. Стол и ванночки заливают на 2 ч 3%-ным раствором карболовой кислоты или 5%-ным раствором лизола. Столы можно овлажнить спиртом и затем прожечь. Клетку, в которой пало лабораторное животное, дезинфицируют, подстилку и остатки корма сжигают.
Взятие крови у лабораторных животных. Кровь у •лабораторных животных берут для исследования, а также для изготовления комплемента и сывороток, необходимых для серологических реакций. У морских свинок и кроликов кровь можно брать из ушной вены или из сердца.
Из ушных вен кровь берут путем надреза или прокола сосуда. Удобно брать кровь из краевой вены ух^а. Шерсть на месте операции выстригают или выщипывают. Для лучшего наполнения сосудов ухо протирают ваткой, смоченной ксилолом. У основания уха сосуд зажимают и острым скальпелем или бритвой делают поперечный надрез его. Первую каплю крови убирают стерильной ватой, затем к месту надреза приставляют пробирку (14 Хб5 мм) и заполняют ее кровью (рис. 14, а), причем кровь должна идти непрерывной струей по стенке пробирки. У белых мышей кровь берут, отсекая кончик хвоста, или путем укола пастеровской пипеткой в сосудистое сплетение, расположенное в области внутреннего угла глаза.
|
|
|
Большое количество крови (и более стерильно) мож-. но взять у кролика или морской свинки при помощи пункции сердца. Помощник фиксирует свинку на столе в спинном положении, чуть наклонив ее на себя; левым боком к оператору. Указательным пальцем левой руки^ оператор отыскивает точку, где сильнее всего ощущается сердечный толчок. Этой точкой обычно'является середина грудной клетки, несколько влево (0, 5—1 см) от средней линии. Для получения крови берут 5—10-грам-1 мовый шприц с толстой иглой длиной 2 см. Жало иглы должно быть предварительно слегка сточено. Шерсть на месте укола выстригают, место укола дезинфицируют.
Грудную стенку прокалывают, держа шприц правой рукой в несколько наклонном положении, спереди назад (рис. 14, б). При проколе надо указательный палец держать на штоке поршня и стараться слегка отодвигать его, чтобы в цилиндре создавалось отрицательное давление (разряжение воздуха). При правильном попадании поршень легко поднимается, а цилиндр заполняется кровью.
От взрослой морской свинки можно взять однократно 5—6 мл крови, от кролика — до 10 мл крови. После этого животному тотчас вводят подкожно физраствор, подогретый до температуры тела, соответственно количеству взятой крови. Повторно кровь у этого же животного можно брать не ранее, чем через 10-^15 дней.
«Занятие 9. КУЛЬТИВИРОВАНИЕ ВИРУСОВ В КУРИНЫХ ЭМБРИОНАХ И В КУЛЬТУРЕ КЛЕТОК КУРИНЫХ ФИБРОБЛАСТОВ
Задание. 1. Провести овоскопию куриных эмбрионов ДМя отбора живых оплодотворенных эмбрионов.
2. Научиться заражать куриные эмбрионы в аллан- тоисную полость.
3. Овладеть техникой вскрытия эмбрионов.
4. Ознакомиться с методом культивирования клеток куриных фибробластов (КФ) и техникой их заражения.
Основное оборудование и материалы. Куриные эмбрионы на 9—10-й день инкубации, вируссодержащий материал (вакцинный штамм вируса болезни Ньюкасла), органы и ткани животных, павших от незаразных болезней. Физиологический раствор, мясо-пептонный бульон (в колбах), спирт, йодированный спирт, 5%-ный раствор йода, антибиотики (пенициллин, стрептомицин), 0, 2%-ный раствор трипсина, солевой раствор Хенкса, питательная среда с 0, 25%-ным ФГМС на растворе Эрла, нормальная сыворотка крови крупного рогатого скота (готовые растворы и среды приобретают через конторы «Зооветснаба»). Овоскоп (ящик с электролампочкой внутри и отверстием для просмотра эмбрионов), штативы для куриных эмбрионов, чашки Петри, конические колбы на 100—250 мл, мерные стаканчики, пробирки, баночка с тампонами, шприцы (по 1 мл) с иглами, резиновые пробки, * 'стеклянные воронки, пинцеты, ножницы с прямыми и изогнутыми концами, пастеровские пипетки, мерные пипетки на 1—2 мл, иглы для взятия крови, вата, марля, парафин или лейкопластырь, фарфоровые ступки с пестиками, газовые или спиртовые горелки, магнитная мешалка, стерилизатор, счетная камера Горяева, микроскопы, тер- ^ мостат.
|
|
|
Место занятия. Лаборатория техникума, вирусологический отдел ветеринарной лаборатории.
Методика проведения занятия. Преподаватель показывает как производится овоскопия (просвечивание) куриных эмбрионов с целью установления их развития. Обращает внимание на то, как отличать живых эмбрионов от погибших. Учащиеся самостоятельно овоскопи- руют эмбрионы, отмечают карандашом места проколов скорлупы.
Затем преподаватель демонстрирует различные методы заражения куриных эмбрионов, после чего учащиеся самостоятельно заражают куриные эмбрионы в аллантоисную полость. Для заражения
можно использовать вакцинный штамм вируса ньюкаслской болезни, органы и ткани животных, павших от незаразных болезней или стерильный физраствор. Зараженные эмбрионы помещают в термостат. Преподаватель показывает технику вскрытия эмбрионов; учащиеся самостоятельно вскрывают 1—2 эмбриона и описывают наблюдаемую при этом картину.
На этом же занятии преподаватель объясняет для чего служат клеточные культуры, демонстрирует под микроскопом заранее приготовленные незараженные культуры куриных фибробластов и культуры этих, же клеток с наличием цитопатогенного действия (ЦПД), вызванного вакцинным штаммом вируса болезни Ньюкасла (ЦПД можно имитировать прогреванием культуры клеток до закипания в них сре;? ы). Затем преподаватель объясняет как изготавливают куль-" туры КФ и как производят их заражение. После этого учащиеся самостоятельно проводят изготовление и заражение культуры клеток.
Заражение куриных эмбрионов производят с диаг ностической целью для обнаружения и идентификации вирусов, а в биологической промышленности — для изготовления вакцин и антигенов. С этой целью берут свежие оплодотворенные инкубированные при 38°С яйца, озоско- пируют (просвечивают) их в темной комнате, чтобы выявить неоплодотворенные яйца и отличить живые эмбрионы от погибших. Неоплодотворенные яйца прозрачны. В оплодотворенных инкубированных яйцах обнаруживают движение эмбрионов и наполнение кровью сосудов хориоаллантоисной оболочки.
Для заражения отбирают яйца с живыми эмбрионами, отмечают простым карандашом границу пуги (воздушное пространство со стороны тупого конца яйца). Куриные эмбрионы заражают вируссодержащим материалом (органы и ткани больных животных и т. п. ). Его растирают в фарфоровой ступке, суспендируют в- мясо-пептонном бульоне (1: 10), фильтруют через 3—4 слоя марли, добавляют растворы антибиотиков (100— 200 ЕД пенициллина и 100—150 ЕД стрептомицина на 1 мл суспензии). Заражают эмбрионы в стерильных условиях — в боксе, который представляет собой специальную комнату с остекленными перегородками. Предварительно бокс дезинфицируют — распыляют 5%-ный раствор карболовой кислоты, после чего включают бактерицидные лампы на 30—40 мин.
Чаще всего заражают эмбрионы в аллантоисную полость. Скорлупу со стороны пуги дезинфицируют йодированным спиртом или прожигают пламенем спиртового ватного тампона, смазывают 5%-ным раствором йода, стерильной иглой прокалывают скорлупу и через это
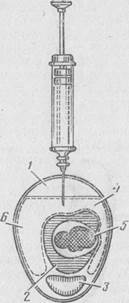
Рис. 15. Заражение куриных эмбрионов в аллантоисную полость:
/ — воздушная камера; 2 — желточный мешок; 3 — белок; 4 и 6 — хориоаллантоисная полость; 5 — зародыш.
отверстие из шприца с иглой вводят в аллантоисную полость материал, используемый для заражения (рис. 15). Затем с помощью пастеровской пипетки заливают отверстие расплавленным парафином или заклеивают лейкопластырем.
Зараженных эмбрионов помещают в термостат при температуре 36—37, 5°С. Сюда же ставят кювет с водой для поддержания влажности в термостате. Длительность инкубирования эмбрионов зависит от характера вируса. Изменения можно обнаружить, как правило, уже к 48—96-му часу. Зараженные эмбрионы ежедневно осматривают, овоскопируют, поворачивая каждый раз другой стороной. Погибших эмбрионов сразу же вскрывают или сохраняют при температуре 4°С.
|
|
Вскрытие погибших эмбрионов. Скорлупу дезинфицируют спиртом и настойкой йода и срезают ножницами по границе пуги. Разрезают скорлуповую и хориоал- лантоисную оболочки и стерильной пастеровской пипеткой отсасывают в пробирку аллантоисную жидкость; Содержимое яйца выливают в чашку Петри и изучают изменения. Чаще их обнаруживают в оболочках эмбриона. Вирусы оспы кур и голубей, болезни Ауески и другие вызывают образование в хориоаллантоисной оболочке < 4> спалительных очагов округлой формы различных размеров. При заражении вирусов болезни Ньюкасла отмечают кровоизлияния в теле эмбриона.
Культивирование клеток куриных фибробластов (КФ) и техника их заражения. При диагностике вирусных болезней и для производства вакцин и диагностикумов* используют различные культуры клеток, в частности однослойные первичные культуры. Их получают из органов и тканей животных и выращивают в питательных
4 -1059
средах на внутренней поверхности стеклянных флаконов (матрасов) или пробирок. Заражение вирусом этих клеток обуславливают его размножение и разрушение клеток— цитопатогенное действие (ЦПД).
Культура фибробластов куриного эмбриона чувствительна ко многим вирусам (болезни Ауэски, чумы плотоядных, болезни Ньюкасла, ларинготрахеита птиц и др. )> поэтому она широко применяется в вирусологии. Ее готовят на основе выпускаемого отечественной промышленностью сухого ферментативного гидролизата мыхуц (ФГМС).
Для приготовления культуры КФ берут 9—10-дневный куриный эмбрион, тупой его конец протирают спиртовым тампоном и прожигают. Верхнюю часть скорлупы по окружности вскрывают ножницами и пинцетом извлекают эмбрион на чашки Петри. Голову и лапки удаляют, а тушку переносят в мерный стаканчик (или банку из-под майонеза), разрезают ножницами на кусочки 2—3 мм величиной, промывают дважды раствором Хенкса (в соотношении 1: 20), встряхивая при этом содержимое. После осаждения ткани надосадочную жидкость сливают. Ткань заливают в соотношении 1: 10 подогретым до 35°С раствором трипсина и переливают в коническую колбу. Туда же опускают простерилизо- ванный кипячением цилиндрический магнитик, входящий в комплект магнитной мешалки. Колбу ставят на магнитную мешалку и 25—30 мин перемешивают содержимое с такой скоростью, чтобы на поверхности жидкости образовывалось воронкообразное углубление. Полученную клеточную взвесь, состоящую к этому времени из одиночных клеток, фильтруют через два слоя марли $ разводят в 2 раза свежеприготовленной ростовой средой, состоящей из 0, 25%-ного ФГМС на растворе Эрла (90%) и сыворотки крови крупного рогатого скота (10%).
Для определения концентрации клеток берут 1 mJi взвеси, тщательно перемешивают и одну каплю вносят под притертое стекло камеры Горяева. Расчет производят
, а • 1000
по формуле х = ———, где х — искомое число клеток в
1 мл суспензии; а — число клеток, подсчитанных во всей решетке камеры; 1000 — число мм3 в 1 мл; 0, 9 — объем счетной камеры в мм3.
В соответствии с расчетом суспензию разводят ростовой средой до концентрации 700—800 тыс. клеток в 1 мл и высевают по 1 мл в пробирки, плотно закрывая их резиновыми пробками (рис. 16). Пробирки размещают на лотках в слегка наклонном положении (под углом 5—7°С) и ставят в термостат при 37°С. Через 24—48 ч в пробирках формируется плотный слой, состоящий из прозрачных фибробластоподобных клеток (монослой, т. е. слой в одну клетку толщиной). Такие культуры КФ готовы для использования в вирусологических целях^
Заражают культуры КФ суспензией органов исследуемого животного (или вирусом), которую готовят путем растирания кусочков органов в фарфоровой ступке до П/олучения пастообразной массы. Ее заливают раствором Хенкса (1: 10), тщательно перемешивают, добавляют пенициллин и стрептомицин каждого по 1000 ЕД на 1 мл.
Из подготовленных пробирок с культурами клеток сливают ростовую среду, вносят в них по 1 мл тканевой суспензии. Чтобы вирус адсорбировался на клетках, пробирки ставят в термостат на 30 мин. Затем исследуемый материал сливают, культуры в пробирках споласкивают раствором Хенкса в объеме 1 мл, затем заливают таким же объемом свежей ростовой среды и вновь помещают в термостат.
Просмотр культур (под микроскопом) производят через каждые 24 ч, сравнивая с контрольными незара- женными культурами. По мере необходимости меняют питательную среду на свежую. ЦПД проявляется, в зависимости от вида вируса, на 1—3 сут, иногда и б более поздние сроки.
Контрольные вопросы к разделу «Основы микробиологии».
1. В чем состоят меры личной профилактики при работе с патологическим материалом, культурами микроорганизмов и животными, больными инфекционными болезнями? 2. Перечислите инфекционные болезни, которыми человек может заразиться от животных. 3. Расскажите устройство микроскопа и правила работы с ним. 4. Как приготовить и окрасить мазки из патологического материала, из культуры микроорганизмов? 5. Какие вы знаете питательные среды, способы их приготовления? 6. Расскажите о технике посевов и пересевов микроорганизмов, получении чистых культур. 7. В чем отличие культивирования вирусов от бактерий?
Раздел второй
Основы общей эпизоотологии
Занятие 10. ПОСТАНОВКА РЕАКЦИИ ПРЕЦИПИТАЦИИ
Задание. 1. Приготовить экстракт (преципитинаген) горячим способом.
2. Профильтровать приготовленный экстракт и пре- ципитирующую сыворотку.
3. Поставить реакцию преципитации методом наслаивания и подслаивания.
Основное оборудование и материалы. Кусочки кожи (от незаразного трупа). Физраствор в колбах, мерные пипетки по 1 мл, пастеровские пипетки, сибиреязвенная преципитирующая и нормальная (лошадиная) сыворотки, асбестовая вата, бактериологические пробирки, маленькие воронки, преципитационные пробирки, штативы, сибиреязвенный антиген для контроля, спиртовые или газовые горелки, водяные бани, фарфоровые ступки с пестиками, стерильный песок.
Место занятия. Лаборатория техникума (при наличии в районе кожевенного завода можно провести занятия в лаборатории Асколи).
Методика проведения занятия. Преподаватель кратко излагает сущность реакции преципитации и цель ее применения, объясняет и показывает технику постановки реакции.
Каждый учащийся самостоятельно готовит преципитиноген п^тем кипячения кусочков кожи, фильтрует полученный экстракт и прец'ипи- тирующую сыворотку, ставит реакцию преципитации методом наслаивания и подслаивания с приготовленным экстрактом, а также контроль реакции, описывает и зарисовывает ход и результаты исследования.
Реакция преципитации основана на взаимодействии двух прозрачных жидкостей, одна из которых содержит антиген (преципитиноген), другая — антитело (преци- питин). При наличии двух специфических компонентов происходит их соединение и на границе жидкостей образуется преципитат в виде беловатого диска (кольца).
В ветеринарной практике реакцию преципитации ставят при исследовании материала на сибирскую язву (кожи, шерсть, паренхиматозные органы, последние особенно в стадии загнивания). Реакцию можно ставить горячим или холодным способами. Разница между ними состоит в приготовлении антигена. Все компоненты, входящие в реакцию, должны быть совершенно прозрачны. В связи с этим необходима фильтрация антигена и сыворотки.
Присланные на исследование пробы патологического материала перед постановкой реакции стерилизуют в автоклаве.
Приготовление компонентов. Для приготовления преципитиногена присланный кусочек кожи измельчают; 1 г измельченной кожи кипятят в 10 мл физраствора (в пробирке) 30—40 мин в водяной бане (горячий способ) или растирают в ступке с песком, заливают 0, 3%-ным карболизированным физраствором в отношении 1: 10 и настаивают 16—18 ч при комнатной температуре (холодный способ). После этого экстракты фильтруют до полной прозрачности через асбестовую вату.
Преципитирующую сибиреязвенную сыворотку готовят на биофабриках. Непосредственно перед постановкой реакции ее следует профильтровать.
Постановка реакции. Реакцию преципитации ставят методом наслаивания или подслаивания. Для постановки реакции используют чисто вымытые, прозрачные сухие преципитационные пробирки (улленгутовские) размером: длина 5—7 см, диаметр 0, 5—0, 6 см.
Мерной пипеткой, а при массовых исследованиях — пипеткой Флоринского (см. занятие 11), наливают в пробирки по 0, 2—0, 3 мл преципитирующей сибиреязвенной сыворотки. После этого пастеровской пипеткой осторож- нр по стенке наслаивают на сыворотку испытуемый экстракт в таком же количестве, как и сыворотку. Затем пробирку ставят в штатив. При использовании метода подслаивания в пробирку наливают 0, 2—0, 3 мл используемого экстракта, после этого пастеровской пипеткой осторожно (опустив ее на дно пробирки) подслаивают преципитирующую сыворотку в таком же количестве.
Реакцию оценивают путем просмотра пробирок на темном фоне при проходящем свете. Реакция считается положительной, если в течение первых 15 мин с момента постановки реакции на границе соприкосновения жидкостей образуется серовато-белый диск (кольцо). Положительную реакцию (ясно выраженное кольцо) отмечают знаком 4-; сомнительную реакцию (нерезкое кольцо) знаком ±; отрицательную реакцию (отсутствие кольца) знаком— (минус).
Непосредственно перед постановкой реакции необходимо проверить ее компоненты. Для этого ставят конт- роли:
1) сибиреязвенный антиген+ преципитирующая сибиреязвенная сыворотка — реакция должна быть положительной;
2) сибиреязвенный антиген + нормальная сыворотка лошади — реакция должна быть отрицательной;
3) физраствор + преципитирующая сибиреязвенная сыворотка — реакция должна быть отрицательной.
В настоящее время применяют также реакцию преципитации в агаровом геле (см. занятие 32).
и
Занятие 11. ПОСТАНОВКА РЕАКЦИИ АГГЛЮТИНАЦИИ
Задание. 1. Поставить реакцию агглютинации (РА) с бруцеллезным антигеном (пробирочным способом) и пластинчатую РА с роз бенгал антигеном (РБП).
2. Изучить способы оценки реакции.
Основное оборудование и материалы. Штативы с агглютинацион- ными пробирками, мерные пипетки объемом 1 и 10 мл, микропипетки объемом 0, 1 мл, специальные шприцы-полуавтоматы, пастеровские пипетки, 0, 5%-ный фенолизированный физраствор, единый бруцеллезный антиген для РА, РСК и РДСК, антиген бруцеллезный цветной для роз бенгал пробы, сыворотки крови для исследования, положительная бруцеллезная и отрицательная сыворотки для контроля, лабораторная аппаратура Флоринского, ванночки, сливные чашки, металлические эмалированные пластинки или израсцовые плитки, карандаши по стеклу, стеклянные палочки, спиртовые или газовые горелки.
Набор пробирок для оценки РА в крестах (реакция на +, + Ht, + +-К + + + + и отрицательная). Указанный набор готовит преподаватель заранее.
Место занятия. Лаборатория техникума, ветеринарная лаборатория (серологический отдел).
Методика проведения занятия. Преподаватель излагает сущность реакции агглютинации, указывает для диагностики каких инфе# ционных болезней она применяется в ветеринарной практике, демонстрирует технику постановки реакции (классическим пробирочным и пластинчатым способами), розлив сыворотки двумя способами (путем последовательного 'разведения и микропипеткой), в т. ч. с помощью лабораторной аппаратуры Флоринского.
Перед постановкой пластинчатой реакции роз бенгал антиген выдерживают 30—40 мин при комнатной температуре и затем тщательно встряхивают. Чтобы показать учащимся положительную реакцию, нужно к нескольким испытуемым пробам сыворотки добавить положительную бруцеллезную сыворотку (1—2 капли на пробирку).
Учащихся разбивают на группы по три человека, они самостоятельно разливают сыворотку, добавляют антиген, ставят контроли реакции. Штативы с пробирками помещают в термостат, учет реакции и демонстрация ее учащимся производится на следующие сутки.
Преподаватель объясняет методы оценки реакции агглютинации. Для этого он использует приготовленный штатив с пробирками, где имеются различные реакции на +, + +, + + +, + + + +, а также отрицательная реакция. Учет РБП проводят непосредственно в ходе занятий.
Пластинчатую реакцию агглютинации с бруцеллезным роз бенгал антигеном применяют при исследовании сыворотки крови у крупного рогатого скота, овец, коз, лошадей, свиней, верблюдов, северных оленей. Ее преимущества перед классической реакцией агглютинации состоят в простоте и быстроте выполнения. Дл^юстановки реак^ ции пригодны прозрачные сыворотки, без эритроцитов? Бруцеллезный антиген для пластинчатой РА — это взвесь в буферном растворе клеток Br. abortus штамма № 19, инактивированных нагреванием и фенолом и окрашенных бенгальской розовой в малиново-розовый цвет. При отсутствии этого антигена можно использовать для занятий обычный бруцеллезный антиген для РА и РСК (РДСК).
Ставят реакцию на чистых металлических эмалированных пластинках или израсцовых плитках с лунками при температуре 18—30° С. На бортиках пластинки против каждой лунки записывают номер испытуемой сыворотки. В начале работы ставят контроль антигена с негативной и позитивной агглютинирующими сыворотками в тех же дозах, а также контроль на спонтанную агглютинацию (к 0, 03 мл антигена добавляют 0, 03 мл физраствора).
Исследуемые сыворотки крови в дозе 0, 03 мл вносят на дно лунки при помощи специального шприца-полуав- томата или микропипетки. При исследовании сыворотки крупного рогатого скота, лошадей, верблюдов и свиней в каждую лунку рядом с сывороткой вносят пипеткой 0, 03 мл (две капли) антигена, а при исследовании сыворотки крови овец, коз и северных оленей — 0, 015 мл (одну каплю). Затем антиген тщательно смешивают с каждой каплей сыворотки активными движениями до получения однородной смеси, распределяя ее при этом по всей поверхности лунок. Пластину покачивают 4 мин, затем учитывают реакцию, слегка наклонив пластину. Агглютинацию, которая происходит позже, не учитывают.
Реакцию считают положительной при наличии выраженной агглютинации окрашенных бруцелл антигена в виде хлопьев розового цвета на белом фоне лункт Если смесь остается гомогенной (агглютинация отсутствует) — реакцию считают отрицательной.
| Сомнительная |
| Отрицательная |
| Сомнительная Отрицательная |
| Отрицательная Не исследуется |
Все сыворотки, с которыми получена положительная РБП в тот же или на другой день исследуют в РА и РСК (РДСК). Оценку «сомнительная» дают только при положительной РБП и отрицательных РА и РСК. Во всех остальных случаях результаты оценивают как положительные (табл. 3).
|
|
|