|
Период полувыведения. Периодом полувыведения называется время, необходимое для очищения плазмы крови от лекарственного вещества на 50%.
|
|
|
|
ПЕРИОД ПОЛУВЫВЕДЕНИЯ
Периодом полувыведения называется время, необходимое для очищения плазмы крови от лекарственного вещества на 50%.
От периода полувыведения также зависит время, необходимое для достижения состояния устойчивой концентрации лекарства. Время, необходимое для достижения устойчивой концентрации лекарственного вещества, как правило, равняется пяти периодам полувыведения (но не пяти интервалам между приемами лекарства). Суть в том, что за каждый период полувыведения концентрация лекарства в организме больного снижается на 50% от того уровня, который был достигнут данной дозировкой. Таким образом, за один период полувыведения в организме больного накапливается только 50% той концентрации лекарства, которой требуется достигнуть. За два периода полувыведения уровень концентрации препарата составит в сумме 75% (50% от последней дозировки плюс половина от тех 50%, что остались с предыдущего периода). За три периода полувыведения достигнутая у больного концентрация состоит из 50% полученной концентрации за последний период, 25% — от предыдущего периода и половины от 25% полученного в начальный период. Это в сумме составляет 87, 5% требуемой концентрации. По достижении 97%, что происходит в течение пяти периодов полувыведения, у больного, по сути, формируется состояние устойчивой концентрации лекарства. Таким образом, мы объяснили, чем определяется время, необходимое для получения устойчивой концентрации лекарственного препарата.
Состояние устойчивой концентрации
Состояние устойчивой концентрации (Ку) предполагает, что концентрация лекарственного вещества в плазме крови будет неизменной до тех пор, пока не будет меняться уровень дозировки препарата (т. е. доза и интервалы между приемами) или не изменится уровень метаболизма и/или выведения под воздействием дополнительных факторов. Уровень дозировки обычно исчисляют количеством лекарственного вещества, принимаемого за 24 ч. По достижении состояния устойчивости концентрация лекарственного вещества в различных частях тела (например, в жировой ткани, в мозговом веществе) становится равновесной. В этом случае количество вещества, выводимого из организма каждые 24 ч, равно количеству вещества, принимаемого каждые 24 ч. Это остается неизменным до тех пор, пока сложившийся режим не будет нарушен в связи с изменениями в течении болезни, в привычках самого больного и его отношении к лечению или в связи с новыми планами лечащего врача.
|
|
|
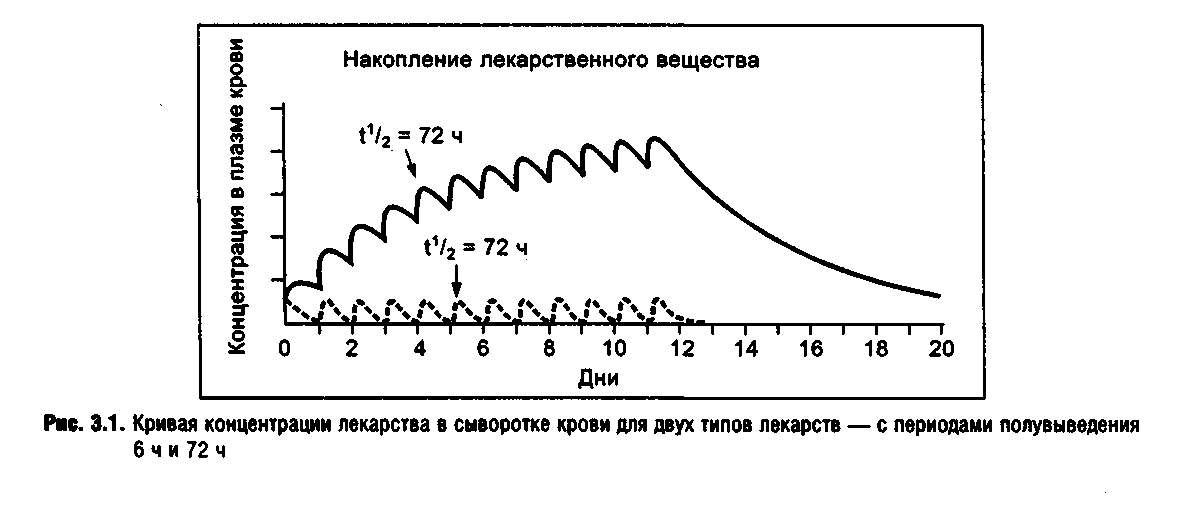
Другое общее правило гласит, что чем более продолжительным является период полувыведения лекарственного вещества, тем больше времени требуется от момента начала приема до обнаружения полного клинического эффекта, положительного или в виде осложнения. На рис. 3. 1 представлены две различные кривые, характерные для лекарств с периодом полувыведения в 72 ч и 6 ч. В тех случаях, когда назначения принимаются однократно в течение дня, как, например, седативно-снотворные средства перед сном, интенсивность накопления в биологических тканях лекарств с такими разными периодами полувыведения будет значительно отличаться. Так, в процессе приема лекарства с периодом полувыведения в 72 ч разница между остаточной концентрацией одного приема и пиком концентрации следующего приема лекарства весьма невелика. А при 6-часовом периоде полувыведения остаточная концентрация лекарства перед следующим приемом будет низкой по сравнению с пиковой концентрацией.
От продолжительности периода полувыведения зависит время, необходимое для оценки клинической реакции, а также время полного выведения лекарства из организма. Например, флуразепам, седативно-снотворный препарат бензодиазепинового ряда, достигает состояния устойчивой концентрации спустя несколько недель после начала приема [8-10]. Таким образом, снижение функций познавательной сферы больного проявится через 2-3 недели после начала приема седативного препарата с ежедневным однократным приемом в вечернее время. И наоборот, если больная забеременела во время состояния устойчивой концентрации, то для исключения тератогенного действия лекарства потребуется аналогичное время после прекращения лечения.
|
|
|
|
|
КИНЕТИКА ПЕРВОГО И НУЛЕВОГО ПОРЯДКА
Кинетикой нулевого порядка называется выведение фиксированного количества препарата в
единицу времени на фоне насыщения ферментной системы, отвечающей за биотрансформацию и выведение лекарств [5, 6]. Алкоголь является классическим примером подобного процесса, когда увеличение его поступления приводит к резкому повышению концентрации в крови. Объясняется это тем, что системы, отвечающие за выведение алкоголя из организма, на определенном этапе становятся полностью задей-ствоваными и до поступления следующей дозы вещества может быть выведена только определенная, фиксированная часть от общего количества. Кинетика первого порядка означает, что выведение вещества из организма за единицу времени прямо пропорционально его введению. Таким образом, здесь существует линейная зависимость (1: 1) между изменением дозировки препарата и его концентрацией в сыворотке крови. В отличие от этого при кинетике нулевого порядка в связи с перенасыщением системы выведения увеличение концентрации происходит более интенсивно, чем при кинетике первого порядка. Примером этому является то, что у 1/3 больных, получающих назначения в виде трициклических антидепрессантов (ТЦА), по достижении концентрации препарата в 200 нг/мл начинает проявляться кинетика нулевого порядка [11, 12]. Поэтому в связи с перенасыщением ферментной системы у таких больных кривая показателей концентрации лекарственного вещества становится в своих верхних отделах более крутой.
|
|
|
Некоторые лекарственные препараты и вещества даже при концентрации в крови выше обычного имеют кинетику нулевого порядка. Но большая часть психотропных препаратов проявляет нелинейную фармакокинетику (явление, занимающее место между кинетикой чисто первого порядка и кинетикой чисто нулевого порядка, когда при превышении клинически приемлемых дозировок препарата появляется тенденция непропорционального увеличения его концентрации). В основе этого феномена лежит механизм последовательной активации разных по структуре и свойствам ферментов, входящих в состав цитохром Р450 (см. разд. " Лекарственное взаимодействие" ), каждый из которых управляет процессом биотрансформации лекарственных веществ при разных концентрациях препарата в крови. При низких концентрациях процесс биотрансформации регулируется теми ферментами, которые имеют высокое химическое сродство, но низкую пропускную способность. Поэтому при нарастании концентрации лекарство быстро перенасыщает эту ферментную систему и происходит резкий непропорциональный рост концентрации в связи с нарастанием дозировки до тех пор, пока не достигает уровня, при котором задействуется в процесс биотрансформации фермент с меньшим структурным сродством, но большей пропускной способностью (примером может служить кинетика флуоксетина, пароксетина, нефазодона) [13-15].
|
|
|