 |
Особенности предоперационного обследования и анестезиологического обеспечения пациентов с заболеваниями сердечно-сосудистой системы
|
|
|
|
Терапия
— Переход на ручную вентиляцию чистым кислородом, поиск утечки в контуре, верификация положения интубационной трубки, аускультация легких и т. д.
— Санация трахеобронхиального дерева.
— Проверка FiO2 кислородным анализатором.
— Терапия шока, если наблюдается нарушение перфузии тканей.
КЛАССИФИКАЦИЯ ЗАБОЛЕВАНИЙ ЛЕГКИХ
Для анестезиолога принципиально важно разделение заболеваний легких на обструктивные, связанные с нарушением пассажа воздуха через трахеобронхиальное дерево, и рестриктивные, т. е. связанные с поражением легочной паренхимы.
Рестриктивные заболевания
Рестриктивные заболевания легких связаны с нарушением податливости (растяжимости) легочной ткани и могут быть хроническими и транзиторными (проходящими). Сопротивление дыхательных путей обычно нормальное, тогда как легочные объемы в той или иной степени снижены. При изучении легочной механики обращает внимание снижение легочного комплайенса.
Транзиторные заболевания
Заболевания, связанные с поражением легочной паренхимы: пневмонии, в том числе аспирационная пневмония, — чаще всего результат рвоты или регургитации во время вводного наркоза (синдром Мендельсона). Общая анестезия вызывает угнетение всех условных и безусловных рефлексов, в том числе рефлексов со слизистой трахеи и бронхов, и таким образом создает условия для попадания в них желудочного содержимого. Данный процесс может происходить на фоне самостоятельного дыхания в результате аспирации рвотных масс (аспирация) или же в результате пассивного затекания желудочного содержимого в трахею у пациента, оперируемого в условиях тотальной миоплегии (регургитация).
|
|
|
И в том и в другом случае могут возникнуть бронхоспазм, ателектазирование, гипоксемия. Выраженность симптомов зависит от объема аспирационных масс и их рН. При попадании в трахею более 0, 4 мл/кг аспирационных масс с рН менее 2, 5 развивается состояние, описанное в литературе как синдром Мендельсона. Последний характеризуется химическим ожогом слизистой трахеи и бронхов с развитием трахеобронхита, микро- и макроателектазированием с развитием пневмонии и/или респираторного дистресс-синдрома. Смертность при синдроме Мендельсона очень высока и зависит от своевременности лечебных мероприятий.
Предрасполагающими факторами к аспирации/регургитации являются:
— замедленная эвакуация из желудка или двенадцатиперстной кишки;
— беременность;
— ожирение;
— регургитация в анамнезе.
Для профилактики аспирации и регургитации необходимо:
— тщательно готовить пациента к плановой операции (легкий ужин накануне, запрет на прием воды и пищи в день операции; пациент может быть взят на плановую операцию не ранее чем через 6 ч после приема пищи; если есть основания предполагать замедленную эвакуацию из желудка, необходимо опорожнение желудка через толстый зонд);
— промывание желудка перед экстренной операцией;
— проводить вводный наркоз и ишубацию пациента в положении с опущенным головным концом, если есть основание предполагать наличие содержимого в желудке;
— использовать прием Селика (давление рукой на перстневидный хрящ в момент интубации);
— следить за тем, чтобы манжетка интубационной трубки полностью перекрывала просвет трахеи;
— использовать желудочный зонд при любых операциях на органах брюшной полости, проводимых в условиях общей анестезии и ИВЛ;
— использовать желудочный зонд при любых операциях продолжительностью более 3 ч, проводимых в условиях общей анестезии и миоплегии.
|
|
|
При возникновении аспирации/регургигации следует:
— перевести больного в положение Тределенбурга и повернуть ему голову в сторону;
— тщательно санировать ротоглотку с помощью салфеток и отсоса, после чего обязательно интубировать;
— провести бронхоскопию, лаваж легких;
— при невозможности проведения санационной бронхоскопии — лаваж до «чистой воды»;
— массивная терапия стероидами;
— антибиотикотерапия — по показаниям, строго обязательна при синдроме Мендельсона или предположении о возможном его развитии;
— терапия возникших осложнений: респираторная терапия при гипоксии, медикаментозная при бронхоспазме и т. д.
Туберкулез, саркаидоз и другие заболевания, связанные с поражением легочной паренхимы, также входят в группу рестриктивных заболеваний легких. При прогрессировании данных заболеваний развивается «легочное сердце» и легочная гипертензия. Вплоть до финальной стадии газовый состав крови может оставаться нормальным.
Респираторный дистресс-синдром взрослых (РДС). Патофизиология заболевания связана с нарушением проницаемости альвеолярной мембраны и увеличением содержания жидкости с высоким содержанием белка в просвете альвеол и интерстиции. Альвеолокапиллярная диффузия газов резко нарушается. РДС — финальная стадия многих системных заболеваний и расстройств, например шока различной этиологии, массивной кровопотери, сепсиса и т. д. Газовый состав крови резко изменен с самого начала заболевания. Требует интенсивной медикаментозной и респираторной терапии, вплоть до проведения ИВЛ.
Четыре основных компонента считаются обязательными при проведении ИВЛ при РДС:
— прессциклическая вентиляция (менее опасна в плане баротравмы легких, которая весьма вероятна при данном страдании). При отсутствии подобной опции у вентилятора используют обычную объемную вентиляцию, но тщательно следят за максимальным давлением на вдохе (не должно превышать 30 см вод. ст. ) и легочньм комплайенсом (см. главу «Мониторинг»).
— нисходящая форма кривой потока в фазу вдоха, что позволяет добиться инспираторного открытия спавшихся альвеол;
— инверсное соотношение вдох/выдох, вплоть до 4: 1, — продлевает время активного транскапиллярного обмена газов;
|
|
|
— создание «переходящего» PEEP (positive end expired pressure — положительное давление в конце выдоха) позволяет поддерживать легкие как бы «подраздутыми», что, в свою очередь, помогает бороться с гиповентиляцией и препятствует образованию микро- и макроателектазов, последнее весьма характерно для развития РДС. В данном случае, по мнению большинства исследователей, PEEP, создаваемый при объемной вентиляции, менее эффективен, хотя данный факт, насколыхо известно, никем не был доказан.
Следует помнить, тем не менее, что в патогенезе РДС существенную роль играют вентиляционно-перфузионные расстройства, возникающие вследствие вентиляции неперфузируемых отделов легких, и наоборот.
При спонтанном дыхании происходит чередование отделов легких, участвующих в газообмене, что позволяет поддерживать ткань легких в активном физиологическом состоянии.
До настоящего времени, к сожалению, не разработано режима ИВЛ (или вспомогательной вентиляции), способного сохранить подобный механизм.
Использование режима CMV+sigh (т. е. подача двойного объема через каждые 50—100 циклов) не решает обсуждаемой проблемы, так же как и использование режимов PEEP или СРАР (continues positive airway pressure — положительное давление в дыхательных путях).
Медикаментозная терапия и профилактика РДС включает обязательное использование стероидов, антибиотиков, диуретиков и т. д. В последние годы не без успеха используются естественные и синтетические сурфактанты.
В принципе, развернутый РДС-синдром — грозное осложнение ряда заболеваний, требующее немедленной интенсивной терапии. Но даже при этих условиях смертность достигает 60— 70%.
Отек легких — интерстициальный или альвеолярный отек, возникающий чаще всего вследствие левожелудочковой недостаточности.
Лечение в первую очередь должно быть направлено на борьбу с острой сердечной недостаточностью, хотя состояние может потребовать перевода на ИВЛ и проведения респираторной терапии (см. главу «Интраоперационное управление гемодинамикой»).
|
|
|
Пневмоторакс
Состояние, развивающееся в результате попадания воздуха в плевральную полость. Оно возникает при:
— спонтанном разрыве шварты или буллы в легком;
— проникающем ранении грудной клетки;
— хирургической операции в соответствующей области;
— как осложнение ряда манипуляций (катетеризации подключичной или внутренней яремной вены, торако-, перикардиоцентезе и т. д. );
— как осложнение вентиляции с высоким давлением на вдохе. Возникающая баротравма и повреждение стенок альвеол могут привести к развитию пневмоторакса.
Клинические проявления пневмоторакса зависят от объема воздуха, попавшего в плевральную полость.
При малых объемах пневмоторакс может никак себя не проявлять. При больших объемах легкое коллабируется, возникает гипоксия.
Особенно опасен напряженный (клапанный) пневмоторакс — ситуация, когда происходит постоянное нагнетание воздуха в плевральную полость без его эвакуации. При этом происходит смещение средостения со сдавлением сердца и магистральных сосудов.
Диагноз ставится на основании аускультации (ослабленное дыхание), уменьшения легочного комплайенса, увеличения пикового давления на вдохе, гипоксии. Верификация — при рентгенографии легких.
Лечение
Заключается в немедленной эвакуации пневмоторакса. Пункция производится во 2—3 межреберье по среднеключичной линии.
Независимо от причин у лиц, находящихся на ИВЛ или которым предполагается выполнение операции в условиях общей анестезии, устанавливается пассивный дренаж.
Хронические заболевания:
— плевриты («сухие» и экссудативные). Следует помнить, что подавляющее большинство плевритов имеет туберкулезную этиологию;
— различные врожденные или прибретенные деформации грудной стенки;
— высокое стояние диафрагмы, которое может быть следствием ожирения, асцита, беременности и т. д.
При рестриктивных заболеваниях гипоксия первична, а нарушения вентиляционно-перфузионных соотношений возникают позднее.
Обструктивные заболевания
К обструктивньм заболеваниям относятся те, которые вызывают увеличение сопротивления в дыхательных путях:
— прежде всего, по тяжести состояния и возможным неблагоприятным последствиям следует говорить о бронхиальной астме — заболевании, связанном с затрудненным выдохом вследствие экспираторной обструкции бронхов разного калибра. Последнее в свою очередь, связано с комплексом причин, включая гиперпродукцию бронхиального секрета, с повышенной сократимостью мышечного слоя верхних дыхательных путей и их отеком. Наиболее частой этиологической причиной страдания являются инфекционные заболевания легких и аллергия на различные медикаментозные и немедикаментозные вещества. Обязательна постановка аллергических проб на все препараты, которые предполагается использовать во время анестезии. Учитывая, что из всех анестезиологических препаратов наиболее выраженным бронходилатирующим действием обладает фторотан, имеет смысл продумать возможность его использования для вводного наркоза и/или для поддержания анестезии. По возможности следует избегать использования пропанидида (эпонтол, сомбревин — выраженный аллергоген, запрещенный к использованию в ряде зарубежных стран), гексенала и тиопентала Na (наличие сульфогидрильных групп может спровоцировать развитие аллергии), в меньшей степени наркотических аналгетиков;
|
|
|
— хронический бронхит приводит к гиперпродукции бронхиального секрета и сужению просвета бронхов и бронхиол или даже их обструкции. Наиболее распространенная причина хронического бронхита — курение. У пациентов данной группы относительно рано выявляются гипоксия и гиперкапния. «Легочное сердце» развивается на поздних стадиях заболевания как закономерный финал легочной гипертензии и правожелудочковой недостаточности;
— эмфизема легких — финал ряда заболеваний легких, выражающаяся в уменьшении эластичности альвеол и иных легочных структур. Это, в свою очередь, приводит к преждевременному закрытию (коллапсу) воздухоносных путей при большем, чем в норме, остаточном легочном объеме. Компенсация достигается за счет увеличения минутной вентиляции (МОД). Гипоксия и гиперкапния появляются на поздних стадиях заболевания;
— констриктивный фиброз — заболевание, связанное с гиперпродукцией бронхиального секрета повышенной вязкости, содержащего большое количество сахаров. Это приводит к обструкции дыхательных путей и их фиброзу. Больные данной группы предрасположены к развитию инфекционных заболеваний легких. Позднее появляются брохоэктазы и признаки дыхательной недостаточности.
Основной причиной гипоксии при обструктивных заболеваниях легких является нарушение вентиляционно-перфузионных соотношений.
Нарушение дыхания возникает вторично, вследствие увеличенной работы дыхания по преодолению повышенного сопротивления в дыхательных путях.
Нередко больные имеют признаки как обструктивного, так и рестриктивного заболевания.
Задача анестезиолога на пооперационном этапе — выявить этиологию страдания, понять его ведущий компонент и назначить соответствующую терапию с целью добиться максимально возможного уровня компенсации.
ОБЩИЙ ОСМОТР И СБОР АНАМНЕЗА
При сборе анамнеза выясняют наличие у больного хронических легочных заболеваний (пневмония, туберкулез и т. д. ), а также социальные и профессиональные факторы, способствующие их появлению: профессиональная вредность (работа в загазованном, запыленном помещении, работа с асбестом, цементом и т. д. ), курение.
Обращают внимание на кашель (возможно, бронхит — необходимо углубленное исследование), нарушение дыхания.
Физикальный осмотр
При осмотре больного фиксируют внимание на:
— цианозе, который может быть проявлением целого ряда расстройств: снижения уровня транспорта кислорода, ухудшения микроциркуляции и перфузии тканей, резкого увеличения потребления кислорода тканями, снижения уровня НЬ;
— ожирении, беременности и искривлении позвоночника (указанные состояния приводят к снижению жизненной емкости и податливости легких и вызывают предрасположенность к ателектазированию и гипоксии);
— кахексии, которая в силу ряда причин (слабость мускулатуры, в том числе и дыхательной, гипопротеинемия, нарушения иммунного статуса) вызывает предрасположенность к пневмонии.
При осмотре грудной клетки отмечают выраженные экспираторные усилия, что может указывать на наличие обструктивного заболевания легких; участие вспомогательных мышц (межреберных, грудино-ключично-сосцевидной и т. д. ); асимметричное движение грудной клетки при дыхании, что наблюдается при плеврите, пневмо-, гидро- и гемотораксе, поражении левой или правой ветви диафрагмального нерва.
При аускультации фиксируют тип дыхания (везикулярное, жесткое и т. д. ), наличие патологических шумов и хрипов. При аускультации сердца следует иметь в виду, что акцент второго тона над легочной артерией может свидетельствовать о наличии легочной гипертензии, развившейся вследствие хронического обструктивного заболевания легких.
Лабораторные и инструментальные исследования
Рентгенологическое исследование легких (рентгенография, томография и компьютерная томография) остается наиболее информативным методом диагностики заболеваний системы дыхания. Из прочих следует назвать:
— исследование газового состава артериальной крови. Снижение РаО2 ниже 60 мм Hg при вдыхании атмосферного воздуха свидетельствует о наличии гипоксии и повышенном риске развития интра- и послеоперационных осложнений со стороны системы дыхания. Увеличение РаСО2 выше 45 мм Hg в покое свидетельствует о финальной стадии легочного заболевания и об отсутствии у пациентов какого бы то ни было резерва системы дыхания. Риск развития легочных осложнений крайне высок. Имеет смысл исследовать газовый состав именно артериальной крови, в ряде случаев — смешанной венозной крови (см. главу «Мониторинг»). Исследовать газовый состав капиллярной крови («из пальца») не имеет смысла, так как слишком много факторов может привести к одним и тем же изменениям.
Помимо истинной гипоксии это могут быть:
— нарушения микроциркуляции вследствие шока, гиповолемии и т. д.;
— нарушения регионарной гемодинамики вследствие вынужденного положения руки, сосудистой патологии и т. п.;
— уровень рН, который изменяется параллельно с РаСО2, может свидетельствовать о респираторном ацидозе или алкалозе;
— функциональное исследование легких с определением объемных и скоростных показателей — ценный дополнительный метод диагностики обструктивных и рестриктивных заболеваний, что более важно, данный тест позволяет оценить эффект предоперационной терапии и резервные возможности системы дыхания;
— электрокардиография, которая позволяет диагностировать легочную гипертензию. ЭКГ-признаками легочной гипертензии являются: смещение электрической оси сердца вправо, легочный зубец Р (высота Р более 2, 5 мм), гипертрофия правых отделов сердца, блокада правой ножки пучка Гиса.
ПРЕДОПЕРАЦИОННОЕ ЛЕЧЕНИЕ ЗАБОЛЕВАНИЙ СИСТЕМЫ ДЫХАНИЯ
Цель предоперационного лечения — добиться максимально возможного эффекта в лечении заболеваний легких и таким образом уменьшить риск развития интра- и послеоперационных осложнений со стороны системы дыхания.
За две недели (в крайнем случае за 24—48 ч) до операции больному запрещают курить. Это позволяет уменьшить содержание карбоксигемоглобина в крови больных и вызывает смещение кривой диссоциации оксигемоглобина вправо. Отказ от курения за 2—4 недели до операции позволяет надеяться на восстановление нормальной функции эндотелия бронхов.
Необходимо провести адекватную терапию выявленного инфекционного заболевания легких. Операция по возможности откладывается до полного выздоровления пациента. При наличии гидро- и гемоторакса производят пункцию с аспирацией содержимого до вводного наркоза. При наличии пневмоторакса производят дренирование плевральной полости. Пассивный дренаж (например, по Бюлау) оставляют на все время проведения ИВЛ, в противном случае высока вероятность развития напряженного пневмоторакса.
Предоперационная физиотерапия, как правило, позволяет в той или иной степени улучшить состояние больных хроническими легочными заболеваниями и, следовательно, уменьшить риск развития послеоперационных осложнений со стороны системы дыхания.
При гигантских грыжах делают пробу со стягиванием, что позволяет в дооперационном периоде прогнозировать вероятность развития острой дыхательной недостаточности после операции.
Если в результате пробы выявлено значительное снижение объемных показателей, дается рекомендация хирургам проводить пластику передней брюшной стенки методами, не приводящими к уменьшению объема брюшной полости (использование синтетических материалов («сетка»), твердой мозговой оболочки и т. д. ).
ОСОБЕННОСТИ ПРЕДОПЕРАЦИОННОЙ ПОДГОТОВКИ БОЛЬНЫХ ХРОНИЧЕСКИМИ ЗАБОЛЕВАНИЯМИ ЛЕГКИХ (ХЗЛ)
Как правило, больные ХЗЛ получают плановую медикаментозную терапию:
— симпатомиметики или В-агонисты вызывают бронходилатацию вследствие влияния на аденилатциклазу (увеличение содержания цАМФ приводит к расслаблению гладкой мускулатуры бронхов; препараты с неспецифической активностью в отношении В1 и В2-рецепторов: адреналин, изопротеренол и т. д. могут провоцировать развитие аритмий и тахикардии; они с осторожностью должны использоваться у больных с ИБС; время отмены препаратов перед операцией решается индивидуально; прием селективных В2-агонистов (алупент), как правило, продолжают до операции);
— ингибиторы фосфодиэстеразы (эуфиллин) увеличивают содержание цАМФ и обладают бронходилатирующим эффектом (данные препараты показаны больным с ХОЗЛ, бронхиальной астмой; лечение тщательно подобранной дозой препарата продолжается до дня операции; обычная доза — 300—1500 мг/сут.; эуфиллин стандартно назначается курильщикам за 7 дней до операции);
— кортикостероиды назначаются больным ХОЗЛ, нечувствительным к действию В-агонистов и ингибиторов фосфодиэстеразы; при их назначении рассчитывают на угнетение отечности эпителия бронхов и снижение их секреции, стабилизацию плазматической мембраны клеток и уменьшение секреции гистамина; тщательно подобранная терапия продолжается до операции;
— парасимпатолитики (атропин) обладают прямым бронходилатирующим эффектом вследствие угнетающего влияния на гуанилатциклазу (уменьшение содержания цГМФ); назначаются в виде ингаляций, терапия продолжается до момента операции;
— муколитики снижают и делают менее вязким секрет бронхов; назначаются в виде ингаляций, терапия продолжается до дня операции.
Премедикация
Больные, постоянно получающие В-агонисты или кортикостероиды, имеют при себе ингалятор до начала вводного наркоза.
Следует особенно осторожно относиться к назначению бензодиазепинов и наркотических аналгетиков из-за опасности угнетения дыхания с развитием гипоксии.
ВЛИЯНИЕ АНЕСТЕЗИИ И ОПЕРАЦИИ НА ФУНКЦИЮ ЛЕГКИХ
Общая анестезия приводит к уменьшению легочных объемов и изменению вентиляционно-перфузионных соотношений. Как правило, общие анестетики снимают регулирующий эффект гипоксии и гиперкапнии на дыхательный центр. У больных со скомпрометированной системой дыхания высока вероятность развития ателектазов в послеоперационном периоде.
Послеоперационная боль еще более усугубляет расстройства легочной функции, так как ограничивает подвижность грудной клетки и мешает больному откашляться.
Механическая вентиляция (ИВЛ) при сравнении со спонтанным дыханием вызывает изменение вентиляционно-перфузионных соотношений.
Вследствие создания положительного давления на вдохе нескомпрометированные участки легких получают большую порцию газовой или газонаркотической смеси. Кровоток в системе легочной артерии определяется силой тяжести и увеличен в пораженных отделах легких.
Таким образом, ИВЛ вызывает как увеличение физиологического мертвого пространства, так и внутрилегочное шунтирование крови (Qs/Qt, ).
Операция приводит к выраженному изменению (уменьшению) объемных параметров дыхания. Так, операция на верхних отделах брюшной полости приводит к уменьшению ЖЕЛ на 75%, а на органах грудной полости — на 50%. Причем восстановление нормального объема дыхания занимает в лучшем случае неделю.
Операции на конечностях не сопровождаются столь существенными изменениями механики дыхания.
Кроме того, следует учитывать, что в физиологических условиях вдыхаемый воздух подогревается и увлажняется в верхних дыхательных путях. Медицинские газы, особенно кислород, обладают выраженным дегидратирующим влиянием и вызывают резкую «сухость» бронхиального дерева. Данный эффект еще более усугубляется при эндотрахеальном наркозе. Все это приводит к повреждению эпителия бронхов и способствует развитию послеоперационнык бронхитов и пневмоний.
В этой связи принципиально важно пользоваться увлажненной и подогретой газонаркотической смесью, особенно при длительных операциях (в настоящее время имеется возможность использовать сухие увлажнители и теплосберегатели, совмещенные с абактериальным фильтром). Использование увлажнителей снижает частоту развития послеоперационных бронхитов на 27%, а у лиц с хроническим бронхитом позволяет избежать развития пневмоний у 47% случаев.
ОСОБЕННОСТИ АНЕСТЕЗИОЛОГИЧЕСКОГО ПОСОБИЯ
Показана кислородотерапия сразу после поступления в операционную.
Регионарная анестезия является предпочтительной для данной категории больных. Это особенно относится к операциям на конечностях и нижнем этаже брюшной полости.
Общая анестезия показана в торакальной хирургии и при операциях на верхнем этаже брюшной полости. По возможности используют сочетание эпидуральной и общей анестезии в надежде сократить расход наркотических аналгетиков, уменьшить выраженность послеоперационной депрессии дыхания и как можно раньше перевести пациента на самостоятельное дыхание.
Обязательно использование увлажнителей во время операции. В послеоперационном периоде — тщательно подобранная респираторная терапия, ранняя активизация больных и ранняя физиотерапия могут уменьшить количество осложнений со стороны системы дыхания.
Глава 3
ОСОБЕННОСТИ ПРЕДОПЕРАЦИОННОГО ОБСЛЕДОВАНИЯ И АНЕСТЕЗИОЛОГИЧЕСКОГО ОБЕСПЕЧЕНИЯ ПАЦИЕНТОВ С ЗАБОЛЕВАНИЯМИ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ
В. В. Субботин
Осложнения со стороны сердечно-сосудистой системы являются ведущей причиной летальности и возникновения жизнеопасных осложнений во время и после оперативных вмешательств. Учитывая, что по разным показаниям в мире ежегодно оперируются около 1 млн. человек с сопутствующей патологией сердца, несложно представить всю важность обсуждаемой проблемы. В этой связи анестезиологу необходимо знать и понимать, как предупреждать и лечить возможные осложнения.
Среди прочих страданий ишемическая болезнь сердца (ИБС) и инфаркт миокарда (ИМ), как ее закономерный финал, в наибольшей степени опасны в плане прогноза предстоящей операции и анестезии.
ИШЕМИЧЕСКАЯ БОЛЕЗНЬ СЕРДЦА
В этиологии ишемической болезни сердца на первом месте стоит атеросклероз, хотя гипертрофия миокарда при кардиомиопатии и аортальном пороке также могут приводить к ишемическим атакам. ИБС — это всегда несоответствие между транспортом кислорода к миокарду (ТмО2) и его потреблением (MVO2). Следует помнить, что кровоснабжение миокарда осуществляется за счет двух венечных артерий (правой и левой) и их ветвей, отходящих от аорты позади створок аортального клапана сердца. Коронарная перфузия осуществляется в основном за счет антеградного давления крови в фазу диастолы, которое определяется как разность между диастолическим артериальным давлением (АДдиа) и центральным венозным давлением (ЦВД).
Исследования последних лет показали, что коронарная перфузия осуществляется также и в фазу систолы, причем вклад данного механизма в кровоснабжение миокарда кислородом значительно больше, чем было принято думать. Данный феномен частично объясняет, как осуществляется коронарная перфузия у лиц с аортальной недостаточностью IV степени. Тем не менее считается, что коронарный кровоток прямо пропорционален перфузионному давлению и обратно пропорционален коронарному сосудистому сопротивлению. В норме коронарный кровоток у среднестатистического человека (масса тела 70 кг) составляет величину порядка 250 мл/мин и может увеличиваться в 4—5 раз, чтобы компенсировать возросшие потребности миокарда в кислороде, например во время физической нагрузки.
Увеличение частоты сердечных сокращений (ЧСС) приводит к укорочению периода диастолического заполнения и уменьшению коронарного кровотока. Поэтому больные ИБС, как правило, плохо переносят тахикардию. На этом, кстати, основано определение резервных (компенсаторных) возможностей миокарда при проведении пробы с чреспищеводной кардиостимуляцией.
О работе сердца можно судить по двум ключевым параметрам:
— сердечному индексу (СИ), который определяется как частное от деления минутного объема сердца (МОС) на площадь поверхности тела (ГШТ);
— ударному индексу — частное от деления ударного объема (УО) на ППТ.
Производительность сердца определяется:
— величиной преднагрузки. В соответствии с законом Франка — Старлинга, чем больше растянуто сердце в период диастолы, тем выше УО. О величине преднагрузки с известной долей вероятности можно судить по величине давления заклинивания легочных капилляров (ДЗ), которое коррелирует с давлением заполнения левого желудочка (r = 0, 7). В норме ДЗ = 8—10 мм Hg. При невозможности измерить ДЗ допустимо принять ее равной диастолическому давлению в легочной артерии минус 2 мм Hg. Следует учитывать, что часто используемая в клинике для этой цели величина центрального венозного давления (ЦВД) совпадает с величиной давления заполнения левого желудочка только в 30% случаев. Гиповолемия приводит к уменьшению, а гиперволемия — к увеличению преднагрузки. Регулируя емкость венозного звена большого круга кровообращения с помощью, например, нитроглицерина, можно изменять величину преднагрузки;
— величиной постнагрузки, которая зависит от тонуса артериального колена большого круга кровообращения и выражается через величину общего периферического сопротивления (ОПС). Последняя рассчитывается по следующей формуле:
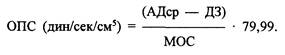
В норме ОПС составляет 1500—1700 (дин/сек/см5). Регулируя ОПС с помощью нитропруссида или допамина (адреналина и т. д. ), можно изменять величину постнагрузки.
— ЧСС;
— сократимостью миокарда (определяется состоянием сердечной мышцы).
Кровь, притекающая к миокарду, имеет насыщение 95—100%, оттекающая — в коронарном синусе — около 30%. Содержание кислорода в артериальной крови определяется количеством гемоглобина (НЬ), его насыщением кислородом (SaO2) и парциальным давлением кислорода (РаО2) или количеством кислорода, растворенного в плазме. Как правило, в клинике последней величиной можно пренебречь. Учитывая, что у больных ИБС уровень Hb, как правило, не изменен, а величина экстракции кислорода и так максимальна, единственньм путем увеличения ТмО2 является увеличение коронарного кровотока.
Потребление кислорода миокардом трудно определить в клинических условиях, однако очевидно, что его величина определяется следующими параметрами:
— систолической работой сердца, которая, в свою очередь, является производной ЧСС, АД и УО;
— сократимостью миокарда. Данный показатель не зависит от пред- и постнагрузки и является производной состояния миокарда. Регулируется симпатической нервной системой. Позитивные инотропные препараты (сердечные гликозиды, допамин и др. ) увеличивают MVO2, тогда как В-адреноблокаторы (пропранолол), блокаторы кальциевых каналов (нифедипин) практически все общие анестетики: в/в (барбитураты, пропофол) и ингаляционные анестетики (изофлюран, десфлюран, севофлюран) уменьшают указанный показатель;
— величиной напряжения (растяжения) стенок желудочков сердца. В соответствии с законом Лапласа, величина растяжения стенки сферы (желудочка) пропорциональна радиусу, таким образом, увеличение объема желудочка приводит к напряжению его стенок и MVO2 возрастает.
Косвенно о величине потребления кислорода миокардом можно судить по разности SpO2 и SvO2. Последнюю величину определяют либо на основании исследования газового состава проб крови, взятой из коронарного синуса, либо на основании мониторинга обсуждаемого показателя с помощью фиброоптического катетера, опять-таки установленного в коронарном синусе.
Принципиально увеличить коронарный кровоток можно следующими путями:
— увеличив перфузионное давление за счет роста системного давления (например, применения а-адреноагонистов);
— увеличив содержание кислорода в артериальной крови (СаО 2 ) с помощью увеличения содержания Hb или его (Hb) насыщения (см. предыдущую главу);
— уменьшив ЧСС с помощью В-адреноблокаторов или наркотических препаратов. Это, в свою очередь, приводит к увеличению диастолы и к возрастанию коронарной перфузии;
— уменьшив конечно-диастолическое давление (КДД) желудочков за счет уменьшения конечно-диастолического объема (КДО), например при использовании нитроглицерина;
— увеличив сократимость, например за счет применения инотропных препаратов (добутамин);
— применив кардиопротекторы, например, показано, что использование неотона (креатин фосфат) повышает УИ. И хотя механизм данного феномена пока неизвестен (по современным представлениям), креатин фосфат не способен проникать через неповрежденную мембрану кардиомиоцита и, следовательно, не должен влиять на метаболизм и сократимость миокарда), клинические и экспериментальные данные убеждают нас в эффективности данного препарата;
— примененив внутриаортальную контрпульсацию, которая увеличивает АДдиа и соответственно коронарный кровоток;
— наконец, при тяжелой левожелудочковой недостаточности может быть предпринята попытка временного протезирования функции левого желудочка за счет обходного шунтирования. При этом миокард работает практически только «на себя».
Пациенты с ИБС, как правило, очень лабильны и требуют очень внимательного отношения и тщательно подобранной предоперационной терапии. Последняя обычно продолжается до момента операции, более того, больные имеют с собой нитраты вплоть до начала вводного наркоза.
Исключением являются:
— длительно действующие В-блокаторы;
— диуретики;
— препараты дигиталиса.
Данные препараты отменяют с таким расчетом, чтобы их действие прекращалось к началу операции.
При выборе метода анестезии следует иметь в виду, что у больных с ИБС риск выполнения операций на грудном отделе аорты, например, в 3—4 раза выше, чем у пациентов, не страдающих ИБС.
Мнение о предпочтительном использовании у данной категории больных регионарных методов анестезии представляется ошибочным. В целом, по-видимому, при грамотно проведенной общей анестезии не больше риска, чем при грамотно проведенном регионарном обезболивании, и наоборот. Вопрос выбора в каждом конкретном случае решается индивидуально и в большей степени зависит от вида и объема предстоящей операции.
ПРИОБРЕТЕННАЯ ПАТОЛОГИЯ КЛАПАНОВ СЕРДЦА
Ревмокардит является наиболее частой причиной поражения клапанного аппарата сердца, однако бактериальный эндокардит, даже после экстракции зуба, может привести к патологическим изменениям клапанов. В этой связи всем больным, оперируемым на клапанном аппарате сердца, рекомендуется профилактическое назначение антибиотиков в пред-, интра- и послеоперационном периоде. Исключение составляют больные с пролапсом митрального клапана без регургигации, пациенты с имплантированным кардиостимулятором или дефибриллятором, профилактическая антибиотикотерапия которым не проводится. Наиболее часто ревмокардит поражает митральный клапан, реже — аортальный и трикуспидальный.
Митральный стеноз
|
|
|


