 |
Экстракорпоральное оплодотворение
|
|
|
|
Экстракорпоральное оплодотворение (ЭКО) — это широко распространенный метод решения проблем бесплодия различной этиологии. В ходе применения этой методики у женщин путем гормональной стимуляции провоцируют рост и созревание сразу нескольких фолликулов, из которых впоследствии извлекаются яйцеклетки. Полученные яйцеклетки помещаются на питательную среду, после чего к ним добавляется суспензия сперматозоидов и происходит оплодотворение (рис. 7.5.1).

Рис. 7.5.1. Схема экстракорпорального оплодотворения
Оплодотворенные яйцеклетки инкубируются до 5 дней на чашках со средой. За это время эмбрионы достигают стадии четырех или восьми бластомеров, после чего их имплантируют в матку, где они продолжают развитие. При этом вынашивать эмбрион может как женщина, ставшая донором яйцеклетки, так и суррогатная мать.
Основными показаниями к процедуре ЭКО являются нарушения функции маточных труб, снижение качества спермы, эндометриоз, необъяснимое бесплодие.
Эффективность лечения определяется различными факторами. Помимо причины бесплодия, большую роль играют возраст женщины и длительность бесплодия.
История ЭКО
Первый человек, зачатый вне тела человека, появился на свет в 1978 году. Предшествовало этому череда открытий, первым из которых стало предположение Левенгука, высказанное еще в 1677 году, о том, что зачатие происходит в результате проникновения сперматозоида в организм женщины.
Спустя более чем 100 лет ученые Хантер выполнил искусственную инсеминацию. Мужчина, страдавший от гипоспадии, не мог в связи с этим иметь детей. Ученый собрал сперму и ввел ее в половые пути женщины. Процедура завершилась наступление беременности.
|
|
|
Лишь в 1827 году впервые было дано описание яйцеклетки и уже в 1891 году была осуществлена первая успешная трансплантация эмбриона, который был перенес от одной самки кролика другой.
В последующие годы были открыты функции гипофиза, исследованы гормоны, который он выделяет. В 1930 году Пинкус впервые применил технологию суррогатного материнства — перенос оплодотворенной яйцеклетки в матку и последующее развитие беременность. В 1934 году О.В. Красовская смогла провести оплодотворение яйцеклетки кролика в лабораторных условиях.
В 1960 в клиническую практику широко вошел метод лапароскопии и уже в 1968 году был предложен метод взятия яйцеклетки. 1975 год стал революционным в истории ЭКО — эмбриолог Эдвардс и гинеколог Степто получили первую беременность. К сожалению, она была внематочной. Однако спустя лишь 3 года на свет появился первый ребенок из пробирки — Луиза Браун.
С появлением в 1979 году УЗИ ситуация изменилась радикально. Теперь яйцеклетку стало возможным получать с помощью пункции, а не лапароскопической операции.
В 1986 году в России родился первый ребенок, оплодотворение которого произошло по технологии ЭКО. В 1989 стало возможной преимплантационная диагностика. С помощью взятия части яйцеклетки стало возможной диагностика генетических нарушений.
В 1994 году появились первые сообщения об успешных ЭКО с помощью метода ИКСИ (введения сперматозоида в яйцеклетку).
Основные этапы ЭКО
Процедуру ЭКО можно разделить на несколько фаз лечения: стимуляция созревания яйцеклеток, забор яйцеклеток (пункция), собственно экстракорпоральное оплодотворение, перенос эмбрионов в полость матки, лечение после переноса.
Стимуляция созревания яйцеклеток. Главное отличие стимулированного цикла в программе ЭКО от естественного заключается в том, что под влиянием гормонов созревает не одна, а несколько яйцеклеток. Затем созревшие яйцеклетки извлекают из яичников, для того, чтобы оплодотворить вне организма. Необходимость получения нескольких яйцеклеток обусловлена фактом, что не каждая яйцеклетка может быть оплодотворена, а также не все эмбрионы имеют одинаковые шансы на имплантацию. Наличие нескольких эмбрионов позволяет выбрать для переноса те из них, у которых вероятность имплантации наилучшая. Чтобы получить максимальное количество зрелых яйцеклеток, но при этом избежать осложнений, гормональная терапия подбирается индивидуально.
|
|
|
Первый шаг лечения направлен на оптимальную подготовку организма к стимуляции гормонами. Проводится регуляция менструального цикла таким образом, чтобы временем овуляции и забора яйцеклеток можно было управлять. Это достигается с помощью медикаментов, которые подавляют продукцию собственных гормонов, стимулирующих работу яичников (ФСГ и ЛГ) – так называемая даунрегуляция. Медикаменты, используемые в фазе даунрегуляции, называются агонистами гонадотропин-рилизинг гормона (агонисты ГнРГ) и воздействуют на ту часть мозга, которая ответственна за выброс гормонов ФСГ и ЛГ. Даунрегуляция используется при проведении длинного протокола стимуляции и назначается с 19 - 22 дня цикла. Препараты могут иметь различные названия и использоваться в виде ежедневных инъекций, назального спрея или депо. Благодаря этой подготовке в дальнейшем улучшается возможность регулировать фазу стимуляции.
При проведении короткого протокола используют антагонисты ГнРГ, которые также применяются для подавления продукции собственных гормонов. Их использование начинается только в фазе стимуляции, т.е. от начала менструации. Благодаря этому общее время лечения уменьшается и снижается риск появления симптомов гипоэстрогении.
Решение о выборе протокола принимает врач в зависимости от исходных данных пациентов.
Для стимуляции созревания яйцеклеток могут быть использованы различные препараты, которые соответствуют естественному гормональному циклу. Они различаются по технологии изготовления.
HMG (человеческий менопаузальный гонадотропин) получают из мочи женщин, находящихся в постменопаузе (климактерическом периоде). HMG содержит в одинаковой мере ФСГ и ЛГ.
|
|
|
Рекомбинантный ФСГ производят с помощью биологических технологий. Это чистый белок, полностью идентичный естественному гормону. Поэтому рекомбинантные препараты часто лучше переносятся пациентами.
В мочевых препаратах чистота и содержание ФСГ может существенно колебаться, а также они чаще вызывают аллергию. Однако вероятность наступления беременности после стимуляции рекомбинантным ФСГ или мочевыми препаратами существенно не различается.
Стимуляция гонадотропинами (ФСГ) начинается, как правило, через 14 дней после начала даунрегуляции (длинный протокол) либо в течение первых трех дней цикла - короткий протокол (1-й день цикла = 1-й день менструации). Лечение гонадотропинами длится в среднем 11 - 13 дней. В течение этого периода, в одно и то же время суток, осуществляются внутрикожные (или внутримышечные) инъекции определенного количества гормона. Если для подавления собственных гормонов используется антагонист ГнРГ, его введение начинается с 5-го – 7-го дня стимуляции. Инъекции можно делать самостоятельно в домашних условиях или в клинике.
Во время стимуляции проводится ультразвуковое наблюдение. Этот мониторинг служит для контроля за количеством и размерами фолликулов, а также толщиной эндометрия. Только таким образом можно выбрать оптимальный момент для индукции овуляции и пункции фолликулов. Также благодаря наблюдению удается снизить риск гиперстимуляции.
Забор яйцеклеток. Когда созревание яйцеклеток в фолликулах подходит к концу, отменяют введение ФСГ. Теперь с помощью гормона ХГЧ (хорионический гонадотропин человека), яйцеклетки подготавливаются к овуляции. ХГЧ берет на себя роль ЛГ, которую последний выполняет в естественном цикле. Спустя в среднем 36 часов после введения ХГЧ, незадолго до овуляции, происходит забор яйцеклеток из фолликулов (пункция фолликулов, рис. 7.5.2).
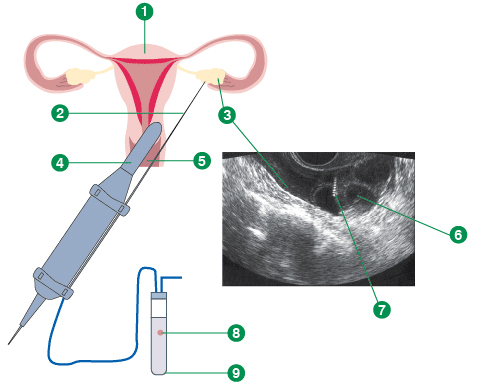
Рис 7.5.2. Пункция фолликулов
1 - матка, 2 - игла для забора яйцеклетки, 3 – яичник, 4 - ультразвуковой датчик, 5 – влагалище, 6 – фолликул, 7 – игла, 8 – яйцеклетка, 9 – пробирка.
|
|
|
Пункция фолликулов проводится через влагалище под контролем УЗИ. Для обезболивания используются успокоительные средства, местная или общая анестезия. После процедуры возможны легкие боли и небольшие кровянистые выделения. Эта процедура не требует госпитализации. После обсуждения результатов пункции пациенты уходят домой.
Оплодотворение и перенос эмбрионов. Для оплодотворения яйцеклеток в день пункции необходимо наличие свежей спермы супруга. В редких случаях супруг сдает сперму заранее, и она хранится в лаборатории при очень низкой температуре (криоконсервация спермы). Получение спермы "по требованию" бывает не всегда возможным. Это связано со стрессом, который нередко испытывают пациенты. Поэтому совершенно необходимо своевременно указать на возможную "проблему" при получении спермы, для того чтобы ситуация была вовремя разрешена.
Перед оплодотворением сперма обрабатывается в лаборатории таким образом, чтобы оплодотворяющая способность сперматозоидов была оптимальной. Далее яйцеклетки и сперматозоиды совместно культивируют в инкубаторе 24 часа в питательной среде.
Эмбрионы культивируют еще 2 или 4 суток. Проводится наблюдение за их дроблением (делением). Параллельно осуществляется выбор тех эмбрионов, которые имеют наилучшие шансы для имплантации и будут использоваться для подсадки. Оставшиеся эмбрионы хорошего качества могут быть сохранены при очень низкой температуре для дальнейших попыток (криоконсервация эмбрионов).
Перенос эмбрионов в полость матки – совершенно безболезненная процедура (рис. 7.5.3). Ее проводят на 3-й или 5-й день после пункции. Перенос эмбрионов происходит с помощью очень тонкого мягкого пластмассового катетера, который через влагалище и цервикальный канал вводится в матку. Если в полость матки переносят более двух эмбрионов, существенно повышается риск многоплодной беременности.
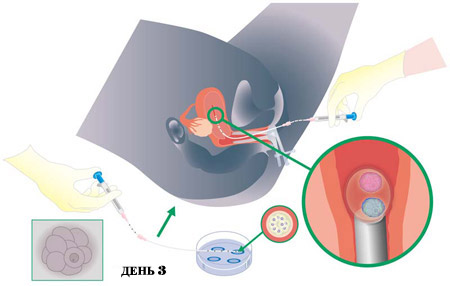
Рис. 7.5.3. Перенос эмбрионов в полость матки.
Наблюдение после переноса эмбрионов. После переноса эмбрионов в полость матки назначают препараты прогестерона и эстрогены, чтобы поддержать имплантацию эмбриона. В этом случае говорят о поддержке лютеиновой фазы.
Спустя 2 недели после подсадки проводится первый тест на беременность. Однако в этот момент еще нельзя оценить и прогнозировать дальнейшее течение беременности. Теперь рекомендуется избегать стрессов, физического и эмоционального перенапряжения. Несмотря на психическое напряжение, необходимо попытаться сохранить равновесие и покой. Не следует вносить существенные изменения в профессиональный и домашний распорядок дня. Чтобы точно знать, как протекает беременность, и получить своевременную помощь, необходимо наблюдение акушера-гинеколога.
|
|
|
Не исключены следующие осложнения:
- внематочная беременность. Эмбрион может выходить через маточную трубу в брюшную полость или начать свое развитие в маточной трубе. Учитывая, тот факт, что ЭКО применяется часто при трубном бесплодии, риск развития внематочной беременности ниже (1 – 2 %) чем у обычных женщин (4–5%);
- многоплодная беременность. При ЭКО вводится сразу несколько оплодотворенных яйцеклеток для увеличения эффективности. Развиваться в полости матки могут все яйцеклетки, обусловливая многоплодную беременность;
- гиперстимуляция яичников. Вследствие лекарственной стимуляции яичники могут увеличиваться в размерах, могут появляться связанным с этим боли;
- инфицирование. Риск этого осложнения крайне низок и связан прежде всего с медицинскими манипуляции. Составляет 0,1 %.
Беременность и роды
Беременность при ЭКО наступает в 20 - 25 % случаев. Поэтому сама процедура называется попыткой. Из 20 наступивших беременностей родами заканчиваются в среднем 18. После введения эмбрионов один раз в 3 дня нужно контролировать уровень гормонов в крови. Через 12 дней выполняется тест на беременность. В случае многоплодной беременности по желанию женщины выполняют редукцию — удаление ненужных эмбрионов.
Роды при беременности после ЭКО ничем не отличаются от обычных. В тех случаях, когда причина бесплодия — болезнь женщины, роды проводятся с учетом конкретной болезни и к способу оплодотворения это уже не имеет никакого отношения.
По мнению врачей, дети, зачатые в пробирке, ни чем не отличаются от остальных. Тем не менее, есть мнение, что такие дети лучше учатся, но чаще болеют. Врачи считают, что это может быть связано с чрезмерной опекой желанного ребенка.
|
|
|


