 |
Значение рН различных систем
|
|
|
|
| Среды организма | рН |
| Сыворотка крови | 7,36-7,44 |
| Чистый желудочный сок | 0,9 |
| Сок поджелудочной железы | 7,5-7,8 |
| Желчь в протоках | 7,4-8,5 |
| Желчь в пузыре | 5,4-6,9 |
| Моча | 4,8-7,5 |
| Молоко | 6,6-6,9 |
| Дистиллированная вода, находящаяся в равновесии с воздухом | 5,5 |
| Морская вода | 8,0 |
| Свежий яичный белок | 8,0 |
Значение рН, благоприятные для развития патогенных бактерий
| Вид бактерий | рН |
| Стафилококки | 7,4 |
| Стрептококки | 7,4-76 |
| Пневмококки | 7,6-7,8 |
| Менингококки | 7,4-7,6 |
| Гонококки | 7,0-7,4 |
В организме человека присутствуют различные буферные системы. Из них наиболее важными являются: гидрокарбонатная, гемоглобиновая, фосфатная и белковая.
Гидрокарбонатная система образована оксидом углерода (IV) (как кислота) и гидрокарбонат-ионом (как сопряженное основание). Для гидрокарбонатного буфера рН рассчитывают по формуле:

Это уравнение носит название уравнения Гендерсона-Гассельбаха. Значение рК  для данного уравнения отличается от справочной величины рКа для Н2СО3, и равно 6,1.
для данного уравнения отличается от справочной величины рКа для Н2СО3, и равно 6,1.
С учетом коэффициента растворимости СО2 получим другую форму уравнения Гендерсона-Гассельбаха:
 , где
, где
 - парциальное давление СО2.
- парциальное давление СО2.
В организме протекает обратимая реакция:
СО2 + Н2О «Н2СО3 «Н+ + НСО 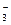
Она ускоряется ферментом карбоангидразой. Изменение концентрации любой составной части этого буфера приводит к смещению равновесия и соотношение концентраций остается постоянным. Буферная емкость гидрокарбонатного буфера по кислоте значительно выше, чем буферная емкость по основанию. Поэтому главное назначение этого буфера в нейтрализации кислот.
Гидрокарбонатный буфер является основной буферной системой плазмы крови и является системой быстрого реагирования, т.к. продукт его взаимодействия с кислотами – СО2 быстро выводится через легкие. Гидрокарбонатный буфер также содержится в эритроцитах, почечной ткани и интерстициальной жидкости.
|
|
|
Гемоглобиновая буферная система представлена двумя слабыми кислотами – гемоглобином и оксигемоглобином – и сопряженными им основаниями, соответственно гемоглобинат- и оксигемоглобинат-ионами:
ННb «H+ + Hb-
кислота основание
HHbO2 «H+ + HbO 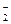
Гемоглобиновый буфер является буферной системой эритроцитов. Оксигемоглобин – более сильная кислота (рКа=6,95), чем гемоглобин (рКа=8,20). Поэтому присоединение кислорода к гемоглобину понижает рН крови. С другой стороны, при отдаче кислорода в тканях рН крови вновь возрастает.
Фосфатная буферная система функционирует в основном в плазме. Она представлена ионами Н2РО  (кислота) и НРО
(кислота) и НРО  (основание). Фосфатная буферная система более консервативна, т.к. избыточные продукты нейтрализации выводятся через почки.
(основание). Фосфатная буферная система более консервативна, т.к. избыточные продукты нейтрализации выводятся через почки.
В организме также функционируют:
· белковая или протеиновая;
· аминокислотная;
· аммиачная (в почках) буферные системы.
Разбор типовых задач
1. Вычислите рН фосфатного буфера, составленного 100 мл 0,1 М КН2РО4 и 50 мл 0,15 М К2НРО4.
Решение: Расчет рН фосфатного буфера проводим по формуле:
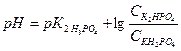
Значение  = 6,8 (берем из справочника).
= 6,8 (берем из справочника).
Так как концентрация вещества пропорциональна количеству вещества:
n = C×V,
то в формулу подставим количества вещества КН2РО4 и К2НРО4.

2. При смешении 10 мл 0,1 М формиата натрия с 5 мл 0,05 М раствора НС1 был получен формиатный буфер. Рассчитайте значение рН этого раствора.
Решение: При смешении этих растворов протекает реакция:
HCOONa + HCl = HCOOH + NaCl
Из расчета количества вещества видно, что HCOONa в избытке.
nHCOONa = 0,01×0,1 = 0,001 моль
nНС1 = 0,005×0,05 = 0,00025 моль
После реакции формиата натрия останется:
nHCOONa = 0,001 - 0,00025 = 0,00075 моль
Вместе с образовавшейся муравьиной кислотой формиат натрия образует формиатный буфер nHCOOН = nНС1 = 0,00025 моль.
|
|
|
Расчет рН ведем по формуле:

Здесь учли, что рКНСООН = 3,75.
3. Как изменится рН фосфатного буфера, содержащего 100 мл дигидрофосфата калия и 300 мл раствора гидрофосфата калия (концентрации исходных растворов равны по 0,1 моль/л), при добавлении к нему 20 мл раствора NaOH с концентрацией 0,1 моль/л?
Решение: Сначала рассчитаем значение рН исходного раствора:
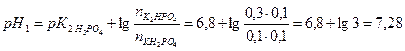
При добавлении NaOH с ним в первую очередь взаимодействует КН2РО4 по схеме:
КН2РО4 + NaOH = NaKHPO4 + H2O
Часть дигидрофосфата переходит в гидрофосфат.
 = 0,1×0,1 = 0,01 моль;
= 0,1×0,1 = 0,01 моль;  = 0,02×0,1 = 0,002 моль
= 0,02×0,1 = 0,002 моль
После реакции дигидрофосфата калия останется:
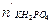 = 0,01 - 0,002 = 0,008 моль
= 0,01 - 0,002 = 0,008 моль
Общее количество гидрофосфата станет:
 = 0,3 × 0,1 + 0,002 = 0,032 моль
= 0,3 × 0,1 + 0,002 = 0,032 моль
Рассчитаем рН полученного раствора:

Изменение рН составит:

4. В каком мольном соотношении надо смешать аммиак и хлорид аммония, чтобы получить буферный раствор с рН = 9,0, если рК 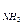 =4,75?
=4,75?
Решение: Расчет рН аммонийного буфера проводят по формуле:

Подставляя значения рН и рК 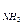 получим:
получим:
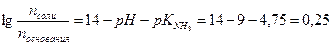
Тогда:

Следовательно, мольное соотношение NH4Cl к NH3 должно быть:
n  : n
: n 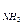 ® 1,78: 1
® 1,78: 1
5. К 100 мл крови для изменения рН от 7,36 до 7,00 надо дабавить 3,6 мл соляной кислоты с концентрацией 0,1 моль/л. Какова буферная емкость крови по кислоте?
Решение: Расчет буферной емкости по кислоте проводят по формуле:

Лабораторная работа
Задание 1. Приготовление буферного раствора.
В три пробирки внесите 0,1 М растворы СН3СООН и СН3СООNa в соотношении (по объему): 9:1, 5:5 и 1:9. Каждый приготовленный раствор хорошо перемешать. Во все три пробирки прибавьте по 3 капли индикатора метилового оранжевого или метилового красного. Сравните и запишите окраску растворов. По известной формуле рассчитайте значения рН во всех трех растворах. В каких пределах изменилось значение рН?
Задание 2. Влияние разбавления на рН буферных растворов.
Приготовьте 3 раствора ацетатного буфера в соотношении 9:1, 5:5 и 1:9 как в предыдущем опыте. Затем в 3 чистые пробирки отберите по 2 мл приготовленных буферных растворов и добавьте в каждую из них по 8 мл дистиллированной воды. Растворы хорошо перемешайте. Во вновь приготовленные растворы (с разбавлением) добавьте по 3 капли индикатора метилового красного как и в первом случае. Сравните окраски растворов между собой и с первыми тремя пробирками. Сделайте заключение по окраске содержимого пробирок. С учетом разбавления исходных растворов вновь рассчитайте значения рН полученных растворов. Результаты наблюдений и расчетов внесите в таблицу по форме и сделайте выводы.
|
|
|
| Номера пробирок | ||||||
| Соотношение кислота: соль в буферном растворе | ||||||
| Окраска растворов после добавления индикатора | ||||||
| Расчетное значение рН |
Задание 3. Определение буферной емкости по кислоте и по щелочи.
В конической колбе приготовьте буферный раствор, смешав 10 мл 0,1 М СН3СООН и 10 мл 0,1 М раствора СН3СООNa. В другой колбе приготовьте раствор – свидетель, смешивая 18 мл 0,1 М СН3СООН и 2 мл 0,1 М СН3СООNa.
В обе колбы внесите по 3 капли раствора метилового оранжевого. Сравните окраску растворов. Затем содержимое первой колбы титруйте из бюретки 0,1 М раствором НС1 до получения одинаковой окраски с раствором – свидетелем. Запишите затраченный объем раствора НС1 и рассчитайте по известной формуле буферную емкость ацетатного буфера. Значение рН содержимого 1 и 2 колб берите из расчетных величин 2 и 3 пробирок (см. табл. из пред. задания). Бюретку с 0,1 М раствором НС1 надо приготовить соблюдая правила ацидометрии параллельно с приготовлением содержимого 1 и 2 колб.
Для определения емкости ацетатного буфера по щелочи надо приготовить колбу с содержанием 10 мл 0,1 М СН3СООН и 10 мл 0,1 М СН3СООNa и раствор – свидетель (другая колба), содержащий 18 мл 0,1 М СН3СООNa и 2 мл 0,1 М СН3СООН. После добавления 3 капель раствора метилового оранжевого в каждую колбу, содержимое 1-ой колбы титруйте из бюретки 0,1 М раствором NaOH до одинаковой окраски с раствором – свидетелем. Записав объем затраченного раствора NaOH рассчитайте буферную емкость по щелочи. Значения рН содержимого 1-ой и 2-ой колб берите из расчетных величин 2 и 1 пробирок (см. табл. из пред. задания). Бюретку с 0,1 М раствором NaOH надо приготовить соблюдая правила алкалиметрии параллельно с приготовлением содержимого 1-ой и 2-ой колб.
|
|
|
Сравните буферную емкость ацетатного буфера по кислоте и по щелочи. Сделайте выводы.
|
|
|


