 |
5. Задачи для внеаудиторной самостоятельной работы.
|
|
|
|
5. Задачи для внеаудиторной самостоятельной работы.
5-1. Давления пара чистых C6H5Cl и C6H5Br при 140 °C равны 123, 7 и 65, 8 кПа. Рассчитать состав раствора C6H5Cl – C6H5Br, который при давлении 100 кПа кипит при температуре 140 °C, а также состав образующегося пара. Каково будет давление пара над раствором, полученным конденсацией образующегося пара?
5-2. Бензол и дихлорэтан образуют смеси, подчиняющиеся закону Рауля. При 40 °С давления пара бензола и дихлорэтана соответственно равны 24, 3 и 20, 6 кПа. Вычислите при этой температуре парциальное давление насыщенных паров каждого компонента и общее давление смеси, содержащей: 1) 0, 2 мольные доли бензола; 2) 500 гбензола и 500 гдихлорэтана.
5-3. Растворимость хлора в воде при 20 °С равна 0, 729 гв 100 гводы. Вычислите массу хлора, растворенного в 5 лводы при давлении 202, 6 кПа. Плотность воды считать равной 1.
5-4. Коэффициент абсорбции метана в воде при 20 °С равен 0, 0331. Сколько граммов метана растворится в 4 л воды при 20 °С и давлении 303, 9 кПа.
5-5. Вычислите осмотическое давление раствора, содержащего в 250 мл0, 538 г фруктозы, при 27 °С?
5-6. Определите осмотическое давление 5-процентного раствора свекловичного сахара при 15 °С. Плотность раствора 1, 019 г/см3.
5-7. Постройте по данным таблицы кривые зависимости парциальных давлений паров ацетона и сероуглерода и общего давления паров смесей от состава жидкости при температуре 35, 17 °С. Пользуясь диаграммой: 1) найдите парциальные давления и общее давление пара смесей, содержащих: а) 20% (мольных) сероуглерода и б) 20 моль сероуглерода + 20 моль ацетона; 2) определите состав смеси, которая будет кипеть при 79, 97 кПа.
| % (мольные) сероуглерода | Давление паров, кПа | |||
| в жидкости | в паре | сероуглерода | ацетона | общее |
| 45, 83 | 45, 82 | |||
| 6, 24 | 25, 06 | 14, 75 | 44, 12 | 58, 87 |
| 13, 30 | 40, 12 | 27, 52 | 41, 09 | 68, 62 |
| 28, 69 | 54, 52 | 43, 81 | 36, 55 | 80, 36 |
| 44, 74 | 60, 94 | 52, 04 | 33, 35 | 85, 38 |
| 61, 61 | 65, 50 | - | - | 87, 12 |
| 67, 13 | 66, 80 | 58, 38 | 28, 92 | 87, 30 |
| 82, 80 | 72, 07 | 61, 97 | 24, 02 | 85, 98 |
| 92, 42 | 80, 29 | 65, 31 | 16, 03 | 81, 35 |
| 96, 92 | 89, 02 | 66, 91 | 8, 264 | 75, 17 |
| 68, 28 | 68, 28 | |||
 5-8. Метиловый спирт и бензол образуют азеотропную смесь, содержащую 39 % СН3ОН и 61% С6Н6, которая кипит при 57, 9 °С. Температуры кипения метилового спирта и бензола соответственно равны 64, 7 °С и 80, 2 °С. Что будет собрано в приемнике и что останется в перегонном аппарате при фракционной перегонке смеси, состоящей из 60% СН3ОН и 40% C6H6?
5-8. Метиловый спирт и бензол образуют азеотропную смесь, содержащую 39 % СН3ОН и 61% С6Н6, которая кипит при 57, 9 °С. Температуры кипения метилового спирта и бензола соответственно равны 64, 7 °С и 80, 2 °С. Что будет собрано в приемнике и что останется в перегонном аппарате при фракционной перегонке смеси, состоящей из 60% СН3ОН и 40% C6H6?
|
|
|
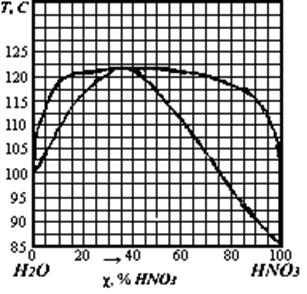
5-9. Используя диаграмму (рис. 5) ответьте на следующие вопросы:
 1) При какой температуре начнется конденсация пара, содержащего 10 % Н2О? Каков состав первой капли жидкости при конденсации?
1) При какой температуре начнется конденсация пара, содержащего 10 % Н2О? Каков состав первой капли жидкости при конденсации?
2) Сколько фаз, какие и какого состава
находятся в равновесии, если раствор, содержащий 20 % Н2О, нагрет до 105 º С?
3) На какие составные части можно разогнать в ректификационной колонне раствор, содержащий 30 % Н2О?
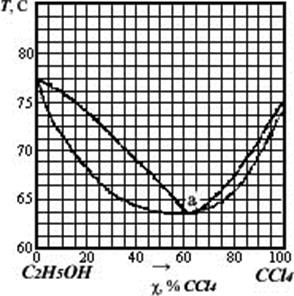
5-10. Используя диаграмму (рис. 6) ответьте на следующие вопросы:
1) Смесь С2Н5ОН и ССl4 неизвестного состава начинает кипеть при температуре 70 º С. Определите ее состав, если при добавлении к ней нескольких миллилитров ССl4 температура начала кипения опустилась до 65º С.
2) Какой состав будет иметь конденсат после ректификации смеси, содержащей 40 % (мольн. ) ССl4?

Занятие №11.
План занятий:
1. Тестовый контроль знаний по теме «Давление пара над раствором. Осмос. Растворимость газов в жидкостях. Закон Генри. Перегонка жидких смесей».
2. Растворы электролитов. Электрохимические системы. Кинетика электродных растворов.
3. Решение задач на тему «Растворы электролитов. Электрохимические системы. Кинетика электродных растворов».
|
|
|
4. Коллоквиум на тему «Химическая термодинамика. Химическое и фазовое равновесие. Растворы (неэлектролитов)».
1. Тестовый контроль знаний по теме «Давление пара над раствором. Осмос. Растворимость газов в жидкостях. Закон Генри. Перегонка жидких смесей».
1. Согласно какому закону изменяется давление насыщенного пара газообразного растворенного вещества, как функция его концентрации в растворе?
1. По закону Рауля;
2. По закону Коновалова;
3. По закону Генри;
4. По закону Нернста – Шилова.
|
|
|


