 |
Химико-технологического процесса
|
|
|
|
Материальный баланс – это основное звено в оценке технико-экономической эффективности химико-технологического процесса.
Для любой закрытой системы, в которой отсутствует взаимодействие с окружающей средой и изменение массы веществ является только результатом химических реакций, справедливо уравнение материального баланса, основанное на законе сохранения массы,
 (3.1)
(3.1)
или
 (3.2)
(3.2)
Левую часть уравнения (2.1) составляет масса всех входящих в аппарат материальных потоков, а правую часть – масса выходящих материальных потоков и материальные потери. В уравнениях (3.1) и (3.2) количество веществ, участвующих в реакциях обычно выражают в г, кг или г/мин, кг/час и т. д. Однако в действительности при химических реакциях вещества расходуются и образуются в мольных соотношениях и поэтому для материальных расчетов более удобно их количества выражать в молях (моль/час).
Для количества веществ, выражаемых числом молей, уравнение (3.2) написать нельзя, так как во многих случаях во время реакции число молей изменяется.
Однако для любой реакции, простой или сложной, можно ввести понятие полноты химической реакции (m), через которую можно легко рассчитать материальный баланс в молях (моль/час).
В частности для простой реакции
νаА + νbB → νCC
верно следующее равенство:
 (3.3)
(3.3)
При этом величина m будет всегда положительная и инвариантна в отношении участников реакции.
Теоретический материальный баланс рассчитывается с учетом только стехиометрии целевой реакции.
Практический материальный баланс рассчитывают с учетом состава исходного сырья, избытка одного из исходных реагентов, степени превращения исходных веществ, селективности, потерь сырья или готового продукта.
|
|
|
В то же время, по материальному балансу, полученному на основании экспериментальных данных, можно решить обратную задачу: определить важнейшие технико-экономические показатели процесса (выход, селективность, степень превращения, расходные коэффициенты и др.).
Степень превращения - это доля реагента, израсходованного на химическую реакцию. Она показывает эффективность использования расходуемых реагентов.
 , (3.4)
, (3.4)
где Хi - степень превращения i-го реагента; Gi,0 – количество i-го реагента в исходной реакционной смеси; Gi -количество i-го реагента в конце процесса.
Селективность – это отношение количества исходного реагента, расходуемого на целевую реакцию, к общему количеству реагента, пошедшего на реакцию (то есть доля реагента, претерпевшего превращение в какой-то продукт).
|
 | |||
| |||
 , (3.5)
, (3.5)
где Ф(А®R) – cелективность процесса по продукту R; G(A®R) - количество вещества А, превращенного в целевой продукт R; GA,0 - начальное количество вещества А; GA - количество вещества А после реакции; хA - степень превращения вещества А.
Выход продукта - отношение фактически полученного количество продукта к максимально возможному количеству, которое теоретически можно получить в соответствии со стехиометрией химической реакции:
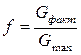 (3.6)
(3.6)
где f - выход продукта; GФ - количество фактически полученного продукта; Gmax - количество продукта в соответствии со стехиометрией реакции.
Для реакции:
νаА + νbB →νRR + νCC
 (3.7)
(3.7)
Для простых необратимых реакций выход продукта равен степени превращения:
 (3.8)
(3.8)
В случае обратимой химической реакции максимально возможное количество продукта – это такое количество, которое теоретически можно получить в момент равновесия, то есть Gmax= G*R:
|
|
|
 (3.9)
(3.9)
Для параллельно протекающих реакций, в которых наряду с целевым продуктом R получаются побочные, например С,

Максимально возможное количество продукта R будет получено в том случае, если весь исходный реагент А будет реагировать только по первой (целевой) реакции:
 (3.10)
(3.10)
Следует отметить, что выразить GR,ф через степень превращения и начальное количество А, в случае сложной реакции, нельзя, так как расходование вещества А происходит не только в целевом, но и в побочном направлении.
Так же будет выглядеть и выражение для выхода целевого продукта R в случае последовательной реакции.
Между выходом целевого продукта, степенью превращения и селективностью существует простая связь:
 (3.11)
(3.11)
Расходные коэффициенты -величины, характеризующие расход различных видов сырья, воды, топлива, электроэнергии, пара на единицу полученной продукции. Особое значение имеют расходные коэффициенты по сырью, поскольку для большинства химических производств 60-70% себестоимости продукции приходится на эту статью расхода. Различают теоретические и практические расходные коэффициенты. Теоретические расходные коэффициенты учитывают расход исходного сырья с учетом стехиометрии реакции.
 , (3.12)
, (3.12)
где  - теоретический расходный коэффициент; ni, nj – стехиометрические коэффициенты при реагенте и продукте; Mri, Mrj – молекулярная масса реагента и продукта соответственно.
- теоретический расходный коэффициент; ni, nj – стехиометрические коэффициенты при реагенте и продукте; Mri, Mrj – молекулярная масса реагента и продукта соответственно.
Практические расходные коэффициенты учитывают селективность процесса, выход продукта, степень превращения и рассчитывают на базе теоретических расходных коэффициентов.
 ,(3.13)
,(3.13)
где  - практический расходный коэффициент; f - технологический выход; xi - степень превращения i -го реагента; F - селективность процесса; ii - содержание i -го реагента в исходном веществе.
- практический расходный коэффициент; f - технологический выход; xi - степень превращения i -го реагента; F - селективность процесса; ii - содержание i -го реагента в исходном веществе.
Расходные коэффициенты обычно рассчитывают на 1 тонну целевого продукта.
Данные материального баланса используют при составлении теплового (энергетического) баланса, термодинамических и кинетических расчетах, расчетах реактора. Правильность составления материального баланса определяется после сравнения приходной и расходной частей, выраженных в единицах массы. При балансовых расчетах обычно наблюдается расхождение между суммой расхода и прихода, которое не должно превышать 5%.
|
|
|
|
|
|


