 |
Определение кислотного числа продукта
|
|
|
|
ОДЕССКИЙ НАЦИОНАЛЬНЫЙ ПОЛИТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ
ХИМИКО-ТЕХНОЛОГИЧЕСКИЙ ФАКУЛЬТЕТ
КАФЕДРА ОРГАНИЧЕСКИХ И ФАРМАЦЕВТИЧЕСКИХ ТЕХНОЛОГИЙ
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
К лабораторным работам по курсу
«ХИМИЯ И ТЕХНОЛОГИЯ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ»
Одесса 2002
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ УКРАИНЫ
ОДЕССКИЙ НАЦИОНАЛЬНЫЙ ПОЛИТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ
ХИМИКО-ТЕХНОЛОГИЧЕСКИЙ ФАКУЛЬТЕТ
КАФЕДРА ОРГАНИЧЕСКИХ И ФАРМАЦЕВТИЧЕСКИХ ТЕХНОЛОГИЙ
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
К лабораторным работам по курсу
«ХИМИЯ И ТЕХНОЛОГИЯ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ»
для студентов специальности 7.110204 –
«Технология фармацевтических препаратов»
Утверждено
На заседании кафедры ОФТ
Протокол № 11 от 02.07.2002
Одесса ОНПУ 2002
Методические указания к лабораторным работам по курсу «Химическая технология лекарственных веществ» для студентов специальности 7.110204 /составители: В.И.Голиков, В.В.Лялин.- Одесса: ОНПУ,2002.- 21с
Составители к.х.н., доц. Голиков Вячеслав Ильич
к.х.н., доц. Лялин Виктор Васильевич
Ответственный за выпуск д.х.н.,проф. Куншенко Б.В.
Утверждено методической комиссией химико-технологического факультета ОНПУ.
Тема 1. ЭТЕРИФИКАЦИЯ
Лабораторная работа
"СИНТЕЗ ЭФИРОВ УКСУСНОЙ КИСЛОТЫ"
Ацетаты жирных спиртов используются в промышленности широко и в больших количествах. Их синтез осуществляется в основном по реакции этерификации, которая является типичным примером обратимой реакции, катализируемой протонодонорными кислотами (серной, соляной, сульфокислотами), катионообменными смолами, тетрабутоксититаном и др. в жидкой фазе.
|
|
|


Cостояние равновесия зависит от молярной массы и строения кислоты и спирта. Практически до конца можно провести процесс этерификации, если непрерывно удалять из сферы реакции хотя бы один из образующихся компонентов (эфир или воду). В промышленности используют их способность отгоняться из реакционной смеси индивидуально или в составе азеотропов (табл.1).
Таблица 1
| Синтезируемый эфир | Отгоняется |
| Этилацетат Бутилацетат Бутилфталат Бутилацетат | Эфир вода + эфир вода + спирт избыт. вода + спец. Агент |
Если отгоняется гетерогенный азеотроп, то после охлаждения он разделяется на два слоя. Верхний, органический слой возвращают обратно в реактор, отводят только нижний - водный слой.
Экспериментальная установка
Экспериментальная установка состоит из куба - термостойкой колбы вместимостью 500 мл со шлифом, дефлегмирующей колонки с ловушкой Дина-Старка и обратного водяного холодильника. Куб обогревается специальным колбонагревателем с закрытой спиралью, напряжение тока на котором регулируется ЛАТРом.
|
|
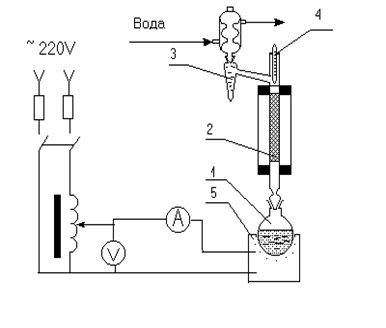
Рис. 1. Схема лабораторной установки
Используемые реактивы:
н-бутиловый спирт - 0,55 моль
уксусная кислота ледяная - 0,50 моль
серная кислота (конц.) - 0,3 мл
н-гексан - 100 мл
сульфат натрия (прокаленный)
Проведение эксперимента
В куб заливают рассчитанное количество спирта, кислоты и катализатора (мерной пипеткой). Колбу присоединяют к дефлегмирующей колонке и сверху, через сепаратор, заливают гексан. При этом часть его остается в сепараторе, а остальное стекает через колонку в куб. Проверив герметичность всех соединений, пускают воду в обратный холодильник и начинают нагрев куба. В ходе синтеза реакционная масса умеренно кипит, а из холодильника в сепаратор стекает 1-2 капли конденсата в секунду. Отмечают время начала кипения.
|
|
|
Через некоторое время при внимательном наблюдении можно заметить начало образования водного слоя на дне ловушки. Для удобства наблюдения за нею надо поместить светлый экран. Начиная с этого момента, сведения об объеме выделившейся воды (ловушка градуирована) и о времени наблюдения заносят в таблицу 2. Необходимо произвести 8-10 замеров.
Таблица 2
| № п/п | Начало кипения | ||||||||
Время, час., мин.
Время после начала кипения t, мин.
Объем воды  , мл. , мл.
|
Время окончания реакции определяют по прекращению выделения воды и по ее количеству. Выключают колбонагреватель, подачу воды в холодильник. После охлаждения реакционной колбы ее содержимое переносят в делительную воронку вместимостью 250 мл, где его сначала промывают 100 мл воды, затем 100 мл водного раствора соды (массовая доля 5 %) и снова водой, как вначале. Хорошо отстоявшийся органический слой аккуратно сливают без капли воды) в сухую коническую колбу вместимостью 200 мл с хорошей пробкой и сушат прокаленным сульфатом натрия несколько часов (в два приема).
Жидкость фильтруют во взвешенный куб ректификационной колонки, оставляя в колбе тяжелый нижний слой сульфата натрия. Взвешивая куб с фильтратом, определяют начальную массу смеси. В отдельные, чистые, сухие, взвешенные приемники отгоняют три фракции: 1-я - до 700С, 2-я - 70-1250С, 3-я - 125-1270С. Последняя фракция - целевая. Взвесив приемники с погонами и куб с остатком, заносят в табл.3 сведения о массах m и подводят материальный баланс. Определяют показатель преломления продукта при 200С и заносят его в таблицу.
Определение кислотного числа продукта
Кислотным числом (К.Ч.) называется число мг КОН, необходимое для нейтрализации свободных кислот, содержащихся в массе 1 г вещества (другое название - "число нейтрализации").
В чистую, сухую колбу вместимостью 100 мл из термостойкого стекла со шлифом и помещают навеску массой около 0,15 г вещества, взвешивают с точностью до 0,0002 г, добавляют 15 мл этилового спирта, 3-4 капли индикатора (0,1 % спиртовый раствор тимолового синего с массовой долей) и титруют 0,1 н спиртовым раствором КОН. Конец титрования определяется переходом окраски от желтой к голубой в щелочной среде. Параллельно проводят слепой опыт.
|
|
|
Расчет кислотного числа ведется по уравнению
К.Ч.  (1)
(1)
где  - объемы 0,1 н раствора КОН, израсходованного на титрование пробы и слепого опыта, мл;
- объемы 0,1 н раствора КОН, израсходованного на титрование пробы и слепого опыта, мл;
m - навеска пробы, г.
|
|
|


