 |
3.3.7.г. Термодинамика общего кислотного и основного катализа
|
|
|
|
3. 3. 7. г. Термодинамика общего кислотного и основного катализа
Параметры активации. Главное уравнение термодинамики в применении к скоростям реакций записывается следующим образом:
G#=H#-TS# (3. 26)
где значком # обозначается, что берется разность между переходным состоянием и реагентами.
Свободная энергия активации пропорциональна логарифму константы скорости: G#= -2, 3RTlgk. Энтальпия активации в одностадийных реакциях или в многостадийных реакциях, медленной стадией которых является первая, всегда положительна, и лишь в редких случаях используется для установления механизма, однако энтропия активации S#=Sо (переходное состояние) - Sо (реагенты) в этом отношении очень информативна. Как и в случае Sо (раздел 3. 3. 3. а), S# можно представить как сумму изменений поступательных, колебательных и вращательных степеней свободы. Чем более упорядоченно друг относительно друга расположены атомы реагирующих молекул в переходном состоянии по сравнению с исходным, и чем более сольватировано переходное состояние по сравнению с исходным, тем S# более отрицательна. Типичные значения энтропии активации для главных типов органических реакций приведены в табл. 3. 1.
Таблица 3. 10.
Типичные значения logА и S# для реакций разных типов
| Тип реакции (пример) | logA | S#, кал/К. моль |
| Мономолекулярная диссоциация А-В А+В | 15-17 (с-1) | +8 до +17 |
| Мономолекулярное отщепление > CX-CY< > C=C< +XY | 12, 5-14 (с-1) | -3 до +4 |
| Мономолекулярная перегруппировка | 9-13 (с-1) | -20 до 0 |
| Бимолекулярная ассоциация А+В А-В | 9-10, 5 (л/моль. с) | -20 до -15 |
| Бимолекулярное замещение А+И-С А-В+С | 7-11 (л/моль. с) | -30 до -10 |
| Бимолекулярная многоцентровая реакция | 5-9 (л/моль. с) | -40 до -20 |
Экспериментально величины Н# и S# можно определить из уравнения Аррениуса:
|
|
|
к=Ае-Ea/RT,
где Ea - энергия активации реакции, которая определяется из температурной зависимости логарифма константы скорости (из наклона прямой в координатах lgk-1/T); А - предэкспоненциальный множитель. Энергия активации связана с энтальпией активации:
Н#=Еа-nRT,
где n - порядок реакции, а предэкспоненциальный множитель связан с энтропией активации соотношением
A=(kT/h)eneS#/R,
где k - постоянная Больцмана; h - постоянная Планка; R - газовая постоянная. Значения logA для разных реакций также даны в табл. 3. 10.
Термодинамические причины общего кислотного (и основного) катализа. Как уже упоминалось в разделах 3. 3. 6. б и 3. 3. 6. в, отличие общего кислотного катализа от специфического катализа ионом лиония состоит в том, что в первом случае в реакции участвует сопряженное основание катализирующей кислоты. Ниже приведены упрощенные схемы переноса протона в воде:
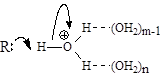
| 
|
| Специфический кислотный катализ R+H++(m+n)H2O | Общий основной катализ R+H++А-+(m+n)H2O |
При сравнении этих двух схем видно, что в случае общего кислотного катализа из-за включения А- в переходное состояние будет происходить дополнительная потеря поступательной и колебательной энергии. Расчеты показывают, что такая потеря составит 15-20 кал/(К. моль) что должно уменьшить скорость реакции в 103-104 раз. Почему же реакция не идет по пути взаимодействия только с ионом лиония, а еще и выбирает такой обременительный путь?
Ответ состоит в том, что включение сопряженного основания в переходное состояние скомпенсирует связанную с этим потерю энтропии. Если сопряженное основание является анионом А-, а остальная часть переходного состояния несет положительный заряд, то электростатическое взаимодействие может скомпенсировать потерю поступательной и вращательной энтропии. Другими словами, включение основания может понизить энтальпию активации. Например, при гидролизе триэтилортоацетата в случае специфического кислотного катализа образуется обладающий высокой энергией протонированный катион, а при общем кислотном катализе такой катион не образуется:
|
|
|
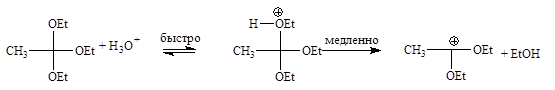
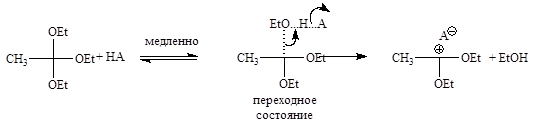
Для данной реакции энергетически (G#) выгоднее идти по второму пути, с потерей энтропии из-за включения в переходное состояние сопряженного основания кислоты АН, но зато с низкой энтальпией, чем преодолевать высокий барьер на стадии образования протонированного катиона - сопряженной кислоты орто-эфира.
|
|
|


