 |
3.3.7.д. Влияние на механизм времени жизни интермедиата
|
|
|
|
3. 3. 7. д. Влияние на механизм времени жизни интермедиата
Если в реакции образуется некий интермедиат, то механизм реакции зависит от времени его жизни. Если интермедиат разлагается мономолекулярно со скоростью большей, чем 1013 с-1 (предельное значение частоты колебаний), или бимолекулярно со скоростью большей, чем 5. 109 л/(моль. с) (предел скорости диффузии), то фактически его не существует, и реакцию нужно рассматривать как согласованный процесс с одновременным разрывом старых и образованием новых связей. Если интермедиат имеет большое время жизни, то он может существовать, но вопрос о том, пойдет ли реакция через него или найдет другой, более легкий, согласованный путь, зависит от строения субстрата, второго реагента, среды, присутствия катализаторов и т. п.
Чтобы проиллюстрировать связь между типом кислотно-основного катализа и времени жизни интермедиата, рассмотрим реакцию присоединения тиолов и тиолят-ионов к молекуле ацетальдегида. В обобщенном виде механизм нуклеофильного присоединения по карбонильной группе можно записать следующим образом:
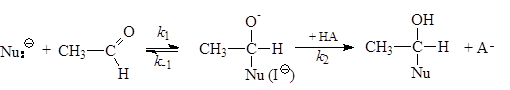 (3. 27),
(3. 27),
где Nu- - анион нуклеофила; k=kAH[AH] - константа скорости протонирования ионного интермедиата I-. Время жизни интермедиата I-зависит от склонности Nu- к отщеплению от этого интермедиата (k-1 в табл. 3. 11) и скорости протонизации I- (kAH[AH]) В первой реакции анион C2H5S- является сильнейшим нуклеофилом (см. разд. 9. 5. в, гл. 9), и следовательно, очень плохой уходящей группой. Этот анион плохо отщепляется от I-, и поэтому k-1 не очень велика. Протонизация I- идет гораздо быстрее, чем обратное отщепление C2H5S-; следовательно, медленной стадией всего процесса будет стадия k1. Кислота АН участвует в реакции только после наиболее медленной стадии k1, и никакого катализа наблюдаться не будет (коэффициент Бренстеда =0).
|
|
|
Таблица 3. 11
Механизм присоединения тиолятов и тиолов к ацетальдегиду
| Nu | к-1 (с-1) | Механизм | |
| C2H5S- | 6. 106 | некаталитический | |
| CH3O-C(O)-CH2S- | 7. 107 | см. рис. 3. 12 | захват I- кислотой АН |
| ArS- | 108-1010 | 0, 16-0, 26 | Н-связывание (предассоциация) |
| RSH | очень быстро | 0, 7 | согласованный |
| CF3CH2ОH (+CH2=O) | 0, 30 | согласованный |
При введении электроноакцепторной группы -СООСН3 анион тиолята становится менее нуклеофильным и более склонен отщепляться от I-, т. е. к-1 увеличивается. Поскольку G#-1 уменьшается, вторая стадия (к2) уже может влиять на скорость. Так, если I- достаточно быстро отщепляет Nu-, то буферная кислота НА может увеличивать общую скорость реакции (3. 27), захватывая I- и таким образом конкурируя или совсем подавляя реакцию к-1. Для Nu= СН3ООССН2S- в отсутствие АН к-1к2 (протонизация осуществляется растворителем, т. е. водой). При низких концентрациях [AH] скорость реакции (3. 27) возрастает вследствие увеличения скорости второй стадии. Теперь проявляется общий кислотный катализ, и величина коэффициента хотя и мала, но не равна нулю. Зависимость свободной энергии от коэффициента реакции показывает диаграмма на рис. 3. 10, б. При высоких АН или при добавлении более сильной кислоты АН стадия к2 становится очень быстрой (кАН5. 10-9 л/(моль. с), т. е. равна скорости диффузии), и тогда медленной будет опять первая стадия (рис. 3. 10, а), катализ исчезнет и уменьшится до нуля. Таким образом, график Бренстеда будет нелинеен.
В третьей реакции из табл. 3. 11. нуклеофилами являются арилтиолаты ArS-, которые как нуклеофилы не очень сильные вследствие делокализации отрицательного заряда по кольцу:

но зато (по этой же причине) имеют свойства хорошо уходящих групп. В этом случае к-1 настолько велика, что I- уже имеет по сравнению со скоростью диффузии очень короткое время жизни. Интермедиат I- не успевает захватиться кислотой, поскольку АН не успевает к нему продиффундировать за столь короткое время жизни. Это приводит к изменению механизма. Теперь вместо захвата реализуется каталитический путь, на котором АН играет роль не переносчика протона, а донора водородной связи с карбонильным кислородом альдегида. Образование водородной связи способствует увеличению скорости стадии присоединения нуклеофила (к1). Такой механизм называется предассоциативным:
|
|
|

Нейтральные тиолы RSH являются еще более слабыми нуклеофилами. Барьер на пути реакции к-1 в этом случае мал, и вследствие этого наблюдать интермедиат не удается. Если интермедиат образуется, то он сразу же протонируется и фактически процесс атаки Nu- и НА будет согласованным (практически одновременное присоединение нуклеофила и протона):
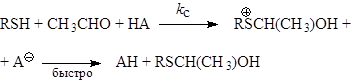
Перенос протона происходит уже не дискретно, а является частью сложного процесса со значительным барьером (кс). Коэффициент Бренстеда поэтому довольно велик: =0, 7. Для присоединения очень слабо нуклеофильного трифторэтанола (см. табл. 3. 11) к формальдегиду интермедиат I- также имеет очень короткое время жизни, и реакция фактически идет по согласованному пути:

* Буферным раствором называется раствор, содержащий сравнимые концентрации относительно слабой кислоты (в рассматривамом случае мета-нитрофенола) и ее сопряженного основания (мета-нитрофенолятного аниона). Роль буфера можно проиллюстрировать следующим примером. При добавлении 0, 01 мл концентрированной HCl в литр воды рН изменяется от 7 до 4. Если такое же количество HCl добавить в буферный раствор, содержащий равные количества ацетата натрия и уксусной кислоты, то рН уменьшится от 4, 75 всего лишь до 4, 74.
|
|
|


