 |
Уровень гормона в гипофизе и плазме
|
|
|
|
Гипофиз. На долю СТГ в гипофизе человека приходится приблизительно 2% влажной массы, что составляет 8—10 мг, хотя современные методы и не позволяют экстрагировать весь присутствующий в железе гормон. Его содержание у мужчин и женщин почти одинаково и существенно не зависит от возраста. Каждые сутки высвобождается менее 5% СТГ, содержащегося в гипофизе, причем считается, что значительная часть гормона подвергается разрушению в гипофизе, даже не будучи секретированной.
Плазма. Уровень СТГ в плазме взрослого человека в покое натощак обычно не достигает 2 нг/мл, а иногда оказывается ниже границы чувствительности метода. У женщин содержание СТГ несколько выше, чем у мужчин, причем при физической работе, когда оно повышается у лиц обоего пола, эта разница становится более отчетливой. В конце внутриутробной жизни и в течение нескольких первых дней после родов уровень СТГ очень высок (часто выше 50 нг/мл). В течение нескольких последующих недель он резко снижается, оставаясь чуть выше, чем у взрослых.
Только очень небольшая часть присутствующего в плазме СТГ экскретируется почками в иммунологически выявляемой форме. Концентрация СТГ в моче отражает его уровень в сыворотке, повышается в условиях гиперсекреции СТГ и снижается при гипопитуитаризме, но диагностическая ценность этого показателя при нарушениях секреции СТГ невелика.
Метаболический клиренс и секреция
Из плазмы СТГ элиминируется главным образом печенью и в меньшей степени почками. Период полужизни СТГ в сыворотке составляет, 20—25 мин [70], а скорость метаболического клиренса — примерно 110 мл/м2 в 1 мин с небольшими колебаниями при состояниях, характеризующихся его избыточной или недостаточной продукцией [71]. При гипотиреозе и диабете находили снижение скорости метаболического клиренса СТГ. В связи с этим, за исключением указанных состояний, изменение уровня СТГ в плазме точно отражает изменение скорости секреции гормона. У здоровых мужчин скорость секреции СТГ составляет примерно 350 мкг/м2 в сутки, тогда как у женщин в пременопаузе эта величина достигает 500 мкг/м2 в сутки.
|
|
|
Регуляция секреции
Секреция СТГ регулируется как рилизинг- (СТГ-РФ), так и ингибирующим (соматостатин) факторами гипоталамического происхождения. В нормальных физиологических условиях как нервные, так и иные механизмы регуляции секреции СТГ замыкаются, по-видимому, на уровне высвобождения одного или обоих факторов, а не прямо влияют на секрецию СТГ на уровне гипофиза. Поскольку в настоящее время высвобождение этих факторов из гипоталамуса in vivo в физиологических условиях не поддается определению, то о таком высвобождении судят по их конечному эффекту — изменению секреции СТГ.
Факторы, влияющие на секрецию СТГ, суммированы в табл. 7—4. Поскольку исходные концентрации СТГ столь часто находятся вблизи нижней границы возможностей определения, для демонстрации тормозных эффектов нередко требуется одновременное использование стимулирующего агента.
Нервная. К нервным стимулам, влияющим на секрецию СТГ, относятся как физические и психические стрессы, так и факторы, определяющие его эпизодическую секрецию и не связанные ни со стрессом, ни с видимыми метаболическими изменениями, что чаще регистрируется у детей и молодых лиц, чем у взрослых. Связанные с состоянием сна (суточные) вспышки секреции СТГ наиболее выражены в детстве, когда они наблюдаются и во время дневного сна, а с возрастом постепенно затухают (рис. 7—8). Установлено, что ночью секретируется 70% от общего суточного количества СТГ. Эти «вспышки» секреции гормона появляются, по-видимому, в начале глубокого сна, поскольку они отсутствуют, если человека будят перед наступлением III и IV стадий сна. Внимательный анализ такой связи у некоторых здоровых лиц при патологических состояниях, сопровождающихся изменениями медленноволнового сна и секреции СТГ, а также при воздействии фармакологических средств (например, имипрамина, флуразепама, метилскополамина и медроксипрогестерона), которые способны блокировать реакцию СТГ, позволил заключить, что ночная секреция СТГ — это процесс, часто начинающийся одновременно с наступлением сна, но не прочно связанный с нервными механизмами, определяющими развитие медленноволнового сна.
|
|
|
Метаболическая. Изменение концентраций энергетических веществ в крови и, что более важно, внутри клеток играет существенную роль в регуляции секреции СТГ. Увеличение содержания сахара в крови, будь то вследствие перорального или внутривен-ого введения глюкозы, подавляет секрецию СТГ. Этот феномен широко используется в диагностике акромегалии. Напротив, снижение уровня глюкозы в крови (а точнее — внутриклеточного метаболизма глюкозы), будь то вследствие действия инсулина или глюкозотолерантного теста в нисходящую фазу, стимулирует секрецию СТГ. Значение внутриклеточного метаболизма сахара иллюстрируется стимулирующим эффектом введения 2-дезоксиглюкозы, вызывающей гипергликемию с одновременной внутриклеточной глюкопенией за счет блокады фосфорилирования глюкозы. На сегодняшний день инсулиновая гипогликемия служит наиболее надежным стимулом, позволяющим оценить секреторную способность соматотрофов. Важными детерминантами реакции СТГ является как абсолютный уровень глюкозы, так и скорость снижения ее концентрации, поскольку быстрое уменьшение содержания глюкозы с гипергликемического уровня до нормы также может вызывать секрецию СТГ. В вентральном гипоталамусе обнаружены чувствительные к глюкозе нейроны, которые, как считают, «запускают» секрецию СТГ-РФ.
Таблица 7—4. Факторы, влияющие на секрецию гормона роста
| Стимулирующие | Угнетающие1 | ||
| Физиологические | |||
| Сон Физическая работа Стресс (физический пли психологический) Состояние после еды: гипераминацидемия гипогликемия (относительная) | Гиперглпкемия после еды Повышение содержания свободных жирных кислот | ||
| Фармакологические | |||
| Гипогликемия: абсолютная: инсулин или 2-дезо-ксиглюкоза относительная: после введевия глюкагона Гормоны: пептиды (АКТГ, a-МСГ, вазопрессин) эстрогены Нейротрансмиттеры и др. a-адренергические агонисты (клони-дин)бета-адренергические антагонисты (про-пранолол) предшественники серотонина (5-ОТ) дофаминергические агонисты (L-ДОФА, апоморфин, бром-криптин) агонисты ГАМК (мусцимол) аналоги анкефалина Пирогены (эндотоксин pseudomonas) | Гормоны: соматостатин гормон роста прогестерон глюкокортикоиды Нейротрансмиттеры и др. a-адренергические антагонисты (фентоламин) -адренергические агонисты (изопро-теренол) серотонинергические антагонисты (метизергид) дофаминергические антагонисты (фенотиазины) | ||
| Патологические | |||
| Снижение содержания белка и голодание Неврогенная анорексия Хроническая почечная недостаточность При акромегалии: ТРГ, ГнРГ | Ожирение При акромегалии: дофаминергические агонисты Гипо- и гипертиреоз | ||
|
|
|
Угнетающие эффекты некоторых факторов можно наблюдать только в присутствии стимуляторов.
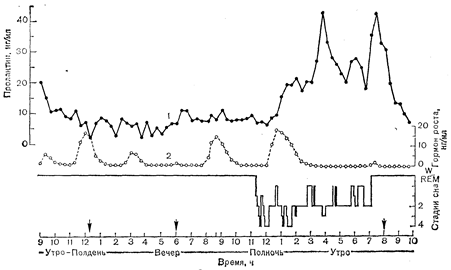
Рис. 7—8. Изменения во время сна секреции пролактина (1) и СТГ (2). Повышение уровня СТГ сопровождает начало медленноволнового сна (ЭЭГ—стадии III и IV), который обычно наступает через 90—120 мин после засыпания. В отличие от этого, кривая секреции пролактина имеет пилообразную форму, причем максимальный уровень регистрируется в конце периода сна или вскоре после пробуждения (Sassin J. и соавт., Science, 1973, 177, 1205). REM — фаза быстрого движения глаз; стрелки указывают на время приема пищи.
Пероральное введение отдельных аминокислот (аргинина, лизина, лейцина и др.), смеси аминокислот или белков стимулирует выброс СТГ. Повышение уровня свободных жирных кислот в плазме, вызываемое путем инфузии жировой эмульсии с гепарином (для активации липопротеиновой липазы), остро подавляет секрецию СТГ. Напротив, быстрое уменьшение содержания свободных жирных кислот стимулирует секрецию СТГ. Механизм действия аминокислот и свободных жирных кислот, равно как и конкретные точки приложения их действия в ЦНС, еще предстоит выяснить.
|
|
|
Гормональная. На секрецию СТГ различными путями влияют многие гормоны. Эстрогены усиливают секреторную реакцию гормона роста на действие многих стимулов, что наблюдается и в отношении пролактина, гонадотропина и ТТГ. Считается, что прогестерон подавляет секрецию СТГ, но доказательства тому весьма ограничены. Реакции СТГ на стимуляцию тормозятся экзогенными глюкокортикоидами, эндогенным гиперкортизолизмом, гипер-и гипотиреозом. Хотя показано, что как стероиды, так и тироксин оказывают свое действие непосредственно на соматотрофы, действие это, по всей вероятности, более сложно и может включать влияния и на гипоталамус, и на образование соматомединов (которое угнетается эстрогенами и глюкокортикоидами) и на другие эффекты СТГ. Сам СТГ по механизму обратной связи оказывает тормозное действие на собственную секрецию, хотя пока не известно, является ли это действие непосредственным или оно опосредовано каким-либо промежуточным веществом (например, соматомедином или одним из субстратов метаболизма). В пользу последней точки зрения свидетельствует существование карликовости Ларона [73], при которой резистентность к действию СТГ (дефект на рецепторном или пострецепторном уровне) сопровождается повышением уровня СТГ в крови.
Некоторые пептидные гормоны (вазопрессин, АКТГ и отдельные его фрагменты, а также a-МСГ) остро повышают секрецию СТГ. В настоящее время их эффект следует считать фармакологическим, который обусловлен, вероятно, взаимодействием этих пептидов с рецепторами СТГ-РФ на соматотрофах. В отличие от этого глюкагон влияет на секрецию СТГ не сразу и его действие, по всей вероятности, опосредуется изменениями углеводного обмена.
Нейротрансмиттеры и нейрофармакологические препараты. Многочисленные данные о нейрохимической медиации секреции СТГ и об эффектах веществ, обладающих нейрофармакологической активностью, подробно рассматриваются в других публикациях [74, 75]. Многочисленные сведения, касающиеся секреции СТГ у человека, можно суммировать следующим образом: независимо от характера действующих факторов их эффекты опосредуются в ЦНС, а конкретнее — в гипоталамусе одним или несколькими нейротрансмиттерами, которые в конце концов обусловливают высвобождение СТГ-РФ или соматостатина. Некоторые существующие в литературе противоречия могут, вероятно, объясняться тем фактом, что эти нейротрансмиттеры высвобождаются локально и что для воспроизведения реакции необходимо возбуждение не одного, а двух или более нейронов с участием не одного, а нескольких нейротрансмиттеров (см. главу 6). Возможно также, что нейротрансмиттер, опосредующий стимулирующую реакцию в одной цепи нейронов, в другой опосредует тормозную реакцию. Имеются указания на роль почти всех классических нейротрансмиттеров (норадреналин, адреналин, дофамин, серотонин и ацетилхолин) в регуляции секреции СТГ. b-Адренергические рецепторы опосредуют, по-видимому, ингибиторные, а a-рецепторы — стимулирующие влияния. Так, b-рецепторные антагонисты (например, пропранолол) усиливают, а a-рецепторные антагонисты (например, фентоламин) подавляют действие различных стимулов. Однако неспецифичность большинства применяемых в.клинике антагонистов рецепторов заставляет с осторожностью относиться к интерпретации отдельных результатов. Дофаминергические рецепторы опосредуют стимулирующие влияния, и такие агенты, как L-дофа (ближайший предшественник дофамина), апоморфин и бромкриптин (агонист дофаминовых рецепторов), стимулируют, тогда как хлорпромазин (аминазин)и пимозид (антагонисты дофаминовых рецепторов) препятствуют реакциям СТГ на многочисленные стимулы. Серотонинергические рецепторы также опосредуют стимулирующие метаболические сигналы, а возможно, и сигналы, обусловливающие секрецию СТГ, связанную со сном, хотя по этому вопросу еще имеются разногласия. В регуляции связанной со сном секреции СТГ участвуют, по-видимому, и холинергические механизмы. Аналоги энкефалина стимулируют секрецию СТГ [76], но роль эндогенных энкефалинов в регуляции секреции этого гормона пока не ясна. Кроме того, имеются данные о стимулирующем влиянии на его секрецию ГАМК-ергических нейронов [77].
|
|
|
ПРОЛАКТИН
Действие
Основной мишенью действия пролактина служит молочная железа, где он в сочетании с другими гормонами стимулирует развитие специфической ткани и лактацию. Пролактин необходим для нормального развития молочных желез у животных многих видов, но у человека его важность в этом отношении пока не установлена. Патологическое увеличение секреции пролактина обычно не сопровождается увеличением размеров молочных желез, а у мужчин гинекомастия развивается на фоне нормального уровня пролактина. Во время беременности пролактин в сочетании с эстрогенами, прогестероном и плацентарным лактогеном и в присутствии инсулина и кортизола обеспечивает дальнейшее развитие молочных желез, что приводит в конце концов к выработке молока. Пролактин специфически стимулирует синтез белков, в том числе лактальбумина, а также жиров и углеводов молока. В интактной ткани молочной железы были найдены и частично охарактеризованы рецепторы пролактина, которые локализуются на альвеолярных поверхностях клеток. Рецепторы пролактина выявлены также в ткани печени и почек, причем пролактин, по-видимому, может увеличивать число своих собственных рецепторов.
Начало лактации после родов обусловлено резким снижением уровня эстрогенов и прогестерона плацентарного происхождения. Действительно, эстрогены, будучи синергистами пролактина в отношении стимуляции развития молочных желез, одновременно являются его антагонистами в отношении влияния на лактацию. Этот феномен служит основой применения эстрогенов для угнетения лактации в послеродовом периоде, а также объясняет частое появление галактореи у женщин с гиперпролактинемией после прекращения приема оральных контрацептивов.
Для поддержания начавшейся лактации требуется непрерывная секреция пролактина. Ее торможение с помощью фармакологических или хирургических средств приводит к прекращению лактации. Секреция пролактина, стимулируемая актом сосания, в течение послеродового периода постепенно снижается до нормального уровня. Однако истинный рефлекс «выброса» молока опосредуется не пролактином, а секрецией окситоцина задней долей гипофиза. Окситоцин вызывает сокращение миоэпителпальных клеток вокруг терминальных ацинарных долек, которые выталкивают содержащееся в них молоко в протоки между дольками.
У крыс пролактин необходим для поддержания секреторной активности желтого тела и поэтому играет роль в сохранении беременности на ее ранних стадиях. У человека этот эффект, по-видимому, не является обязательным, хотя для продукции прогестерона клетками гранулезы человека все же нужны небольшие количества пролактина [78]. Высокий его уровень, напротив, обусловливает прогрессирующее торможение секреции прогестерона. Пролактин вместе с ФСГ и ЛГ присутствует в фолликулярной жидкости, причем есть данные, согласно которым он может блокировать стимулирующее влияние ФСГ на секрецию эстрогенов развивающимся граафовым пузырьком.
Помимо своего влияния на физиологию репродуктивной системы, пролактин у животных некоторых видов оказывает действие на поведение, а также на водно-электролитный обмен, хотя в отношении человека данные о подобных эффектах пока не слишком убедительны. У птиц и мышей пролактин усиливает проявления материнского инстинкта, что играет существенную роль в жизненном цикле этих видов. Хотя у человека повышенный уровень пролактина сопутствует многим психическим ощущениям (см. далее), усиление секреции гормона является, по-видимому, следствием, а не причиной таких ощущений. У млекопитающих некоторых видов пролактин снижает также экскрецию натрия, калия и воды почками и потенцирует эффекты альдостерона и вазопрессина. Попытки обнаружить эти эффекты у человека пока не увенчались успехом.
Метаболические эффекты пролактина у гипофизэктомированных животных напоминают таковые гормона роста и включают стимуляцию синтеза белка, калоригенеза и образования в хряще хондроитинсульфата. Введение овечьего пролактина людям с дефицитом гормона роста вызывает задержку азота, гиперкальциурию, мобилизацию липидов, нарушение толерантности к углеводам и некоторый рост скелета. У больных с гиперпролактинемией можно наблюдать и гиперинсулинемию, свидетельствующую об инсулинорезистентности, которая исчезает после подавления секреции пролактина [79].
Методы определения
Биологические методы. Стимулирующее влияние пролактина на зобный мешок голубей легло в основу биологического определения этого гормона, применявшегося в течение многих лет. Чувствительность биологического определения удалось повысить путем регистрации синтеза лактозы или казеина в молочных железах мышей в середине беременности. Эти методы обеспечили получение многих данных о содержании пролактина в плазме, но впоследствии все же были вытеснены радиоиммунологическими методами.
Радиоиммунологические методы. Уже вскоре после идентификации пролактина человека в качестве отдельного гормона был разработан метод его радиоиммунологического определения с использованием антител к овечьему пролактину, которые дают перекрестную реакцию с гормоном человека [80]. В настоящее время вместо гетерологичных антител в соответствующих методах используют гомологичные антитела к пролактину человека. Специфичность этих методов относительно высока, и сколько-нибудь значительная перекрестная реакция с СТГ или плацентарным лактогеном человека отсутствует.
Радиорецепторные методы. Разработаны также радиолигандные методы определения пролактина, в которых чаще всего используют мембраны молочных желез беременных крольчих [81]. Хотя эти методы достаточно чувствительны для определения уровней пролактина в плазме, надежность их ограничивается тем, что мембраны связывают и СТГ, который вытесняет радиоактивный пролактин. Как и в отношении СТГ, сравнение результатов радиоиммунологического и радиорецепторного определений может помочь различить биологически активный и биологически неактивный пролактин, что имеет существенное значение при некоторых клинических состояниях.
|
|
|


