 |
Транспорт двуокиси углерода. Транспортные формы СО2 крови. Анион бикарбоната. Карбаминовые соединения. Кривая диссоциации СО2-гемоглобин
|
|
|
|
Транспорт двуокиси углерода
[рчнячительное количество СО2. Следовательно,
разделе рассматриваются транспорт СО2, включая многочисленные формы СО2 в крови, и кривая диссоциации СО2.
Транспортные формы СО2 крови
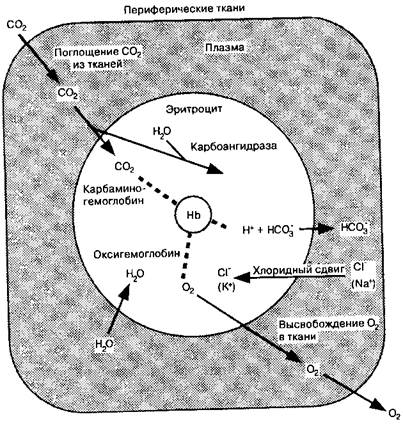
Двуокись углерода легко диффундирует. Ее способность к диффузии в 20 раз превышает таковую у кислорода. По мере образования в процессе клеточного метаболизма СО2 диффундирует в капилляры и транспортируется к легким в трех основных формах: (1) в виде растворенной СО2, (2) в виде аниона бикарбоната и (3) в виде карбаминовых соединений (рис. 10-4).
Растворенная СО2
СО2 очень хорошо растворяется в плазме. Количество растворенной в плазме СО2 определяется произведением ее парциального давления и коэффициента растворимости (а = 0. 3 мл/л крови/мм рт. ст. ). Около 5 % общей двуокиси углерода в артериальной крови находится в форме растворенного газа.
Анион бикарбоната
Эта форма СО2 является преобладающей (90 %) в артериальной крови. Бикар-бонатный анион является продуктом реакции СО2 с водой с образованием Н2С(> { и ее диссоциации на водород и ион бикарбоната:
СО2 + Н2О «~> Н2СО3о Н+ + НСО3". [10-12]
Реакция между СО2и Н2О протекает медленно в плазме и очень быстро в эритроцитах, где присутствует внутриклеточный фермент карбоашидраза. Она облегчает реакцию между СО2 и Н2О с образованием Н2СОЛ; вторая фаза уравнения [ 10 -121 протекает быстро без катализатора.
По мере накопления HCO: i внутри эритроцита анион диффундирует через клеточную мембрану в плазму. Мембрана эритроцита относительно непроницаема для ЬГ, как и вообще для катионов, поэтому ионы водорода остаются внутри клетки. Электрическая нейтральность клетки в процессе диффузии НСО3 в плазму обеспечивается притоком ионов хлора из плазмы в эритроцит, что формирует так называемый хлорид ный сдвиг (рис. 10-4).
|
|
|
Часть FT, остающихся в эритроцитах, забуферивается, соединяясь с гемоглобином. В периферических тканях, где концентрация СО2 высока и значительные количества Нг накапливаются эритроцитами, связывание Н1 облегчается деоксигенаци-ей гемоглобина. Восстановленный гемоглобин лучше связывается с протонами, чем оксигенированный. Таким образом, деоксигенация артериальной крови в периферических тканях способствует связыванию Hf посредством образования восстановленного гемоглобина. Это увеличение связывания СО2 с гемоглобином известно как эффект Холдейна (рис. 10-5).
Карбаминовые соединения
Третьей формой транспорта СО2являются карбаминовые соединения, образованные в реакции СО2 с концевыми аминогруппами белков крови. Основным белком крови, связывающим СО2> является гемоглобин (особенно глобимовая часть молекулы). Этот процесс описывается следующей реакцией:
Hb-NH2 + СО2< -> Hb-NH COOH < -> Hb-NHCOO + Н4 [10-13]
Реакция СО; , с аминогруппами иротекаетбысфо. Как и вслучае бо. чге лп кого
160 _____
Рис. 10-4. С02-
транспорт в крови, иллюстрирующий образование НСО~ и кар-баминовых соединений, хло-ридиый сдвиг и святил ванне Н +. При hoi-лощении О2 и высвобождении СО2 и легочных капиллярах реакции, представленные па схеме, протекают в обратном па-правлении
единений легче протекает с деоксигенированными формами гемоглобина. Карбами-новые соединения составляют около 5 % общего количества СО2, транспортируемого артериальной кровью.
С точки зрения сравнительного вклада каждой из этих форм в артерио-венозную разницу по концентрации СО2, около 60 % принадлежит HCCV, карбаминовым соединениям - около 30 % и растворенной СО2 - около 10 %.
Кривая диссоциации СО2-гемоглобин
|
|
|
Присутствие в крови всех трех форм СО2 создает равновесие между растворенной СО2 (РСО2) и СО2, химически связанной с другими веществами (рис. 10-5).
В отличие от S-образной кривой диссоциации оксигемоглобина, кривая диссоциации СО2-гемоглобина более линейна. Особое физиологическое значение имеет то, что общее содержание СО2 при любом уровне РСО2 зависит от степени оксигена-ции гемоглобина (эффект Холдейна).
По мере того, как в периферических тканях происходит отщепление О2 от гемоглобина, он присоединяет СО2все более активно. Отсюда, общее содержание СО2в крови больше при любом уровне тканевого РСО2. В этом можно убедиться, сравнивая кривые диссоциации СО? для полностью деоксигенированной, полностью окси-генироианной и частично оксигенированной крови с РО2, эквивалентным смешанной венозной крови (рис. 10-6).
о ~.,,.. „„ч, т, 1, ^пг»1; и. 1гп. т аптрпмя лмтй кпови с РаСО? 40 мм рт. ст. содержание СО^
Рис. 10-5. Эффект Холдейна. Связывание СО2 с гемоглобином увеличивается при деоксигепации артериальной крови. Содержание СО2 выше при данном Рассь в деоксигенированной крови
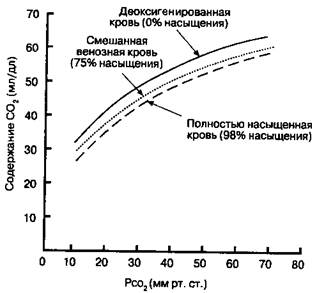
ферических тканях, кровь, прошедшая капилляры, насыщена кислородом на 75 %. При РСО2 около 46 мм рт. ст. содержание СО2 в смешанной венозной крови (т. е. крови, входящей в правый желудочек и представляющей смесь венозной крови от всех тканей тела) составляет приблизительно 530 мл/л (рис. 10-6, точка Б). Повышенное сродство деоксигенированной крови к СО2 объясняет добавочные 20-30 мл СО2/л сверх того, что могло бы быть поглощено без изменения насыщения оксигемоглобина.
|
|
|


