 |
Антикоагулянты прямого действия.
|
|
|
|
Гепарин. Нормальный физиологический антикоагулянт, постоянно присутствующий в сосудах и держащий «в узде» систему свертывания, предупреждая ее включение по случайным или малозначимым поводам, удерживает в рациональных границах времени и масштаба процесс гемокоагуляции. Природный гепарин не является однородным веществом, это — смесь сернокислых эфиров мукополисахаридов разной молекулярной массы (от 2000 до 30 000 Да).
Гепарин вырабатывается преимущественно тучными клетками рыхлой соединительной ткани и базофильными лейкоцитами и может депонироваться в разных органах. В обычном коммерческом гепарине лишь 1/3 молекул обладает антикоагулянтными свойствами, остальные, по существу, — балласт, с которым связаны возможные аллергические реакции. Гепарин выпускают в виде натриевой соли, он подвергается биологической стандартизации, поскольку состав смеси молекул при его получении оказывается весьма различным. Согласно международному стандарту, в 1 мг препарата должно быть 130 ЕД.
В настоящее время предпочтение отдают низкомолекулярным фракциям гепарина (молекулярная масса 2000—6000 Да), которые обладают высокой биодоступностью, более выраженным, стабильным и длительным антикоагулянтным эффектом, дают меньше осложнений, в первую очередь аллергического характера, — эноксапарин натрия (клексан, анфибра), надропарин кальция (фраксипарин), далтепарин натрия (фрагмин) и др. Получают их методом деполимеризации природного гепарина. Выпускают в специальных шприцах-дозаторах разового использования по 0, 2—1 мл с содержанием антикоагулянта 10 тыс. МЕ в 1 мл.
Полисахаридные цепочки гепарина несут на себе множество отрицательных зарядов серной кислоты — это самая сильная органическая кислота из всех известных.
|
|
|
Считают, что в сосудах гепарин покрывает мономолекулярным слоем обращенную в просвет поверхность эндотелия, сообщая ей дополнительный и сильный электроотрицательный заряд, препятствующий адгезии Тц и образованию микротромбов, и что это — еще одна защита от неконтролируемого свертывания крови. Механизм действия гепарина сложен, сам он собственно антикоагулянтным действием не обладает. Функция его состоит в связывании фрагмента молекулы (12—16 сульфатированных моносахаридов в составе цепочки) с белком крови — антитромбином III. Этот специфический белок переходит из неактивной формы в активную и в составе комплекса с гепарином блокирует протеолитическую способность факторов свертывания на разных этапах коагуляционного каскада (см. рис. 2).
Результатами этого являются:
— инактивация Xа, IXа, XIа, XIIа и VIIа активированных факторов свертывания;
— блокирование протеолитической активности тромбина (фактор IIа) и фактора XIII, обеспечивающих превращение фибриногена в фибрин и стабилизацию фибрина.
Однако наиболее сильно инактивируются комплексом антитромбин III — гепарин факторы Xа (низкомолекулярные фракции гепарина) и IIа (высокомолекулярные фракции).
Наиболее надежно гепарин подавляет свертывание крови в венах. Он предупреждает как локальное образование тромбов, так и диссеминированное внутрисосудистое свертывание.
Гепарин является наиболее надежным и действующим очень быстро антикоагулянтом. После однократного введения в вену эффект развивается почти сразу и продолжается 8—12 ч.
Эноксапарин и фраксипарин вводят подкожно, причем оптимальной областью инъекции считают подкожную клетчатку передней стенки живота (кожную складку оттягивают двумя пальцами и держат до конца введения, иглу направляют перпендикулярно), при этом эффект продолжается до 18 ч, а пик действия (максимальная концентрация в крови) достигается через 3 ч после инъекции. Эти препараты достаточно вводить 1—2 раза в сутки.
|
|
|
Гепарин натрия применяют в острых случаях внутривенно по 15—20 тыс. ЕД (острый инфаркт миокарда), а в критических ситуациях (тромбоэмболия легочной артерии) — 40—60 тыс. ЕД; затем переходят на подкожное введение по 5—10 тыс. ЕД каждые 4 ч. Первые порции гепарина могут вливаться и капельно. Считают, что минимальная доза гепарина, проявляющая антикоагулянтный эффект, составляет 35 ЕД/кг. За один-два дня до отмены гепарина суточную дозу постепенно снижают на 2500—5000 ЕД при каждой инъекции, без увеличения интервалов между введениями. Это предупреждает возможную реакцию отдачи в виде гиперкоагуляции при внезапной отмене препарата.
Показаниями для применения гепарина являются:
1) тромбоз коронарных сосудов, осложненный инфарктом миокарда;
2) тромбофлебиты; профилактика тромбоэмболий у больных с эмболиями в анамнезе при операциях и в ближайшем послеоперационном периоде;
3) большие ортопедические операции; операции на сердце и сосудах — профилактически за 1—2 ч до операции, затем каждые 8—12 ч в течение периода иммобилизации, как правило, не менее 7 дней;
4) операции гемодиализа и при экстракорпоральном кровообращении;
5) тромбофлебиты поверхностных вен ног — гепарин в форме мази, наносимой дважды в сутки под хорошо перфорированное покрытие из полиэтилена и нетугое бинтование.
При применении гепаринов с профилактической целью особое значение придается его воздействию на фактор Xа, инактивация которого имеет ключевое значение, так как дальше начинается ускоряющийся процесс гемокоагуляции на каждом из последующих этапов. Этот фермент, к счастью, проявляет особую чувствительность к комплексу гепарин — антитромбин III и блокируется относительно малыми дозами антикоагулянта. Как отмечалось, особенно активны в отношении его низкомолекулярные фракции препарата. Средством выбора для профилактической терапии является эноксапарин 100 МЕ/кг (1 мг/кг) 1—2 раза в сутки или надропарин кальция 86 МЕ/кг 2 раза в сутки.
Оптимальным и обязательным критерием достаточности (и отсутствия избыточности) антикоагулянтного действия гепарина, эноксапарина и фраксипарина является активированное (частичное или парциальное) тромбопластиновое время (АЧТВ), которое рекомендуется поддерживать на уровне, превосходящем норму в 1, 5—2, 5 раза, в зависимости от состояния больного и цели применения.
|
|
|
Осложнения при использовании гепарина. Основное и наиболее тревожное — кровотечения, обусловленные недостаточно обоснованным дозированием, плохим гемостазом в ходе операции и другими трудно прогнозируемыми причинами. В качестве антидота гепарина используют полипептид с положительным зарядом, который связывает в крови заряженные отрицательно молекулы гепарина, — протамина сульфат. Он выпускается специально для этой цели в ампулах и должен быть под рукой при лечении гепарином, эноксапарином, фраксипарином. Применяют его из расчета 1 мг протамина на 1 мг введенного ранее гепарина (порядка 130 ЕД). Действие антидота проявляется сразу и продолжается примерно 2 ч. Обычно начальные дозы составляют 50 мг, при продолжающемся кровотечении введение повторяют в той же дозе, но не превышая максимальную дозу в 150 мг в течение 1 ч. Суточные дозы определены в 5—8 мг/кг не менее чем в 2 приема с интервалом (интервалами) в 6 ч. Контроль за АЧТВ обязателен.
Кровотечения как осложнение гепаринотерапии чаще наблюдаются у женщин и больных с почечной недостаточностью. Эноксапарин и фраксипарин реже вызывают это осложнение. Из других побочных эффектов следует иметь в виду преходящую тромбоцитопению (у 25 % больных) и ее тяжелую форму (у 5 %). К гепарину, реже — к его низкомолекулярным фракциям, может наблюдаться повышенная чувствительность. Поэтому препараты должны осторожно назначаться больным с аллергической настроенностью. У лиц с генетически обусловленным дефицитом антитромбина III препараты не оказывают антикоагулянтного эффекта.
Противопоказания. Гепарин противопоказан больным с кровотечениями, геморрагическими диатезами, гемофилией, тромбоцитопенией, тяжелой гипертонией, геморрагическими инсультами, инфекционным эндокардитом, активным туберкулезом, язвенной болезнью. Беременным его назначают только по жизненным показаниям. Низкомолекулярные фракции противопоказаны беременным, особенно в I триместре.
|
|
|
Гирудин, бивалирудин (ангиокс). Протеолитический фермент слюнных желез пиявок гирудин обладает уникальной способностью специфически ингибировать только активированный тромбин (фактор IIа), в том числе в тромбах. Его действие не зависит от наличия антитромбина III. Медицинские пиявки применяются с глубокой древности для лечения поверхностных тромбофлебитов вен нижней конечности. Получение гирудина из естественных источников в ощутимых количествах нереально; сейчас синтетическим путем получают полипептидный аналог гирудина — бивалирудин (ангиокс). Он вошел в медицинскую практику как альтернатива гепарину при операциях на сердце и сосудах, а также в случаях тромбоцитопении, вызванной гепарином. Вводят препарат внутривенно. По-прежнему в медицине пользуются пиявками (гирудотерапия). Интерес к гирудотерапии возрос в связи с открывшейся возможностью использования противовоспалительных, рассасывающих свойств биологически активных ферментов пиявок помимо гирудина.
Дабигатрана этексилат (прадакса) — антикоагулянт прямого действия, предназначенный для перорального применения. Непосредственно ингибирует тромбин (фактор IIa) и препятствует превращению фибриногена в фибрин. Является пролекарством, в плазме крови быстро гидролизуется и превращается в активное вещество дабигатран. Применяется для профилактики тромбоэмболических осложнений (тромбоэмболии легочной артерии, инсульта и др. ) при фибрилляции предсердий и после операций на тазобедренном суставе в качестве альтернативы антикоагулянту непрямого действия варфарину. Назначается внутрь в капсулах по 150 мг 2 раза в сутки. Удлиняет время свертывания крови (АЧТВ), регулярного контроля показателей свертываемости крови не требует.
Побочные эффекты: кровотечение, тошнота, рвота, диарея, повышение активности трансаминаз и уровня билирубина в плазме крови.
Ривароксабан (ксарелто) — антикоагулянт прямого действия для перорального применения. Селективно ингибирует фактор свертывания крови Xа и тормозит переход протромбина в тромбин. Применяется для профилактики инсульта и артериальных тромбоэмболий при фибрилляции предсердий и после ортопедических операций; лечения венозного тромбоза и тромбоэмболий. По эффективности и безопасности применения превосходит низкомолекулярные гепарины.
Назначают для профилактики тромбоэмболических осложнений внутрь в таблетках по 20 мг 1 раз в сутки, для лечения тромбоза и тромбоэмболий — по 15 мг 2 раза в сутки. Не требует контроля показателей свертываемости крови.
|
|
|
Побочные эффекты: может вызывать кровотечение, тошноту, реже головную боль, желтуху.
Натрия цитратиспользуется практически только для консервирования крови. Цитратный анион связывает в труднодиссоциирующую соль ионы кальция, выводя из реакций этот необходимый участник гемокоагуляции. В консервированной крови цитрат находится в некотором (гарантирующем) избытке, поэтому при массивных гемотрансфузиях он начинает ощутимо связывать также ионы кальция собственной крови больного. В результате нарушаются не только свертываемость крови, но и другие кальцийзависимые процессы, в том числе снижаются сократимость миокарда, сосудистый тонус. Для предупреждения и лечения этих осложнений гемотрансфузии целесообразно компенсировать сдвиги внутривенным введением небольших количеств раствора кальция хлорида.
Антикоагулянты непрямого действия. К ним относят синтетические вещества — производные кумарина — варфарин, аценокумарол (синкумар) — и индандиона — фениндион (фенилин). Их называют также антагонистами витамина К. Механизм противосвертывающего действия состоит в ингибировании фермента печени эпоксид-редуктазы, необходимого для образования активной формы витамина К — гидрохинона. Витамин К-гидрохинон активирует в печени карбоксилазу — фермент, осуществляющий карбоксилирование (включение СО2) нескольких остатков глутаминовой кислоты белков синтезируемых факторов свертывания II, VII, IX, X. При этом сам витамин К переходит в неактивную форму — эпоксида. Антикоагулянты этой группы выступают в качестве конкурентных антагонистов витамина К, они исключают его участие в циклической реакции (блокируют его реактивацию в этом процессе). Функция фермента карбоксилазы становится невозможной. В результате образуются неполноценные факторы, не способные участвовать в коагуляционном каскаде. В первую очередь проявляется торможение синтеза факторов VII и IX, в последующем — II и X, т. е. раньше и сильнее страдает образование активного тромбопластина, запускающего каскад, затем уже ключевого фактора X и протромбина.
В соответствии с механизмом действия непрямые антикоагулянты эффективны только в организме. Препараты действуют не сразу, поскольку в крови факторы свертывания уже есть, причем элиминируются они довольно медленно (например, Т1/2 фактора VII составляет 6 ч, а протромбина — 60 ч). Латентный период у разных препаратов составляет 24—72 ч, зато эффект сохраняется в течение нескольких суток. Непрямые антикоагулянты хорошо и почти полностью всасываются в ЖКТ, в плазме крови значительная доля их связывается альбуминами. В печени они подвергаются биотрансформации (меньше всего — аценокумарол) и выделяются с мочой. Они хорошо проникают через плацентарный барьер и могут вызвать кровоизлияние у плода, в связи с чем противопоказаны при беременности и кормлении. Вследствие длительного действия и относительно медленной элиминации при лечении данными средствами (чаще применяется варфарин) легко развивается функциональная и материальная кумуляция, что требует осторожного дозирования как в начале лечения, так и при поддержании эффекта, а также контроля за свертыванием крови.
Критерием степени антикоагуляционного эффекта служит протромбиновое время (время свертывания плазмы крови в секундах), определяемое по Квику.
Время кровотечения — критерий для гепарина — под влиянием непрямых антикоагулянтов не изменяется. Задача состоит в том, чтобы осторожно увеличить продолжительность протромбинового временени в 2—3 раза (до 25—30 % нормы) и удерживать его на этом уровне в течение всего курса терапии (иногда — годами). Это достигается индивидуальным дозированием под контролем АЧТВ. Последнее определяют ежедневно в первые дни терапии, затем 1—2 раза в неделю. После достижения нужного плато и надежного удержания на нем — 1 раз в месяц или в несколько месяцев, по усмотрению лечащего врача. Для более определенного количественного обозначения эффекта по предложению ВОЗ рекомендовано стандартизировать метод и оценивать состояние свертывания крови с использованием международного индекса чувствительности (МИЧ) тромбопластина, а протромбиновый тест выражать в показателе международного нормализованного отношения (МНО). Такое исследование, а также подбор и корректировку доз варфарина проводит специалист-гематолог.
В неотложных ситуациях (тромбоэмболии, инфаркт миокарда, ишемический инсульт и др. ) антикоагулянты непрямого действия по быстроте, надежности и управляемости эффектом сильно уступают гепарину. Их место в антикоагуляционной терапии — предупреждение тромбообразования при хронической патологии.
Основными показаниями к назначению являются:
— лечение тромбофлебитов, предупреждение тромбоэмболий;
— профилактика тромбоза коронарных и мозговых артерий, в том числе у лиц, перенесших инфаркт или инсульт;
— профилактика тромбозов после пластики сосудов, сердечных клапанов, после других сложных операций на сердце и сосудах в порядке замены антикоагулянтов прямого действия, применяемых в остром периоде, и перехода на длительное лечение;
— профилактика тромбозов и тромбоэмболий при ревматических пороках сердца.
Противопоказания к применению непрямых антикоагулянтов те же, что и для гепарина. Их нельзя назначать параллельно с гепарином и с осторожностью назначать (под гематологическим контролем) совместно с антиагрегантами. Недостаточность жирорастворимого витамина K (в пище, при заболеваниях печени) также служит противопоказанием, как и выраженная недостаточность функций печени и почек. Следует иметь в виду, что антикоагулянты непрямого действия вступают в сложное фармакокинетическое взаимодействие со многими лекарственными средствами. Это требует осторожности и корректировки доз при совместном их применении (подробности обычно приводятся в инструкциях).
Побочные эффекты: кровотечение, диарея, нарушение функции печени, аллергические реакции, редко некроз кожи. При проведении лечения, кроме периодического определения протромбинового времени, необходимо следить за возможным появлением эритроцитов в моче, кровоточивостью десен (при чистке зубов), кровотечениями из носа, кровоизлияниями в подкожную клетчатку при легких ушибах, сдавлениях; за другими проявлениями геморрагического диатеза. Для остановки кровотечений следует вводить водорастворимый аналог витамина К1 — менадиона натрия бисульфит (викасол, витамин К3), комплекс витамин К-зависимых факторов свертывания (протромплекс 600), содержащий II, VII, IX и X факторы.
Серьезным аргументом в пользу назначения антикоагулянтов непрямого действия является высокий уровень протромбина и фибриногена в крови.
ФИБРИНОЛИТИЧЕСКИЕ СРЕДСТВА
Вещества естественной природы, прямо участвующие в лизисе свежеобразованного тромба или активирующие плазминоген крови.
Фибринолитическая система предназначена для предохранения (вместе с другими антифакторами) от внутрисосудистого свертывания крови, ограничения процесса тромбоза и восстановления проходимости сосуда, после того как кровотечение прекратилось. Основной участник процесса — плазмин, или фибринолизин (термины равнозначны), — постоянно присутствует в крови в неактивной форме, но под влиянием активаторов переходит в активный протеолитический фермент, для чего от плазминогена нужно отщепить фрагмент и открыть его активный центр. Такое же действие могут оказывать и другие протеолитические ферменты — трипсин, химотрипсин, урокиназа, фермент стрептококков стрептокиназа (рис. 3).
Протеолитическое действие фибринолизина проявляется в лизисе свежеобразованных нитей фибрина в формирующемся тромбе до растворимых фрагментов. Продукты деградации фибрина тормозят полимеризацию его мономеров и образование тромбопластина. Фибринолизин оказывает рассасывающее действие только на свежие тромбы до ретракции (сжатия) фибрина.
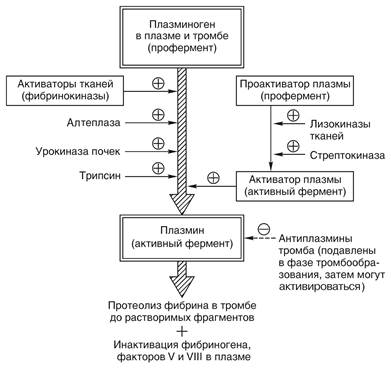
Рис. 3. Схема активации системы плазмина (фибринолизина) с растворением фибрина и реканализацией сосуда
Фибринолизин (плазмин). В виде профермента получают из плацентарной крови и переводят в активную форму с помощью трипсина. Применение его в качестве средства профилактики и лечения тромбозов сейчас почти везде остановлено в связи со слишком широким (не только в месте тромбоза) системным действием и большим числом побочных реакций. Местное же использование в рассасывающих глазных пленках и для очищения раневой поверхности от нежизнеспособных некротических тканей, являющихся питательной средой для микроорганизмов, продолжается.
Активаторы плазминогена. Именно они в настоящее время рассматриваются в качестве основных средств проведения фибринолитической терапии. Для этой цели предложены и используются алтеплаза (актилизе), тенектеплаза (метализе), урокиназа, проурокиназа (пуролаза), стрептокиназа.
Наибольшие надежды связывают с естественным тканевым активатором плазминогена (t-PA), который освобождается в основном эндотелием сосудов в месте образования тромба. Он переводит профермент в активный плазмин в самом формирующем тромбе, т. е. в том месте, где это и необходимо. Этот фактор получают методом генной инженерии и выпускают в виде препаратов алтеплазы и тенектеплазы. Предполагалось, что препарат не будет приводить к системной активации профермента и риск осложнений сведется к минимуму. Нельзя сказать, что эти надежды полностью оправдались, хотя частота геморрагических осложнений и аллергических реакций по сравнению с другими активаторами, тем более фибринолизином, все же меньше. Тенектеплаза обладает большей избирательностью действия на фибрин тромба, устойчива к ингибиторам активатора плазминогена, действует более продолжительно.
Урокиназа образуется в почках, по-видимому, для предупреждения тромбообразования в сосудах почечных клубочков при сгущении крови после фильтрации ее жидкой части. В очень небольших количествах она выделяется с мочой (получают из культуры клеток почек человека). В крови оказывает прямое активирующее действие на плазминоген, не обладает фибриноспецифичностью. Проурокиназа (предшественник урокиназы) — рекомбинантный препарат, обладает большей избирательностью по отношению к фибрину тромба. Таким же действием обладает фермент стрептокиназа, полученный из культуры бета-гемолитического стрептококка. Препарат стрептокиназы в 5—10 раз дешевле других активаторов плазминогена. Вводятся все активаторы плазминогена внутривенно капельно, но оптимальным считают инъекцию через катетер в область локализации тромба, если это технически доступно. Дозируются урокиназа, проурокиназа и стрептокиназа в ЕД, алтеплаза и тенектеплаза — в мг. Определение конкретных показаний, дозировки и само применение осуществляют специалисты-кардиологи или опытные реаниматологи.
Показаниями к применению активаторов плазминогена являются:
— инфаркт миокарда в острой фазе (в составе комплексной терапии);
— острая и рецидивирующая эмболия легочной артерии и ее ветвей;
— осуществление реканализации артериовенозных шунтов, других пересаженных сосудов, протезов;
— тромбоз и эмболия периферических артерий, тромбоз глубоких вен (таза, конечностей);
— в офтальмологии (местное применение) — тромбоз центральных вен сетчатки, завершившееся кровоизлияние в переднюю камеру глаза, стекловидное тело.
Тромболитическая терапия эффективна лишь в фазу формирования тромба до завершения полимеризации фибрина и ретракции сгустка. Применительно к инфаркту миокарда включает период от 30 мин до 6 ч после появления симптомов; менее надежно, но возможно положительное действие и в интервале между 6 и 12 ч. Примерно такие же сроки эффективности тромболитической терапии и по другим показаниям. Результаты в целом оценивают достаточно высоко, причем для нее не усматривают возрастных границ. Вместе с тем это неотложная терапия, которая должна выполняться врачом высокой и специальной квалификации.
После ее окончания показано применение гепарина с последующим переходом на непрямые антикоагулянты.
Осложнения тромболитической терапии могут быть серьезными. Прежде всего это кровотечения, нередко скрытые, наиболее опасные — внутричерепные (порядка 0, 5 % случаев). При использовании стрептокиназы — частые аллергические реакции (гиперемия, сыпь, лихорадка, диарея, боли в животе, позвоночнике, бронхоспазм, редко — анафилактический шок), острая гипотензия (до 10 % случаев). Урокиназа и проурокиназа не обладают антигенными свойствами, они невелики у алтеплазы и тенектеплазы. Иногда возникают так называемые реперфузионные аритмии при инфаркте и восстановлении кровотока в ранее тромбированном сосуде.
Основными противопоказаниями к тромболитической терапии являются: инсульт в предшествующие 2 мес., нейрохирургические операции и травмы черепа в течение последних 6 нед., активное или недавнее кровотечение разной локализации, выраженная гипертензия (АД выше 180/110 мм рт. ст. ), артериовенозные дефекты и аневризмы, серьезные операции, биопсии, травмы в последние 2 нед., мерцание предсердий при митральном пороке, активный туберкулез, первая половина беременности, менструация.
|
|
|


