 |
Максимально допустимые количества жидкости (мл) для некоторых видов лабораторных животных в зависимости от пути введения
|
|
|
|
| Вид животного | Вес, г | Пути введения | ||||
| В желудок | Под кожу | В/м | В/в | В/б | ||
| Мышь | 20-24 25-30 >30 | 0,5 0,8 1,0 | 1,0 | 0,5 | 0,2-0,5 | 1,0 |
| Крыса | 100-190 200-240 250-300 >300 | 3,0 4,0-5,0 6,0 8,0 | 10,5 | 5,0 | 2,0 | 5,0 |
| Морская свинка | 250-300 >300 | 4,0-5,0 6,0 | 15,0 | 5,0 | 5,0-8,0 | 5,0 |
| Кролик | 2000-2400 2500-3000 >3000 | 100,0 150,0 200,0 | 30,0 | 15,0 | 20,0 | 20,0-30,0 |
При исследовании острой токсичности образцов биологически активных химических соединений наблюдение за животными осуществляют в течение 6 часов непрерывно, затем – периодически, не менее чем в течение 3-х суток. Сроки наблюдения могут быть увеличены, в зависимости от особенностей механизмов действия исследуемых веществ и конкретных целей задач исследования.
При исследовании подострой токсичности образцов биологически активных химических соединений продолжительность наблюдения составляет 28 суток.
В период непрерывного наблюдения у подопытных животных с точностью до минуты регистрируется время проявления основных симптомов интоксикации. После окончания срока наблюдения группы подопытных животных расформировываются. Выживших животных по окончанию эксперимента, как правило, подвергают эвтаназии.
Оцениваемыми токсикометрическими показателями биологически активных химических соединений являются:
медианно-эффективные (ЕD50), минимально-эффективные (ЕD5) и максимально-эффективные (ЕD95) дозы вызывающие регистрируемый целевой токсический эффект у подопытных животных при конкретном виде аппликации;
быстродействие (Δts) – время проявления регистрируемого целевого эффекта при воздействии биологически активных химических соединений в медианно-эффективной дозе, выраженное в минутах (часах).
|
|
|
При регистрации гибели животных во время испытания подострой токсичности рассчитывают индекс кумуляции – отношение величины медианно-смертельной дозы (LD50) при однократном введении к суммарной величине LD50 при повторных введениях.
Расчёт медианно-эффективных доз (токсодоз) образцов исследуемого вещества для грызунов и зайцеобразных выполняют методом пробит-анализа. Для собак и других крупных животных допустимо применение экспресс-методов.
Для характеристики безопасности применения образцов биологически активных химических соединений рассчитывают широту токсического действия (ШТД) в соответствии с формулой (1):
 (1)
(1)
и индекс Брокка-Шнайдера в соответствии с формулой (2):
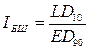 (2)
(2)
В ходе наблюдения за подопытными животными после воздействия изучаемых образцов биологически активных химических соединений определяют параметры зависимости «доза-время-эффект», регистрируют продолжительность целевого эффекта и клинические особенности проявления токсического процесса.
Исследование специфической активности биологически активных химических соединений проводят с использованием комплекса методик, позволяющих всесторонне оценить выраженность, скорость формирования и продолжительность целевого эффекта в зависимости от дозы (токсодозы) введенного вещества, а также соотнести уровни различных категорий токсодоз. Перечень применяемых методик определяется исходя из необходимости оценки характера и выраженности целевого эффекта.
Все павшие в течение периода наблюдения животные подлежат вскрытию с морфо-гистологическим описанием изменений состояния внутренних органов.
При оценке специфической активности антидотов регистрируются и рассчитываются следующие показатели:
─ коэффициент защиты – отношение медианно-эффективной дозы химического соединения по целевому эффекту без применения антидота к медианно-эффективной дозе на фоне применения антидота;
|
|
|
─ антидотная мощность – отношение максимально-эффективной дозы химического соединений по целевому эффекту без применения антидота к медианно-эффективной дозе на фоне применения антидота;
─ индекс гарантированной защиты – отношение количества максимально-эффективных доз химического соединения по целевому эффекту без применения антидота к минимально-эффективной дозе на фоне применения антидота.
Наряду с выраженностью специфической активности антидотов оценивают:
─ время наступления защитного эффекта и его продолжительность;
─ спектр антидотной эффективности (универсальность), характеризующий групповую специфичность антидота;
─ полноту защитного действия, характеризующую способность антидота купировать максимальное количество морфофункциональных изменений при интоксикациях.
При исследовании фармакокинетики образцов биологически активных химических соединений у животных отбирают пробы биоматериала в сроки, позволяющие фиксировать: не менее трех точек, приходящихся на фазу нарастания концентрации; не менее трех точек, описывающих пик концентрации; не менее пяти точек, характеризующих фазу снижения концентрации исследуемого вещества вплоть до регистрации следовых количеств. На основании экспериментального материала рассчитывают следующие показатели:
b – постоянная убывания на хвосте распределения (мин);
Сmax – максимальная концентрация (мкг/мл);
AUC – полная площадь под кривой (мин мкг/мл);
Сmax/AUC – скорость всасывания (мин-1);
MRT – среднее время удерживания (мин);
Vo – центральный объем распределения (мл/кг);
Сl – общий клиренс (мл/мин/кг);
V – стационарный объем распределения (мл/кг);
Тэфф – эффективная длительность процесса (мин).
Протокол эксперимента. Все результаты экспериментов протоколируют в соответствии с требованиями Приказа Министра здравоохранения РФ от 19 июня 2003 года № 267.
|
|
|


