 |
Приготовление рабочего титрованного раствора трилона Б
|
|
|
|
11.3.1 Рассчитать навеску кристаллогидрата двунатриевой соли этилендиаминтетрауксусной кислоты Na2C10H14N2O8 · 2H2O, необходимую для приготовления 100 мл раствора с молярной концентрацией эквивалента 0,05 моль/л.
11.3.2 Взять навеску кристаллогидрата трилона Б на аналитических весах, соблюдая правила взвешивания и ведя соответствующую запись.
11.3.3 Перенести навеску в мерную колбу на 100,0 мл, соблюдая правила перенесения, растворить в небольшом объёме воды, довести объём раствора до метки и тщательно перемещать.
11.3.4 Рассчитать титр и молярную концентрацию эквивалента приготовленного рабочего раствора трилона Б.
11.4 Ход определения общей жесткости воды
11.4.1 Подготовить бюретку к титрованию, промыть её дистиллированной водой и небольшим объёмом рабочего раствора трилона Б.
11.4.2 Отмерить цилиндром в колбу для титрования 100 мл водопроводной воды, прилить 5,0 мл аммонийной буферной смеси для создания щелочной среды (рН = 10), прибавить по каплям раствор индикатора (хромогена чёрного) до появления хорошо заметной, но не очень тёмной розово-красной окраски.
11.4.3 Оттитровать воду рабочим раствором трилона Б до перехода розово-красной окраски. 
11.4.4 Повторить титрование трижды, фиксируя затраченные объёмы рабочего раствора V1, V2, V3; вычислить средний объём.
11.4.5 Вычислить суммарную молярную концентрацию эквивалента ионов Са2+ и Mg2+ в анализируемой воде.
11.4.6 Перевести молярную концентрацию эквивалента ионов Са2+ и Mg2+ в миллимолярную концентрацию эквивалента. Это и будет жёсткость воды.
11.4.7 Полученный результат с точностью до сотых долей записать на доске, а к себе в тетрадь занести результаты определения жёсткости воды студентами всей группы. Вычислить средний результат. Сделать вывод о жёсткости анализируемой воды.
|
|
|
Расчётные формулы:
1)  ;
;
2) 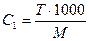 ;
;
3)  ;
;
где С1 = С (Na2C10H14N2O8 · 2H2O)
С2 = С (½Са2+ + ½ Mg2+), моль/л
Жесткость = С2 · 1000, ммоль/л
12 Лабораторная работа № 11
Определение зольности пищевых кислот
Ряд пищевых кислот, в том числе лимонную, молочную, винно-каменную, аскорбиновую и другие, используют в производстве безалкогольных напитков. Аскорбиновую кислоту применяют для витаминизации, молочную – при приготовлении кваса, винно-каменную – для сухих шипучих и нешипучих порошкообразных смесей, сорбиновую – для повышения стойкости напитков, поскольку она тормозит развитие дрожжей и грибков.
Экспериментальная часть.
Приборы и посуда: аналитические весы, тигли, муфельная печь.
Реактивы: пищевая кислота, раствор нитрата аммония (NH4NO3), 10 %.
Ход выполнения.
В фарфоровый тигель, прокаленный до постоянной массы, вносят кислоту (2-3г), взвешивают на аналитических весах. Ставят в муфельную печь, осторожно прогревая тигель. Затем поставить в среднюю часть муфеля, прокаливают в течение часа. Вынимают тигель, немного охлаждают и содержимое смачивают 2 – 3 каплями раствора нитрата аммония, после чего продолжают прокаливание ещё минут 10 – 15. Охлаждают в эксикаторе до комнатной температуры, взвешивают, записав массу (m3’) прокаливание тигля в течение 5 – 10 минут повторяют до постоянной массы, каждый раз охлаждая в эксикаторе.
Результаты записывают в таблицу.
Таблица 3 - Результаты взвешивания тигля в ходе анализа
| Показания | Обозначение | Результаты взвешивания | |
| Масса пустого тигля | m1 | ||
| Масса тигля с навеской | m2 | ||
| Масса тигля с золой | Результаты последовательного взвешивания до | m3´ | |
| m3´´ | |||
| m3´´´ | |||
| постоянной массы | m3 |
Содержание золы вычисляется по формуле:
ω(золы) = (m3 – m1)·100/ (m2 - m1)
|
|
|
Содержание золы в сухой кислоте не должно превышать 0,35%.
13 Лабораторная работа № 12
|
|
|


