 |
Контрольные вопросы. Химический анализ ЛРС,
|
|
|
|
КОНТРОЛЬНЫЕ ВОПРОСЫ
1. Дайте определение понятия «ксантоны».
2. Приведите классификацию ксантонов.
3. Охарактеризуйте физико-химические свойства ксантонов.
4. Напишите формулу мангиферина и укажите его биологическое действие.
5. Перечислите качественные реакции на ксантоны.
6. Назовите семейства и лекарственные растения, наиболее богатые ксантонами. Приведите их латинские названия.
7. Перечислите препараты на основе ксантонов и их применение.
8. Дайте определение понятия «лигнаны».
9. Приведите классификацию лигнанов.
10. Охарактеризуйте физико-химические свойства лигнанов.
11. Перечислите семейства и лекарственные растения, наиболее бога-тые лигнанами. Приведите их латинские названия.
12. Идентифицируйте по гербарному образцу одно из лекарственных растений: золототысячник малый, расторопша пятнистая, элеутеро-кокк колючий, лимонник китайский, подофилл щитовидный.
13. Укажите сроки заготовки и особенности сушки сырья золототысяч-ника малого, расторопши пятнистой, элеутерококка колючего, ли-монника китайского, подофилла щитовидного.
14. Расскажите о путях и способах использования сырья золототысяч-ника малого, расторопши пятнистой, элеутерококка колючего, ли-монника китайского, подофилла щитовидного.
15. Назовите отечественные препараты на основе флаволигнанов и при-ведите их зарубежные аналоги.















 ТЕМА
ТЕМА
8 Флавоноиды
Флавоноиды — это растительные ароматические соединения, производные дифенилпропана (С6—С3—С6) различной степени окисленно-сти и замещения. Флавоноиды можно рассматривать как производные хрома-на и хромона, содержащие в положении 2, 3 или 4 арильный радикал.
|
|
|
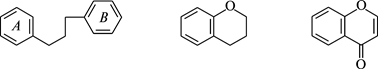
дифенилпропан хроман хромон
Классификация флавоноидов основана на ряде признаков, таких как сте-пень окисленности пропанового фрагмента, положение бокового фенильно-го радикала, величина гетероцикла и др. По расположению кольца В выделя-ют собственно флавоноиды (эуфлавоноиды), изо- и неофлавоноиды.

флаван изофлаван
неофлаван
Кроме мономерных флавоноидов существуют димерные формы (напри-мер, бифлавоноиды Ginkgo biloba). Флавоноиды могут конденсироваться между собой и другими фенольными соединениями: фенолкарбоновыми
и оксикоричными кислотами, лигнанами, а также с изопреноидами и алка-лоидами.
В растениях флавоноиды встречаются преимущественно в виде гликози-дов, реже — в виде агликонов. Многообразие флавоноидных гликозидов обу-словлено значительным набором сахаров и местом присоединения их к агли-кону, а также тем, что сахара могут иметь различную величину и конфигура-цию циклов и гликозидных связей (фуранозная и пиранозная формы моносахаридов, D- и L-изомеры, α - или β -связь), порядок и сочетание саха-ров и связей.
По типу связи различают О- и С-гликозиды флавоноидов. О-гликозиды легко гидролизуются кислотами и ферментами. С-гликозиды не гидролизуют-ся ферментами и разбавленными кислотами, их гидролиз осуществляется сме-сью Килиани (хлористоводородная концентрированная и уксусная кислоты).
1 2 6 Фенольные соединения. Тема 8. Флавоноиды




Рис. 8. 1.
Физико-химические свойства. Флавоноиды (от лат. flavus — желтый) — кри-сталлические оптически активные вещества, имеющие окраску от белой до желто-оранжевой в зависимости от структуры. Например, флаваноны, изо-флавоны — бесцветные, флавоны и флавонолы — желтые, халконы и ауро-ны имеют цвет от ярко-желтого до красно-оранжевого. Антоцианы окраше-ны в красный или синий цвет в зависимости от рН среды.
|
|
|
Флавоноиды лишены запаха, некоторые из них имеют горький вкус. Са-мым горьким является нарингенин, который в 5 раз более горький, чем хи-нина гидрохлорид.
Агликоны хорошо растворяются в диэтиловом эфире, ацетоне и спиртах, почти не растворяются в бензоле и хлороформе. Флавоноидные гликозиды растворяются в спиртах и спирто-водных смесях. Монозиды лучше раствори-мы в крепком спирте, дигликозиды — в 50 %-ном спирте, гликозиды с тре-мя и более сахарами — в слабом спирте и даже в воде.
Выделение. Для выделения флавоноидов используют последовательную экстракцию сырья рядом органических растворителей с возрастающей по-лярностью: хлороформ, ацетон, спирт и спирто-водные смеси.
Для качественных реакций используют извлечение, очищенное от сопут-ствующих липофильных веществ.
Качественные реакции. Общей реакции, специфической для всех классов флавоноидов, не существует.
Наиболее часто для обнаружения флавоноидов в ЛРС применяют циани-диновую реакцию (проба Snoda). Реакция основана на восстановлении флаво-ноидов атомарным водородом в кислой среде до антоцианидинов с образо-ванием ярко-розового окрашивания.
| Общие сведения | 1 2 7 | |

Цианидиновую реакцию не дают халконы, ауроны, катехины, но они могут образовывать в кислой среде окрашенные оксониевые соли.
Цианидиновая реакция по Брианту позволяет определить агликоновую или гликозидную природу исследуемого вещества. К окрашенному раствору про-дукта цианидиновой реакции прибавляют равный объем н-октанола и встря-хивают. Гликозиды остаются в воде, а агликоны переходят в слой органиче-ского растворителя.
С раствором щелочи флавоны, флавонолы, флаваноны приобретают жел-тое окрашивание, халконы и ауроны — желто-оранжевое, оранжево-красное.
С железа (III) хлоридом образуются окраски от зеленой (флавонолы) до ко-ричневой (флаваноны, халконы, ауроны) и красновато-бурой (флавоны).
|
|
|
Флавоны, халконы, ауроны, содержащие свободные орто-гидроксиль-ные группы в кольце В, при обработке спиртовых растворов свинца ацета-том средним образуют осадки, окрашенные в ярко-желтый или красный цвета. Антоцианы образуют осадки, окрашенные как в красный, так и в си-ний цвет.
Флавоноиды вступают в реакцию комп-лексообразования с 5 %-ным спиртовым ра-створом алюминия хлорида, с 2 %-ным спир-товым раствором циркония (III) хлорида. Фла-воноиды, имеющие две оксигруппы у С-3 и С-5, дают хелаты желтого цвета за счет образования водородных связей между кар-бонильной и гидроксильными группами.
Реакция с борно-лимонным реактивом (ре-акция Вильсона). Флавоноиды, у которых гидроксильная и карбоксильная группы от-делены углеродным атомом, образуют ком-плексы с кислотой борной, которые не раз-рушаются лимонной и щавелевой кислота-ми. При этом появляется желтая окраска или ярко-желтая флуоресценция, которая резко усиливается в УФ-свете.


Флаваноны и флаванонолы восстанавливаются натрия боргидридом
с образованием окрашенных продуктов пурпурно-красного, фиолетового или синего цвета.
1 2 8 Фенольные соединения. Тема 8. Флавоноиды




Катехины, а также производные флороглюцина и резорцина с 1 %-ным раствором ванилина в кислоте хлористоводородной концентрированной образу-ют малиново-красное окрашивание.
Хроматографический анализ. Для идентификации флавоноидов широко применяют различные виды хроматографии: бумажную, ТСХ, газожидкост-ную. Учитывают окраску пятен в видимом и УФ-свете до и после проявления хромогенными реактивами, величину Rf, или время удерживания. Флавоны
и флавонол-3-гликозиды в УФ-свете обнаруживаются в виде коричневых пя-тен; флавонолы и их 7-гликозиды — в виде желтых или желто-зеленых пятен. Изофлавоноиды в видимом свете не проявляются.
После просматривания в УФ-свете хроматограммы обрабатывают одним из реактивов: 5 %-ным спиртовым раствором AlCl3 с последующим нагрева-нием при 100±5 °С в течение 3—5 мин; 5 %-ным раствором SbCl3 в тетрахлор-метане; 10 %-ным спиртовым раствором щелочи. Это позволяет получить зоны с более яркой флюоресценцией в УФ-свете. Типовая хроматограмма флаво-ноидов представлена на цв. вкл. VII, рис. 1, а ориентировочная окраска пятен флавоноидов — в табл. 8. 1.
|
|
|
Т а б л и ц а 8. 1
Окраска пятен флавоноидов на хроматограммах

Количественное определение. Универсального метода количественного оп-ределения флавоноидов нет. В каждом отдельном случае подходят индивиду-ально, используя весовой, фотометрический, полярографический, потен-циометрический, объемный или комплексонометрический методы.
Наибольшее распространение получили спектральные методы анализа, которые можно классифицировать по реакциям образования окрашенных продуктов: восстановления в кислой среде или с натрия боргидридом; реак-ции комплексообразования с металлами; соединение с солями диазония; взаимодействие со щелочами.
Биологическая активность. Флавоноиды обладают широким спектром дей-ствия: капилляроукрепляющим, желчегонным, диуретическим, гепато-защитным, седативным, противовоспалительным, противоязвенным, гемо-
| Химический анализ ЛРС, содержащего флавоноиды | 1 2 9 | |
статическим, бактерицидным, гипотензивным, гипогликемическим, анабо-лизирующим, противолучевым, антиоксидантным и др.
Химический анализ ЛРС,
|
|
|


