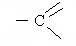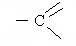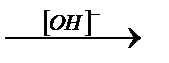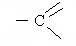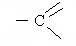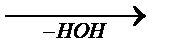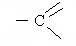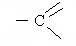Оксимы применяются для получения пестицидов, лекарственных веществ, реактивы для анализа.
Реакции полимеризации и поликонденсации
1) Образование полиформальдегида идет с разрывом двойной связи карбонильной группы и приводит к образованию линейного полимера с открытой цепью или циклического:
Линейная полимеризация
| линейный полимер формальдегида
|
СН
2= О + СН
2 = О + СН
2 = О +...→ СН
2 - О - СН
2 - О - СН
2 – О …
или
nСН2 = О → (- СН2 - О -)n
Циклическая полимеризация
Н
2С + СН
2→
2) Образование альдегидов; при этом образуется более сложные соединения в результате возникновения новых связей между атомами углерода.
В начальной стадии конденсации альдегида с альдегидом образуется альдоль (соединение, одновременно содержащее альдегидную и спиртовую группу). Реакция протекает в присутствии оснований по схеме:
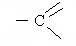
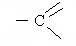
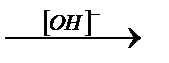
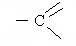
+
Этот тип конденсации получил название альдольной конденсации (по существу является реакцией полимеризации). Полученный альдоль при нагревании легко отщепляет молекулы Н
2O с образованием непредельного кротонового альдегида:
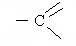
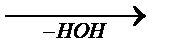
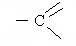
СН
3 - СН – СН СН
3 - СН = СН
Эта реакция пример кротоновой конденсации. В реакциях полимеризации молекулы мономеров соединяются друг с другом через кислород, а в реакциях конденсации через атомы углерода. Альдегиды вступают в реакции конденсации и с соединениями других классов, что используется в производстве пластмасс.
Отдельные представители и их использование в промышленности.
 1) Муравьиный альдегид
1) Муравьиный альдегид (
формальдегид, метаналь)
Образуется при неполном сгорании метана угля, дерева.
В промышленности получается каталитическим окислением или дегидрированием метилового спирта.
Формальдегид – ядовитый газ, tk = - 19,20С, tпл = - 920С, 33-40% водный раствор называют формалином. Формальдегид может вступать в реакцию конденсации альдольного типа с образованием моносахаридов:
6 СН2О → С6Н12 О6
Формальдегид используется при производстве лекарственных средств (уротропин), используется в медицине, в производстве высокомолекулярных соединений, взрывчатых веществ, различных смол, используется в производстве пластмасс.
Применяется в кожевенной промышленности при дублении кожи, дезинфицирующее средство для протравы семян. Содержится в дыме (образуется при сгорании угля и дерева), а на консервирующем действии дыма основано копчение мясных, рыбных и других продуктов.
 2) Уксусный альдегид
2) Уксусный альдегид
В промышленности получается из ацетилена (ацетальдегид) по реакции Кучерова. Уксусный альдегид – низкокипящая жидкость (tk = +200С). В малых концентрациях запах прелых яблок (в них и содержится).
Находит промышленное применение для получения этилового спирта, уксусной килоты, сухого спирта (метальдегида (СН3СНО)4).
3) Ацетон (диметил кетон или пропанон) СН
3 – С - СН
3
Бесцветная жидкость (tk = +56,10С)
со специфическим запахом.
Применяется в промышленности как растворитель лаков, красок, в производстве кинопленок, ацетатного шелка, органического стекла, полимеров, клея, а также в парфюмерии.
4.Карбоновые кислоты. Понятие о карбоновых кислотах. Карбоксильная группа как функциональная. Гомологический ряд предельных однооснóвных карбоновых кислот. Получение карбоновых кислот окислением альдегидов. Химические свойства уксусной кислоты: общие свойства с минеральными кислотами и реакция этерификации. Применение уксусной кислоты на основе свойств. Высшие жирные кислоты на примере пальмитиновой и стеариновой.
Воспользуйтесь поиском по сайту: