 |
Тесты к теме: Поверхностные явления. Адсорбция.
|
|
|
|
1. Подвижная поверхность раздела возникает на границе:
а) жидкость – газ;
б) жидкость – твёрдое тело;
в) жидкость – жидкость;
г) твёрдое тело – газ.
2. Неподвижная поверхность раздела возникает на границе:
а) жидкость – газ;
б) жидкость – твёрдое тело;
в) жидкость – жидкость;
г) твёрдое тело – газ.
3. Сорбцией называется:
а) притяжение (сцепление или прилипание) приведённых в контакт поверхностей двух конденсированных фаз;
б) самопроизвольное изменение формы граничной поверхности;
в) самопроизвольное накопление (поглощение) газообразного или растворённого в жидкости вещества на поверхности либо в объеме конденсированной фазы (твёрдого тела или жидкости);
г) образование поверхности раздела между двумя несмешивающимися фазами.
4. Адгезией называется:
а) притяжение (сцепление или прилипание) приведённых в контакт поверхностей двух конденсированных фаз;
б) самопроизвольное изменение формы граничной поверхности;
в) самопроизвольное накопление (поглощение) газообразного или растворённого в жидкости вещества на поверхности либо в объеме конденсированной фазы (твёрдого тела или жидкости);
г) образование поверхности раздела между двумя несмешивающимися фазами.
5. Адсорбция – это:
а) накопление частиц адсорбтива на поверхности адсорбента;
б) накопление частиц адсорбента на поверхности адсорбтива;
в) накопление частиц адсорбата на поверхности адсорбтива;
г) накопление частиц адсорбата внутри адсорбента.
6. Абсорбция – это:
а) объемное поглощение газообразного вещества конденсированной фазой;
б) процесс смешивания между собой различных газов;
в) объемное поглощение растворённого в жидкости вещества твердой фазой;
|
|
|
г) процесс смешивания между собой двух взаиморастворимых жидкостей.
7. Физической сорбцией называется процесс:
а) накопления одного вещества на поверхности или в объеме другого вещества, происходящий за счёт действия сил химической связи;
б) накопления одного вещества на поверхности или в объеме другого вещества, происходящий за счёт действия межмолекулярных или ван – дер – ваальсовых сил;
в) накопления одного вещества на поверхности или в объеме другого вещества, сопровождающийся образованием новых химических соединений;
г) накопления сорбтива на поверхности или в объеме сорбента, не сопровождающийся химическим взаимодействием, приводящим к образованию новых веществ.
8. Хемосорбция – это процесс избирательного накопления сорбтива на поверхности или в объеме сорбента:
а) происходящий за счёт химического взаимодействия и приводящий к образованию новых веществ;
б)при котором частицы обоих взаимодействующих веществ не теряют своей индивидуальности;
в)происходящий за счёт сил кулоновского взаимодействия между заряженными частицами, которые при этом не теряют своей индивидуальности;
г) сопровождающийся образованием новых соединений, которые не образуют самостоятельную фазу.
9. Физическая сорбция в отличие от хемосорбции:
а) является обратимым процессом;
б) протекает с незначительным тепловым эффектом (Q ≤ 20кДж/моль)
в) является необратимым процессом;
г) определяется только временем диффузии сорбтива к поверхности сорбента и не зависит от активационного фактора.
10. Хемосорбция в отличие о физической сорбции:
а) является более избирательным процессом и очень сильно зависит от природы сорбента и сорбтива;
б) протекает с гораздо большей скоростью и не зависит от температуры;
в) сопровождается значительным тепловым эффектом (Q ≥ 40 кДж/моль);
|
|
|
г) является необратимым процессом.
11. Капиллярная конденсация – это:
а) разновидность химической сорбции;
б) разновидность физической сорбции;
в) процесс, протекающий при повышенной температуре (t > t кип. жидк.);
г) процесс поглощения газа твердым пористым адсорбентом, сопровождающийся его частичной конденсацией.
12. Повышение температуры:
а) приводит к увеличению физической сорбции;
б) приводит к увеличению химической сорбции;
в) не влияет как на физическую, так и на химическую сорбцию;
г) приводит к уменьшению физической сорбции.
13. Древесный уголь, сажа, графит лучше адсорбируют:
а) неполярные органические жидкости;
б) полярные органические и неорганические жидкости;
в) электролиты из водных растворов;
г) неэлектролиты из водных растворов.
14. Полярные адсорбенты (ионные кристаллы) лучше адсорбируют:
а) неполярные органические жидкости;
б) полярные органические и неорганические жидкости;
в) электролиты из водных растворов;
г) неэлектролиты из водных растворов.
15. Величина адсорбции Г в системе СИ измеряется в:
а) моль/л;
б) моль/м2;
в) моль/см2;
г) моль/кг.
16. Поверхностное натяжение – это:
а) суммарная внутренняя энергия молекул, находящихся в поверхностном слое;
б) избыточная суммарная внутренняя энергия молекул, находящихся в поверхностном слое площадью 1 м2 или 1см2 по сравнению с суммарной внутренней энергией молекул, расположенных в таком же по размерам слое, но в глубине фазы;
в) работа, которую нужно совершить, чтобы переместить молекулы из глубины фазы для создания поверхности площадью 1м2 или 1см2;
г) суммарная потенциальная энергия молекул, находящихся в поверхностном слое площадью 1м2 или 1см2.
17. Поверхностное натяжение жидкости:
а) не зависит от природы газовой фазы, с которой она граничит;
б) не зависит от температуры жидкости;
в) не зависит от внешнего давления;
г) не зависит от площади поверхности жидкости.
18. Поверхностное натяжение индивидуальной жидкости:
а) возрастает с уменьшением температуры;
б) возрастает с увеличением температуры;
в) возрастает с увеличением взаимодействия между её молекулами;
г) возрастает с увеличением давления.
|
|
|
19. Высокое значение поверхностного натяжения воды при 298 К по сравнению с другими жидкостями обусловлено:
а) ее значительной диэлектрической проницаемостью;
б) формой и размерами ее молекул;
в) способностью молекул Н2О образовывать межмолекулярные водородные связи;
г) величиной ее относительной молекулярной массы.
20. Поверхностная энергия жидкости может быть уменьшена:
а) за счет изменения способа расположения ее молекул друг относительно друга;
б) за счет уменьшения площади ее поверхности;
в) за счет уменьшения ее поверхностного натяжения;
г) за счет уменьшения ее температуры.
21. По отношению к Н2О ПАВ являются:
а) такие органические соединения как спирты, амины, карбоновые кислоты;
б) насыщенные и ненасыщенные углеводороды;
в) ароматические углеводороды;
г) неорганические и органические электролиты.
22. По отношению к Н2О ПИВ являются:
а) алканы и циклоалканы;
б) сильные неорганические кислоты;
в) соли и щелочи;
г) моносахариды.
23. По отношению Н2О ПНВ являются:
а) соли азотной кислоты;
б) соли уксусной кислоты;
в) глюкоза;
г) сахароза.
24. Поверхностно – активные вещества поверхностное натяжение растворителя:
а) повышают;
б) понижают;
в) в зависимости от концентрации могут как повышать, так и понижать;
г) не изменяют.
25. Поверхностно – инактивные вещества поверхностное натяжение растворителя:
а) повышают;
б) уменьшают в очень сильной мере;
в) не изменяют;
г) могут, как повышать, так и понижать в зависимости от своей концентрации.
26. Поверхностно – неактивные вещества:
а) повышают поверхностное натяжение растворителя, только присутствуя в растворах в больших количествах;
б)изменяют поверхностное натяжение растворителя только при малых концентрациях;
в)практически не изменяют поверхностное натяжение растворителя, присутствуя в растворе даже в значительных количествах;
г) не способны растворяться в растворителе.
27. При растворении ПАВ концентрация их молекул в поверхностном слое жидкости по сравнению с таким же слоем, но расположенным в ее глубине:
|
|
|
а) практически одинаковая;
б) значительно выше;
в) всегда во много раз ниже;
г) может быть как ниже, так и выше в зависимости от времени наблюдения.
28. При растворении ПИВ концентрация их частиц в поверхностном слое жидкости по сравнению с таким же слоем, но расположенным в ее глубине:
а) практически одинаковая;
б) значительно выше;
в) всегда во много раз ниже;
г) может быть как ниже, так и выше в зависимости от времени наблюдения.
29. Уравнение Гиббса для расчета величины адсорбции Г на границе раздела жидкость – газ выглядит следующим образом:
а) Г = К·С1/n;
б) 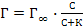 ;
;
в) 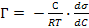 ;
;
г) 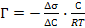 .
.
30. Поверхностная активность вещества g показывает:
а) как изменяется поверхностное натяжение раствора при увеличении концентрации растворенного вещества в 2 раза;
б)во сколько раз увеличивается поверхностное натяжение раствора при увеличении концентрации растворенного вещества в 2 раза;
в)во сколько раз уменьшается поверхностное натяжение раствора при уменьшении концентрации ПАВ в 2 раза;
г) как изменяется поверхностное натяжение раствора при увеличении концентрации растворенного вещества на единицу.
31. Поверхностная активность вещества g рассчитывается по формуле:
а)  ;
;
б)  ;
;
в)  ;
;
г) 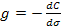 .
.
32. Величина адсорбции Г имеет положительное значение при:
а) dσ>0 и dc>0;
б) dσ<0 и dc>0;
в) dσ<0 и dc<0;
г) dσ=0 и dc>0.
33. Величина адсорбции Г имеет отрицательное значение при:
а) dσ>0 и dc>0;
б) dσ<0 и dc>0;
в) dσ<0 и dc<0;
г) dσ=0 и dc>0.
34. Поверхностная активность ПАВ имеет наибольшее значение:
а) при его малых концентрациях в растворе;
б) при его высоких концентрациях в растворе;
в) независимо от его концентрации в растворе;
г) при его концентрации в растворе равной 1 моль/л.
35. Поверхностная активность ПАВ имеет наименьшее значение при:
а) при его малых концентрациях в растворе;
б) при его высоких концентрациях в растворе;
в) независимо от его концентрации в растворе;
г) при его концентрации в растворе равной 1 моль/л.
36. К ПАВ относятся вещества, молекулы которых:
а) состоят только из гидрофобной углеводородной цепи;
б)являются симметричными и обе их части являются или гидрофильными, или гидрофобными;
в)имеют несимметричное строение и состоят из сравнительно небольшой полярной группы и длинного углеводородного радикала;
г) могут иметь самое различное строение.
37. Полярная и неполярная части молекулы ПАВ соединяются между собой:
а) ковалентной связью;
б) ионной связью;
в) водородной связью;
г) межмолекулярными связями.
38. Поверхностная активность ПАВ возрастает с:
|
|
|
а) увеличением длины его углеводородного радикала;
б) уменьшением длины его углеводородного радикала;
в) увеличением его растворимости;
г) уменьшением его растворимости.
39. Поверхностная активность ПАВ равна нулю:
а) в области малых концентраций;
б) в области больших концентраций;
в) при Г = Г∞;
г) ни при каких условиях не может быть равна нулю.
40. Зависимость поверхностной активности ПАВ от длины его углеводородного радикала определяется:
а) изотермой его адсорбции;
б) правилом Дюкло-Траубе;
в) уравнением Гиббса;
г) уравнением Лэнгмюра.
41. К молекулярным или неионогенным ПАВ относятся:
а) алифатические спирты;
б) соли жирных карбоновых кислот;
в) сложные эфиры;
г) третичные амины.
42. К ионогенным катионактивным ПАВ относятся:
а) вторичные или третичные амины;
б) некоторые высшие карбоновые кислоты;
в) простые эфиры;
г) ароматические спирты.
43. К ионогенным анионактивным ПАВ относятся:
а) фенолы;
б) соли жирных карбоновых кислот;
в) сульфоалканы;
г) сложные эфиры.
44. Амфолитные ПАВ:
а) являются электронейтральными молекулами;
б) содержат в молекуле одну или несколько гидрофильных групп, способных быть как донорами, так и акцепторами протонов в зависимости от рН раствора;
в) могут быть как ионогенными, так и неионогенными в зависимости от их концентрации в растворе;
г) являются симметричными молекулами, гидрофильная и гидрофобная части которых имеют одинаковые размеры.
45. Площадь So, занимаемая одной молекулой ПАВ в поверхностном слое жидкости при Г = Г∞, зависит от:
а) размеров молекулы ПАВ;
б) длины её углеводородного радикала;
в) размеров её гидрофильной части;
г) концентрации ПАВ в растворе.
46. В насыщенном мономолекулярном слое молекулы ПАВ располагаются:
а) горизонтально поверхности жидкости;
б) перпендикулярно поверхности жидкости;
в) беспорядочно;
г) или горизонтально, или вертикально поверхности жидкости в зависимости от концентрации ПАВ в растворе.
47. Площадь, занимаемая одной молекулой ПАВ в поверхностном слое при их малой концентрации в растворе зависит от:
а) размеров молекулы ПАВ;
б) размеров её гидрофильной части;
в) концентрации ПАВ в растворе;
г) температуры раствора.
48. Площадь So, занимаемую одной молекулой ПАВ в насыщенном мономолекулярном слое при Г = Г∞, можно рассчитать по формуле:
а) So = v·ρ;
б)So = Г·М;
в)So = No·Г;
г) 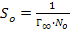 .
.
49. Длину молекулы ПАВ можно рассчитать по формуле:
а) l = v·ρ;
б) l = ρ/m;
в) l = M·ρ/Го;
г)  .
.
50. Поверхность твёрдого адсорбента:
а) является однородной;
б) обладает одинаковыми адсорбционными свойствами;
в) содержит в своём составе так называемые адсорбционные или активные центры;
г) содержит малые участки с повышенным запасом свободной поверхностной энергии Гиббса.
51. Адсорбция на твёрдой поверхности в отличие от адсорбции на поверхности жидкости:
а) может быть как мономолекулярной, так и полимолекулярной;
б)может осуществляться только за счёт действия сил физической природы;
в)происходит, в первую очередь, на её определённых участках, обладающих повышенным запасом внутренней энергии;
г) всегда является необратимым процессом.
52. Мономолекулярная адсорбция газа по Лэнгмюру на твёрдом адсорбенте:
а) происходит на всей поверхности адсорбента;
б) происходит только на активных центрах адсорбента;
в) является обратимым процессом;
г) осуществляется только за счёт действия сил химической природы.
53. Уравнение Лэнгмюра, описывающее адсорбцию газа на твёрдой поверхности, имеет вид:
а) 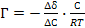 ;
;
б) 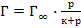 ;
;
в) 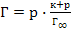 ;
;
г) 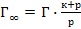 .
.
54. Уравнение Лэнгмюра позволяет описать:
а) любой участок изотермы адсорбции;
б)только тот участок изотермы адсорбции, который имеет прямолинейный характер;
в)только тот участок изотермы адсорбции, который изображается параболической кривой;
г) только тот участок изотермы адсорбции, который изображается прямой, параллельной оси абсцисс.
55. Уравнение Фрейндлиха позволяет описать:
а) любой участок изотермы адсорбции;
б) только тот участок изотермы адсорбции, который имеет прямолинейный характер;
в) только тот участок изотермы адсорбции, который изображается параболической кривой;
г) только тот участок изотермы адсорбции, который изображается прямой, параллельной оси абсцисс.
56. Уравнение Фрейндлиха для адсорбции газа имеет следующий вид:
а) 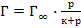 ;
;
б) Г = K·p1/n;
в) 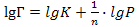 ;
;
г) Г = n·pk.
57. Удельную поверхность твёрдого адсорбента можно рассчитать по формуле:
а) Sуд =Г∞·NA;
б) Sуд = Г∞·NA·K;
в) Sуд = Г·∞NA·So;
г) Sуд = Г∞·NA/So.
58. Константа К в уравнении Фрейндлиха для адсорбции газа представляет собой:
а) величину адсорбции Г при равновесном давлении газа равном единице;
б)равновесное давление газа, при котором все активные центры, расположенные на поверхности твердого адсорбента, насыщены молекулами газа;
в)величину адсорбции Г при равновесном давлении газа равном атмосферному;
г) величину адсорбции Г∞ при данных внешних условиях.
59. Предельное значение адсорбции газа Г∞ на данном адсорбенте:
а) не зависит от величины температуры;
б) с увеличением температуры уменьшается;
в) с увеличением температуры увеличивается;
г) зависит от температуры сложным образом.
60. Предельное значение адсорбции газа Г∞ на данном адсорбенте с увеличением температуры:
а) достигается при более низком равновесном давлении газа р;
б) достигается при более высоком равновесном давлении газа р;
в) достигается всегда при одном и том же равновесном давлении газа р;
г) не изменяет своей величины.
61. При одинаковых внешних условиях на активированном угле лучше всего будет адсорбироваться газ:
а) кислород;
б) водород;
в) азот;
г) хлор.
62. Из воздуха на твердом адсорбенте лучше всего будет адсорбироваться:
а) водяной пар;
б) углекислый газ;
в) кислород;
г) азот.
63. Адсорбция газа на твердом адсорбенте зависит от:
а) его цвета и запаха;
б) природы адсорбента и адсорбтива;
в) температуры кипения газа;
г) равновесного давления газа над твердым адсорбентом.
64. Согласно теории БЭТ – Поляни образование дополнительных адсорбционных слоев на твердом адсорбенте:
а) происходит за счет сил межмолекулярного взаимодействия;
б) в результате конденсации молекул пара;
в)происходит только после завершения формирования первого мономолекулярного слоя;
г) возможно при незаконченном первом мономолекулярном слое.
65. При адсорбции из растворов на твердом адсорбенте:
а) всегда происходит накопление только растворителя;
б)может происходить как адсорбция растворенного вещества, так и растворителя;
в) осаждаются только молекулы растворенного вещества, независимо от его природы;
г) могут осаждаться как молекулы, так и ионы растворенного вещества.
66. Величину адсорбции Г из растворов на твердом адсорбенте можно рассчитать по формуле:
а)  ;
;
б) 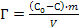 ;
;
в)  ;
;
г) 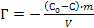 .
.
67. Соотношение между адсорбированными на твердом адсорбенте молекулами растворенного вещества и растворителя зависит от:
а) времени, в течение которого происходит процесс адсорбции;
б)собственной адсорбционной способности этих соединений на твердом адсорбенте;
в) концентрации раствора;
г) массы адсорбента.
68. На активированном угле из бинарной системы бензол – анилин:
а) лучше будет адсорбироваться бензол;
б) лучше будет адсорбироваться анилин;
в) оба вещества будут адсорбироваться в одинаковой мере;
г) оба вещества не будут адсорбироваться.
69. На силикагеле (SiO2) из бинарной системы бензол – анилин:
а) лучше будет адсорбироваться бензол;
б) лучше будет адсорбироваться анилин;
в) оба вещества будут адсорбироваться в одинаковой мере;
г) г) оба вещества не будут адсорбироваться.
70. С помощью гидрофильного адсорбента (глина, силикагель) ПАВ лучше извлекается из:
а) воды;
б) бензола;
в) гексана;
г) этанола.
71. С помощью гидрофобного адсорбента (уголь, графит, парафин) ПАВ лучше извлекается из:
а) воды;
б) бензола;
в) гексана;
г) этанола.
72. Отрицательная адсорбция на твердом адсорбенте происходит:
а) если вместо растворенного вещества адсорбируется растворитель;
б) при использовании разбавленных растворов;
в) при использовании концентрированных растворов;
г) если растворитель и адсорбент очень сильно различаются своей полярностью.
73. Специфическая или избирательная ионная адсорбция происходит на:
а) неполярном адсорбенте;
б) любом твердом адсорбенте;
в) ионных кристаллах;
г) твердом адсорбенте, поверхность которого образована полярными молекулами, способными к диссоциации в водном растворе.
74. Адсорбционная способность ионов в водном растворе зависит от:
а) величины их заряда;
б) степени гидратации;
в) радиуса в гидратированном состоянии;
г) массы иона.
75. При примерно одинаковом радиусе, с увеличением величины заряда адсорбционная способность ионов:
а) возрастает;
б) уменьшается;
в) остается неизменной;
а) изменяется сложным образом.
76. При одинаковой величине заряда с возрастанием радиуса ионов их адсорбционная способность:
а) а)возрастает;
б) уменьшается;
в) остается неизменной;
г) изменяется сложным образом.
77. Наличие гидратной оболочки у иона:
а) увеличивает его адсорбционную способность;
б) ослабляет его адсорбционную способность;
в) не влияет на его адсорбционную способность;
г) влияет на его адсорбционную способность сложным образом.
78. Для однозарядных катионов щелочных металлов в случае их адсорбции из водного раствора лиотропный ряд выглядит следующим образом:
а) Cs+>Rb+>K+>Na+>Li+;
б) Cs+<Rb+<K+<Na+<Li+;
в) Li+> Cs+>Na+> K+>Rb+;
г) Li+< Cs+<Na+< K+<Rb+.
79. Вид потенциалопределяющих ионов при их избирательной адсорбции на ионном кристалле определяется с помощью правила:
а) Дюкло –Траубе;
б) Шульца – Гарди;
в) Панета – Фаянса;
г) Гендерсона – Гассельбаха.
80. Эквивалентная ионная адсорбция:
а) характерна только для слабых электролитов;
б) характерна только для сильных электролитов;
в) характерна для любого электролита;
г) не характерна никакому электролиту.
81. Для однозарядных галогенид – анионов в случае их адсорбции из водных растворов лиотропный ряд выглядит следующим образом:
а) I-<Br-<Cl-<F-;
б) I->Br->Cl->F-;
в) F->I->Cl->Br-;
г) F-<I-<Cl-<Br-;
82. Из ионов щелочных металлов в водном растворе наибольшей адсорбционной способностью обладает:
а) Cs+;
б) Rb+;
в) К+;
г) Na+.
83. Из галогенид – анионов, находящихся в водном растворе, наименьшей адсорбционной способностью обладает:
а) I-;
б) Br-;
в) Cl-;
г) F-.
84. На твердом ионном адсорбенте BaSO4, согласно правила Панета – Фаянса, из раствора, содержащего смесь ионов Ba2+, Cl-, Na+, NO3-, в первую очередь будет адсорбироваться:
а) Ba2+;
б) Na+;
в) Cl-;
г) NO3-.
85. Двойной электрической слой на поверхности твердого адсорбента образуется:
а) при эквивалентной ионной адсорбции;
б) при избирательной ионной адсорбции;
в) при ионообменной адсорбции;
г) всегда, независимо от вида ионной адсорбции.
86. Катионитом будет являться адсорбент, содержащий в своем составе многочисленные:
а) –SO3H – группы;
б) –COOH – группы;
в) –NH2 – группы;
г) –ОН – группы.
87. Анионитом будет являться адсорбент, содержащий в своем составе многочисленные:
а) –SO3Na – группы;
б) –NH3+Cl- - группы;
в) –NH2 – группы;
г) –SH – группы.
88. Аниониты диссоциируют с выделением в раствор:
а) катионов;
б) анионов;
в) OH- – ионов;
г) Н+ –ионов.
89. Катиониты диссоциируют с выделением в раствор:
а) катионов;
б) анионов;
в) OH- – ионов;
г) Н+–ионов.
90. Хроматографические методы анализа используются для:
а) определения размеров молекул растворённых веществ;
б) разделения веществ в смесях;
в) определения количественного и качественного состава смесей различных соединений;
г) выделения индивидуальных веществ из смесей.
91. Хроматографические методы анализа основаны на:
а) различной способности индивидуальных веществ проходить через полупроницаемые мембраны;
б) различной способности индивидуальных веществ проходить через диализационные мембраны;
в) различной адсорбционной способности индивидуальных веществ;
г) различной электропроводности растворов химических соединений.
92. В распределительной хроматографии подвижная и неподвижная фазы находятся в:
а) жидком агрегатном состоянии;
б) любом агрегатном состоянии;
в) жидком или твёрдом агрегатном состоянии;
г) твердом или газообразном состоянии.
93. Адсорбционная хроматография основана на различной способности отдельных компонентов смеси:
а) подвергаться электролитической диссоциации;
б) вступать в химическое взаимодействие с веществом неподвижной фазы;
в)вступать во взаимодействие с поверхностью адсорбента и удерживаться на его активных центрах;
г) проходить через диализационные мембраны.
94. В газо–жидкостной хроматографии неподвижная фаза находится в:
а) газообразном состоянии;
б) твёрдом состоянии;
в) жидком состоянии;
г) любом агрегатном состоянии.
95. К основным хроматографическим параметрам, характеризующим поведение веществ в колонке, относятся:
а) коэффициент распределения Rf;
б) время удерживания tR;
в) удерживаемый объем VR;
г) коэффициент диффузии D.
96. Время удерживания tR – это время от момента ввода анализируемой пробы до:
а) полного элюирования вещества из колонки;
б)начала регистрации детектором индивидуального вещества, входящего в состав смеси;
в)регистрации самописцем максимума пика индивидуального вещества на хроматографии;
г) окончания удерживания индивидуального вещества смеси на неподвижной фазе.
97. Основы хроматографического метода анализа были разработаны ученым:
а) Цветом;
б) Лэнгмюром;
в) Фрейндлихом;
г) Ребиндером.
98. Адсорбционная способность иона усиливается при:
а) уменьшении величины его заряда;
б) возрастании величины его заряда;
в) уменьшении его радиуса;
г) увеличении его радиуса.
99. На кристаллах AgI из раствора, содержащего смесь солей КF и СН3СООAg, преимущественно будут адсорбироваться ионы:
а) К+;
б) F-;
в) Ag+;
г) СН3СОО-.
100. На кристаллах Са3(РО4)2 из раствора, содержащего смесь солей СаCl2 и К2SO4, преимущественно будут адсорбироваться ионы:
а) Са2+;
б) К+;
в) Сl-;
г) SO42-.
Ответы.
|
|
|


