 |
3.1.3 Определение термодинамических параметров реакции, протекающей в гальваническом элементе
|
|
|
|
Для обратимо работающего гальванического элемента при Р и Т = const изменение энергии Гиббса 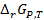 равно максимальной полезной работе W, взятой с обратным знаком
равно максимальной полезной работе W, взятой с обратным знаком 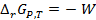 . С другой стороны, электрическая работа, связанная с переносом заряда, соответствующего одному молю вещества, между электродами с разностью потенциалов Е (ЭДС), равна
. С другой стороны, электрическая работа, связанная с переносом заряда, соответствующего одному молю вещества, между электродами с разностью потенциалов Е (ЭДС), равна 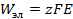 (см. выражение (3. 5)).
(см. выражение (3. 5)).
В результате получим выражение:
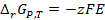 (3. 14)
(3. 14)
Изменение энтропии, характеризующее электрохимическую реакцию, равно
 (3. 15)
(3. 15)
Из термодинамики известно, что
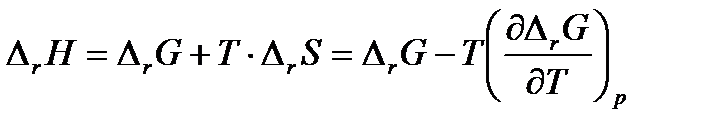 (3. 16)
(3. 16)
Подставим в уравнение (3. 16) уравнение (3. 14), преобразуем и получим:
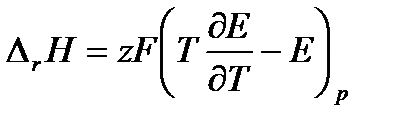 (3. 17)
(3. 17)
Последнее уравнение является одной из форм уравнения Гиббса – Гельмгольца и позволяет рассчитать тепловой эффект реакции, протекающей в элементе, если известны его электродвижущая сила и температурный коэффициент ЭДС  . Знак
. Знак  связан со знаком температурного коэффициента ЭДС. Действительно,
связан со знаком температурного коэффициента ЭДС. Действительно, 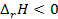 (теплота выделяется), если
(теплота выделяется), если 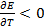 или
или 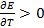 , но
, но  . Энтальпия увеличивается (
. Энтальпия увеличивается ( 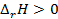 ), если
), если 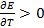 и
и  . В последнем случае элемент работает с поглощением теплоты из окружающей среды. Если
. В последнем случае элемент работает с поглощением теплоты из окружающей среды. Если 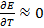 , то
, то  , т. е. в этом случае все тепло практически можно превратить в работу, и коэффициент полезного действия такого элемента приближается к 100%.
, т. е. в этом случае все тепло практически можно превратить в работу, и коэффициент полезного действия такого элемента приближается к 100%.
При достижении равновесия при Т, Р = const изменение энергии Гиббса равно нулю и для термодинамической константы равновесия электро-химической реакции, протекающей в гальваническом элементе, справедливо:
|
|
|
 , (3. 18)
, (3. 18)
где  – изменение энергии Гиббса химической реакции, протекающей при условии, что активности всех компонентов равны единице. По определению стандартный потенциал электрода – это потенциал при активностях окисленной и восстановленной формы равных единице. Стандартная ЭДС – разность стандартных потенциалов. Следовательно,
– изменение энергии Гиббса химической реакции, протекающей при условии, что активности всех компонентов равны единице. По определению стандартный потенциал электрода – это потенциал при активностях окисленной и восстановленной формы равных единице. Стандартная ЭДС – разность стандартных потенциалов. Следовательно,
 (3. 19)
(3. 19)
где  – стандартная ЭДС и стандартные потенциалы положительного и отрицательного электродов, соответственно.
– стандартная ЭДС и стандартные потенциалы положительного и отрицательного электродов, соответственно.
Пример: Составим элемент, в котором обратимо протекает реакция:

Используя стандартную ЭДС этого элемента рассчитаем стандартные термодинамические функции этой реакции, константу равновесия при температуре 325 К, если температурный коэффициент стандартной ЭДС составляет  В/К.
В/К.
Решение: Сначала нужно выяснить, из каких электродов состоит гальванический элемент, на котором протекает данная реакция.
В данной реакции серебро окисляется, повышая свою степень окисления, а  восстанавливается, понижая свою степень окисления. Хлорид серебра
восстанавливается, понижая свою степень окисления. Хлорид серебра  и каломель
и каломель  , участвующие в реакции, являются малорастворимыми соединениями (см. таблицу 78 справочника [2]), следовательно, они входят в состав электродов второго рода: хлорсеребрянного и каломелевого.
, участвующие в реакции, являются малорастворимыми соединениями (см. таблицу 78 справочника [2]), следовательно, они входят в состав электродов второго рода: хлорсеребрянного и каломелевого.
Запишем электродные реакции, протекающие на электродах с учетом стехиометрических коэффициентов заданной реакции:
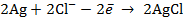
и
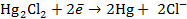
В суммарной реакции участвуют 2 электрона (  ).
).
|
|
|
Электрод, на котором протекает реакция окисления (хлорсеребрянный), будет располагаться на схеме гальванического элемента слева, а электрод, на котором идет реакция восстановления (каломелевый), - справа.
Электроды второго рода обязательно включают в себя хорошо растворимое соединение с анионом, одноименным аниону малорастворимого соединения. Поэтому хорошо растворимое соединение нужно включить в схему гальванического элемента, несмотря на то, что оно не входит в суммарную реакцию.
Гальванический элемент можно представить в виде гальванического элемента с переносомионов через границу раздела жидких фаз (т. е., с двумя жидкими фазами, между которыми располагается мембрана или электролитический мостик):

или без переноса ионов через границу раздела жидких фаз (с одной жидкой фазой, общей для двух электродов):

В таблице 79 [2] найдем стандартные потенциалы хлорсеребрянного и каломелевого электродов: +0, 222 В и +0, 268 В, соответственно. Стандартная ЭДС данного гальванического элемента при Т = 298 К:

Используя температурный коэффициент ЭДС  и приняв, что в указанном интервале температур зависимость Е0 = f(T) линейна, найдем:
и приняв, что в указанном интервале температур зависимость Е0 = f(T) линейна, найдем:
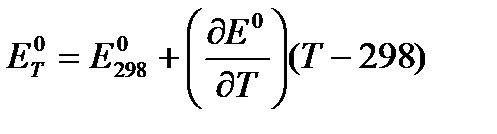
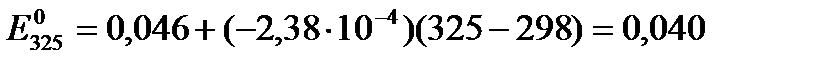 В.
В.
По формуле (3. 19) найдем  :
:

Термодинамическую константу равновесия найдем из формулы (3. 18):

Далее по формулам (3. 15) и (3. 16) рассчитаем изменение энтропии и тепловой эффект реакции при 325 К:
 Дж/(моль·К)
Дж/(моль·К)
 Дж/моль.
Дж/моль.
|
|
|


