 |
5. Приведем примеры соединений в устойчивых степенях окисления (простое вещество, оксиды и гидроксиды см. п.11)
|
|
|
|
Алгоритм
1. Найдем положение химического элемента в П. С. Д. И. Менделеева и составим электронную формулу, воспользовавшись реальной электронной схемой (см. п. 2) и сделаем вывод: указываем семейство и тип элемента. (см. п. 5 и п. 8)
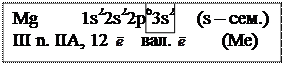 |
2. Графически изобразим валентные электроны в нормальном и возбужденном состояниях (см. п. 6 и п. 7)
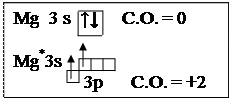 |
3. Укажем окислительно-восстановительные свойства атома, помня, что это металл (см. п. 8)
|
4. Исходя из числа неспаренных электронов в нормальном и возбужден-ном состояниях, укажем устойчивые С. О. (см. п. 9 или п. 10)
|
5. Приведем примеры соединений в устойчивых степенях окисления (простое вещество, оксиды и гидроксиды см. п. 11)
Mg0, Mg+2O
6. Укажем характер оксидов и гидроксидов (см. п. 11)
|
ТЕМА 3. КОВАЛЕНТНАЯ ХИМИЧЕСКАЯ СВЯЗЬ
1. Ковалентная связь – это связь за счёт общих электронных пар.
Н · + · Н → Н: Н
2. Механизмы образования:
а) обменный б) донорно-акцепторный
А · + · В → А: В А: + В → А: В
3. По способам перекрывания атомных орбиталей (А. О. ) различают:
σ -связь π -связь
перекрываются А. О. по линии связи перекрываются А. О. перпендикулярно ядер (лобовое перекрывание) линии связи ядер (боковое перекрыва-
ние)
|
|
|
Особенности: Особенности:
1) σ -связь первичная 1) π -связь вторичная
2) Еσ – высокая => прочная 2) Еπ > Еσ => слабая
3) σ -локализованная. 3) π -нелокализованная.
! Ковалентная связь строго направлена.
! Направленность зависит от типа гибридизации центрального атома в молекуле.
Гибридизация (смешение) - изменение первоначальной формы А. О. и образование новых А. О., но совершенно одинаковой формы. => Выигрыш энергии, т. к. связи за счёт гибридных А. О. более прочные.
Гибридная атомная орбиталь (Г. А. О. ) –
ассиметричная гантель
 |
Таблица 4 - Тип гибридизации и геометрия частицы
| Тип гибридизации | А. О. участвующие в гибридизации | Число Г. А. О. | Положение Г. А. О. относительно ядра центрального атома | Геометрия частицы |
| 1. sp | + s p | 2 ГАО sp | 180º | линейная |
| 2. sp2 | + p s p | 3 ГАО sp2 | 120˚ | треугольная угловая |
| 3. sp3 | + p s p p | 4 ГАО sp3 | 109˚ 28' | тетраэдр пирамида угловая |
| 4. sp3d | + p s p d p | 5 ГАО sp3d | y z x | тетраго- нальная пирамида плоский квадрат |
| 5. sp3d2 | + + s p d p p d | 6 ГАО sp3d2 | y z x | октаэдр |
|
|
|
РЕШЕНИЕ ТИПОВОЙ ЗАДАЧИ ПО ТЕМЕ: «ХИМИЧЕСКАЯ СВЯЗЬ»
Определите тип гибридизации и геометрию молекулы Н2О.
Алгоритм
1. Найдём центральный атом (ц. а. ) в молекуле – тот атом, степень окисления которого выше независимо от знака.
1. Н2+О-2 => ц. а. – О (ст. ок. ) = -2 => в атоме 2 неспаренных ē.
2. Определим число периферийных атомов (Н) – координационное число (к. ч. ), которое указывает на число σ -связей.
 |

 2. К. ч. (О) = 2 => 2 σ -связи. σ О σ Н
2. К. ч. (О) = 2 => 2 σ -связи. σ О σ Н
Н
3. Составим графическое изображение валентных электронов ц. а. в соответствующей степени окисления.
 |
8О 1s22s22p4
IIп. IVA вал. 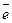
2p
| ↑ ↓ | ↑ | ↑ | |
| ↑ ↓ | |||
2s
 |
4. Определим тип гибридизации, зная, что в гибридизации участвуют только те валентные А. О., которые образуют σ -связи (орбитали с неспаренными электронами, а также орбитали со спаренными электронами последнего энергетического уровня (Э. У. ). На графическом изображении отсечём А. О., идущие на образование 2-х σ -связей и орбитали со спаренными электронами
 |
  
| ↑ | ↑ |
2p
2s => тип гибридизации sp3
2 σ -связи
 | |||
 | |||
5. Изобразим гибридизацию рисунком (см. табл. п. 3).
 |
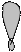







 р ↑ ↓
р ↑ ↓







 + p → → O
+ p → → O




 p
p

 s ↑ ↓
s ↑ ↓
 | |||||
 | |||||
 | |||||

 6. Покажем перекрывание А. О. ц. а. – О – с переферийными атомами – Н (зная, что от него в образовании связей участвуют 1s1орбитали.
6. Покажем перекрывание А. О. ц. а. – О – с переферийными атомами – Н (зная, что от него в образовании связей участвуют 1s1орбитали.
 |
↑ ↓
|
|
|
↑ ↓ H
H
7. Изобразим геометрию частицы (см. табл. 1 п. 3).
 |
↑ ↓
↑ ↓ 

 O
O
H H
Угловая молекула
 |
|
|
|



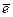 → Mg+2 (ок-с)
вос-ль
→ Mg+2 (ок-с)
вос-ль