 |
Пятая аналитическая группа катионов
|
|
|
|
К пятой аналитической группе относятся катионы  . В атомах элементов этой группы, таких, как марганец и железо, происходит достройка третьего электронного слоя от 8 до 18 электронов, сурьма и висмут имеют либо законченные 18-электронные внешние слои, либо оболочки, содержащие 18+2 электронов в двух наружных слоях.
. В атомах элементов этой группы, таких, как марганец и железо, происходит достройка третьего электронного слоя от 8 до 18 электронов, сурьма и висмут имеют либо законченные 18-электронные внешние слои, либо оболочки, содержащие 18+2 электронов в двух наружных слоях.
Эти элементы, за исключением висмута и магния, имеют переменную степень окисления и обладают тенденцией к комплексообразованию. Гидроксиды катионов пятой группы, кроме сурьмы (III), не обладают амфотерностью и не образуют растворимых аминокомплексов. Они количественно осаждаются избытком гидроксидов 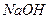 и
и 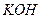 .
.
Групповой реагент - 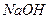 и
и 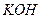 . Гидроксиды этих элементов нерастворимы в растворах щелочей.
. Гидроксиды этих элементов нерастворимы в растворах щелочей.
5.1 Частные реакции на катион Fe2+
Растворы солей железа (II) окрашены в бледно-зелёный цвет, разбавленные растворы бесцветны.
Гидроксиды 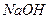 ,
, 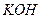 осаждают катионы
осаждают катионы 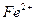 в виде
в виде  :
:
 (белый осадок)
(белый осадок)
На воздухе в результате частичного окисления кислородом осадок приобретает серо-зелёный цвет:

Гексациано(III)феррат калия  с
с 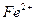 даёт синий осадок гексациано(III)феррата железа (II), называемый «турнбулевой синью»:
даёт синий осадок гексациано(III)феррата железа (II), называемый «турнбулевой синью»:

Осадок нерастворим в кислотах, но разлагается щелочами с выделением гидроксидов  . Предел обнаружения железа – 0,02 мкг. Реакция специфична.
. Предел обнаружения железа – 0,02 мкг. Реакция специфична.
Выполнение реакции: К 2-3 каплям слабокислого раствора, содержащего ионы железа (II), добавляют 1-2 капли раствора реагента. Образуется синий осадок. Реакция даёт хороший результат при pH=3. Свободные 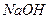 и
и 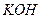 вызывают разложение турнбулевой сини. Катионы
вызывают разложение турнбулевой сини. Катионы  и другие катионы V группы не мешают определению.
и другие катионы V группы не мешают определению.
Диметилглиоксим ( реактив Чугаева) образует с катионом 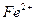 в аммиачных растворах устойчивое комплексное соединение красного цвета:
в аммиачных растворах устойчивое комплексное соединение красного цвета:
|
|
|

где  диметилглиоксим.
диметилглиоксим.
Комплексное соединение  с
с  хорошо растворимо в воде. Предел обнаружения железа – 8 мкг. Мешают ионы никеля (II), образующие нерастворимый в воде диметилглиоксимат никеля красного цвета. Мешающее влияние железа (III), образующего в аммиачной среде окрашенный гидроксид, устраняют добавлением лимонной, щавелевой или винной кислоты.
хорошо растворимо в воде. Предел обнаружения железа – 8 мкг. Мешают ионы никеля (II), образующие нерастворимый в воде диметилглиоксимат никеля красного цвета. Мешающее влияние железа (III), образующего в аммиачной среде окрашенный гидроксид, устраняют добавлением лимонной, щавелевой или винной кислоты.
Выполнение реакции: К 2-3 каплям раствора, содержащего ионы железа (II), добавляют каплю 20%-ного раствора винной кислоты, 1 каплю диметилглиоксима и по каплям раствор аммиака до щелочной реакции (pH=9). Раствор окрашивается в красный цвет.
5.2 Частные реакции на катион Fe3+
Гидроксиды  и
и  образуют с ионами
образуют с ионами  красно-бурый осадок
красно-бурый осадок  , нерастворимый в избытке щелочей и солей аммония:
, нерастворимый в избытке щелочей и солей аммония:

Гексациано(II)феррат калия  образует с
образует с  тёмно-синий осадок «берлинской лазури», аналогичный по составу «турнбулевой сини». Поскольку
тёмно-синий осадок «берлинской лазури», аналогичный по составу «турнбулевой сини». Поскольку  больше
больше  , сначала проходит окислительно-восстановительная реакция:
, сначала проходит окислительно-восстановительная реакция:

Далее продукты реакции взаимодействуют между собой с образованием темно-синего осадка «берлинской лазури»:

Различие в окраске и свойствах «берлинской лазури» и «турнбулевой сини» объясняется тем, что состав осадка не полностью соответствует написанной выше формуле. Осадок «берлинской лазури» растворяется в сильных кислотах и при добавлении избытка реагента. Предел обнаружения железа – 0,2 мкг. Мешают большие количества ионов металлов, которые дают окрашенные осадки с гесациано(II)ферратом калия. Мешают фториды и оксалаты, образующие устойчивые комплексы с  .
.
Выполнение реакции: К 1-2 каплям раствора, содержащего ионы  и имеющего рН 1-3, добавляют каплю реагента. Наблюдают образование темно-синего осадка «берлинской лазури».
и имеющего рН 1-3, добавляют каплю реагента. Наблюдают образование темно-синего осадка «берлинской лазури».
Роданид аммония  с
с  образует роданид железа кроваво -красного цвета:
образует роданид железа кроваво -красного цвета:

|
|
|
Предел обнаружения железа – 0,5 мкг. Мешают фосфаты, арсенаты, оксалаты, тартраты, фториды, образующие с  устойчивые комплексные соединения.
устойчивые комплексные соединения.
Выполнение реакции: К 1-2 каплям раствора, содержащего ионы железа (III), добавляют каплю раствора  . Появляется кроваво-красное окрашивание раствора. Добавляют несколько капель изоамилового спирта или эфира и встряхивают. Органическая фаза окрашивается в красный цвет.
. Появляется кроваво-красное окрашивание раствора. Добавляют несколько капель изоамилового спирта или эфира и встряхивают. Органическая фаза окрашивается в красный цвет.
5.3 Частные реакции на катион Mn2+
Гидроксиды калия и натрия (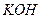 и
и 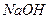 ) осаждают
) осаждают  c образованием белого осадка, растворимого в кислотах, но нерастворимого в щелочах:
c образованием белого осадка, растворимого в кислотах, но нерастворимого в щелочах:

Окисление иона  в анион
в анион  . Эта реакция позволяет открыть ион
. Эта реакция позволяет открыть ион  в присутствии ионов всех аналитических групп. В качестве окислителей можно использовать оксид свинца, персульфат аммония и другие с редокс-потенциалом больше 1,51 В.
в присутствии ионов всех аналитических групп. В качестве окислителей можно использовать оксид свинца, персульфат аммония и другие с редокс-потенциалом больше 1,51 В.
а) Окисление оксидом свинца ( ):
):

Условия реакции:
1. Реакция проводится при рН<2, при нагревании.
2. Хлорид марганца брать нельзя.
3. Анионы - восстановители мешают открытию ионов  в виде
в виде  , их следует предварительно удалить.
, их следует предварительно удалить.
б) Окисление персульфатом аммония  в присутствии
в присутствии  (катализатор). Ионы серебра (I) окисляются персульфатом аммония до ионов серебра (II):
(катализатор). Ионы серебра (I) окисляются персульфатом аммония до ионов серебра (II):

Далее ионы серебра (II) окисляют ионы марганца (II) до перманганат – иона, а ионы серебра при этом регенерируются:

Предел обнаружения марганца – 2 мкг. Мешают восстановители, в том числе хлорид - ион и большие количества  .
.
Выполнение реакции: К 5 - 6 каплям раствора  прибавляют каплю 2 М
прибавляют каплю 2 М  1 – 2 капли концентрированной
1 – 2 капли концентрированной  1-2 капли раствора
1-2 капли раствора  и нагревают. В нагретую окислительную смесь вносят при помощи стеклянной палочки минимальное количество раствора, содержащего ионы
и нагревают. В нагретую окислительную смесь вносят при помощи стеклянной палочки минимальное количество раствора, содержащего ионы  и не содержащего хлорид - ионов, перемешивают и наблюдают красно-фиолетовую окраску раствора.
и не содержащего хлорид - ионов, перемешивают и наблюдают красно-фиолетовую окраску раствора.
5.4 Частные реакции на катион Bi3+
Хлорид олова (II) в щелочной среде восстанавливает висмут (III) до металлического висмута (осадок черного цвета):

Следует избегать прибавления концентрированной щелочи и нагревания, так как в этих условиях может выпасть чёрный осадок металлического олова вследствие разложения гидроксокомплексов олова (II):

Если же избыток щелочи слишком мал, при стоянии может образоваться чёрный осадок оксида олова. Предел обнаружения висмута – 20 мкг.
|
|
|
Выполнение реакции: К 2-3 каплям раствора, содержащего ионы олова (II), прибавляют по каплям 30%-ный раствор 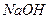 до образования осадка гидроксида олова (II) и последующего его растворения. К полученному раствору добавляют каплю раствора нитрата висмута. Образуется чёрный осадок.
до образования осадка гидроксида олова (II) и последующего его растворения. К полученному раствору добавляют каплю раствора нитрата висмута. Образуется чёрный осадок.
Иодид калия 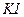 образует с ионами висмута (III) в кислой среде комплексные соединения состава
образует с ионами висмута (III) в кислой среде комплексные соединения состава  , где
, где 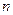 =1-6;
=1-6;  - осадок чёрного цвета, растворимый в избытке
- осадок чёрного цвета, растворимый в избытке 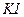 :
:

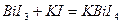
При сильном разбавлении раствора, содержащего  , получается оранжевый осадок соли
, получается оранжевый осадок соли  :
:

Предел обнаружения висмута – 0,5 мкг.
8-Оксихинолин с комплексным ионом  образует нерастворимое в воде оранжево-красное соединение
образует нерастворимое в воде оранжево-красное соединение  . В растворе должны отсутствовать
. В растворе должны отсутствовать  осаждающие
осаждающие  , а также окислители, окисляющие
, а также окислители, окисляющие  до
до  , в частности
, в частности  и
и  . Мешающее влияние окислителей устраняют, прибавляя
. Мешающее влияние окислителей устраняют, прибавляя 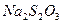 или
или  . Реакцию можно выполнить капельным методом. Предел обнаружения висмута – 1 мкг.
. Реакцию можно выполнить капельным методом. Предел обнаружения висмута – 1 мкг.
Выполнение реакции:
1) К 3-5 каплям раствора, содержащего ионы висмута (III), добавляют по каплям раствор 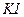 . Наблюдают образование осадка и его растворение в избытке
. Наблюдают образование осадка и его растворение в избытке 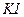 , при этом раствор окрашивается в оранжевый цвет.
, при этом раствор окрашивается в оранжевый цвет.
2) Полоску фильтровальной бумаги смачивают раствором  , после чего наносят каплю раствора, содержащего ионы висмута, каплю раствора реагента (смесь 8-оксихинолина и
, после чего наносят каплю раствора, содержащего ионы висмута, каплю раствора реагента (смесь 8-оксихинолина и 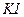 в массовых соотношениях 1:1). Образование оранжево-красного пятна указывает на присутствие висмута.
в массовых соотношениях 1:1). Образование оранжево-красного пятна указывает на присутствие висмута.
Дитизон в интервале рН 3 – 10 образует с ионами висмута (III) внутрикомплексное соединение. Дитизонаты висмута хорошо растворяются в 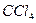 и
и 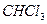 , растворы окрашены в оранжевый цвет. Предел обнаружения висмута – 0,5 мкг. В присутствии
, растворы окрашены в оранжевый цвет. Предел обнаружения висмута – 0,5 мкг. В присутствии  мешают только
мешают только  и
и  . Мешающее влияние
. Мешающее влияние  устраняют его окислением до
устраняют его окислением до  . Свинец из экстракта реэкстрагируется ацетатным буферным раствором с рН 3-4.
. Свинец из экстракта реэкстрагируется ацетатным буферным раствором с рН 3-4.
Выполнение реакции: К 1-2 каплям исследуемого раствора прибавляют 2-3 капли раствора  , доводят рН раствора до 9 раствором аммиака и экстрагируют 0,02 %-ным раствором дитизона в
, доводят рН раствора до 9 раствором аммиака и экстрагируют 0,02 %-ным раствором дитизона в 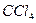 . Наблюдают оранжевое окрашивание экстракта.
. Наблюдают оранжевое окрашивание экстракта.
|
|
|
5.5 Частные реакции на катион Mg2+
Гидроксиды  образуют с
образуют с  белый аморфный осадок
белый аморфный осадок  , растворимый в кислотах и солях аммония.
, растворимый в кислотах и солях аммония.
Гидрофосфат натрия 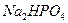 дает с катионом
дает с катионом  в присутствии
в присутствии  и
и  белый кристаллический осадок фосфата магния-аммония
белый кристаллический осадок фосфата магния-аммония  :
:

При рН>10 могут образоваться  и
и  . Рекомендуется к кислому анализируемому раствору прибавлять аммиак до рН~9. Из-за образования
. Рекомендуется к кислому анализируемому раствору прибавлять аммиак до рН~9. Из-за образования  рН раствора поддерживается постоянным.
рН раствора поддерживается постоянным.
Осадок растворяется в сильных кислотах и в уксусной кислоте:

Предел обнаружения магния – 10 мкг. Мешают многие ионы, образующие малорастворимые фосфаты; катионы первой группы не мешают.
Выполнение реакции: К 1-2 каплям раствора, содержащего ионы магния, прибавляют 2-3 капли 2 М 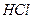 , 1 каплю раствора
, 1 каплю раствора 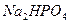 и при перемешивании по каплям прибавляют 2М
и при перемешивании по каплям прибавляют 2М 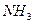 до появления запаха аммиака (рН~9). Выпадает белый кристаллический осадок.
до появления запаха аммиака (рН~9). Выпадает белый кристаллический осадок.
8-Оксихинолин (люминесцентная реакция). 8-Оксихинолин образует с ионами магния при рН 9-12 флуоресцирующий зелёным светом оксихинолинат. Предел обнаружения магния – 0,025 мкг. Интенсивность свечения повышается при обработке влажного пятна с оксихинолинатом магния раствором 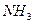 . Мешают
. Мешают 
Выполнение реакции: На фильтровальную бумагу наносят каплю раствора, содержащего ионы магния, и каплю этанольного раствора реагента. Образующийся оксихинолинат магния обрабатывают каплей 10%-ного раствора аммиака. При рассмотрении влажного пятна в ультрафиолетовом свете наблюдается зеленое свечение.
5.6 Частные реакции на катион Sb3+
Гидролиз. При разбавлении раствора выпадает белый осадок хлористого стибила (ион Sb3+ гидролизуется в большей степени, чем соли Bi3+):

К 2-3 каплям раствора хлорида сурьмы добавьте 5-10-кратный избыток дистиллированной воды. Выпадает белый коллоидный осадок.
Тиосульфат натрия 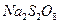 c катионом
c катионом  при нагревании образует красный осадок сероокиси сурьмы
при нагревании образует красный осадок сероокиси сурьмы  :
:


Восстановление иона  до металлической сурьмы:
до металлической сурьмы:

На очищенную наждачной бумагой цинковую, алюминиевую или железную пластину нанести каплю подкисленного соляной кислотой (рН 1-2) анализируемого раствора. Через 2-3 минуты поверхность пластины чернеет.
5.7 Частные реакции на катион Sb5+
Гидролиз. При разбавлении растворов солей сурьмы водой образуется белый осадок основной соли, растворимый в избытке соляной кислоты:

Гидроксиды натрия, калия и аммония образуют с  белый осадок метасурьмяной кислоты:
белый осадок метасурьмяной кислоты:

Металлы: цинк, олово, магний, железо действуют на  так же, как и на катион
так же, как и на катион  .(восстанавливают до металла):
.(восстанавливают до металла):
5Fe + 3SbCl5 Û 3Sb + 5FeCl3
Метиловый фиолетовый в солянокислых средах даёт с катионом  фиолетовое окрашивание.
фиолетовое окрашивание.
|
|
|
|
|
|


