 |
6.4.2. Метод ионно-электронных уравнений (метод полуреакций)
|
|
|
|
6. 4. 2. Метод ионно-электронных уравнений (метод полуреакций)
Этот метод применяется для подбора коэффициентов в уравнениях реакций, протекающих в растворах. Он основан на составлении уравнений процессов окисления и восстановления с помощью ионов и молекул, реально существующих в растворе. Степени окисления атомов не используют, а учитывают заряды ионов и характер среды (рН), в которой протекает ОВ-реакция. В качестве частиц среды в водных растворах могут принимать участие следующие частицы: Н+, ОН- и Н2О.
Таблица 5. 1
Схема участия частиц среды в ОВР в зависимости
от кислотности раствора
| Кислотность раствора (рН) | Исходные частицы | Продукты |
| Кислая среда (рН< 7) | Н+ и Н2О | Н2О и Н+ |
| Нейтральная среда (рН = 7) | Н2О | Н+ и (или) ОН- |
| Щелочная среда (рН> 7) | ОН- и Н2О | Н2О и ОН- |
Последовательность действий при подборе коэффициентов методом полуреакций следующая:
1. Написать уравнение в ионно-молекулярной форме, в котором сильные электролиты записывают в виде ионов, а слабые электролиты, газы и осадки – в виде молекул;
2. Определить кислотно-щелочность среды;
3. Определить частицы, изменившие свой заряд или состав, и записать полуреакции окисления и восстановления;
4. Составить материальный баланс для этих полуреакций, т. е. количество атомов каждого из присутствующих элементов в левой и правой частях уравнения должно быть одинаковым. В случае, когда исходные частицы содержат большее число атомов кислорода, чем полученные, то в кислой среде каждый атом кислорода связывается двумя ионами водорода образуя воду, а в нейтральной и щелочной средах – молекулой воды в два гидроксид-иона. Если же исходные частицы не содержат кислорода или содержат меньшее число атомов кислорода, чем полученные, то недостающее число атомов кислорода восполняют в нейтральной и кислой средах за счет молекул воды, а в щелочной – за счет двух ионов ОН-.
|
|
|
5. Уравнять полученные полуреакции по зарядам с участием электронов.
6. Составить электронный баланс между полуреакциями, учитывая, что количество принятых электронов должно равняться количеству отданных. Далее просуммировать полуреакции: сложить отдельно левые части и отдельно правые части уравнений. Если в суммарном уравнении имеются одинаковые частицы в левой и правой частях уравнения, то привести подобные (сократить).
7. Полученные коэффициенты перенести в молекулярное уравнение и проверить материальный баланс.
Рассмотрим метод ионно-электронных уравнений для уравнивания ОВР между KMnO4 и KNO2 в кислой, нейтральной и щелочной средах.
I. В кислой среде реакция протекает по уравнению:
KMnO4 + KNO2 + H2SO4 ®MnSO4 + KNO3 + K2SO4 + H2O
1. Записываем это уравнение в ионно-молекулярной форме. Для этого все сильные электролиты представляем в виде ионов, а слабый электролит H2O оставляем в виде молекул:
K++MnO4-+Na++NO2-+2H+ +SO42-®Na++NO3-+ Mn2++SO42- +2K++SO42-+H2O
2. В уравнении присутствуют ионы Н+, следовательно, реакция протекает в кислой среде.
3. Определяем частицы, изменившие свой заряд или состав:
MnO4-® Mn2+ и NO2-® NO3-
4. На основании этих превращений составляем материальный баланс с участием частиц среды. Ион MnO4- потерял 4 моля атомов кислорода, которые в кислой среде связываются 8 молями ионов водорода и превращаются в молекулы воды. Ион NO2- с участием воды приобрел 1 моль атомов кислорода:
|
|
|
MnO4- + 8H+ ® Mn2+ + 4H2O
NO2- + H2О ®NO3- + 2Н+
5. Полученные полуреакции необходимо уравнять по зарядам. В первом уравнении суммарный заряд слева равен (+7), а справа – (+2), значит, перманганат-ион присоединил 5 электронов и восстановился. Во втором уравнении слева (-1), а справа – (+1), следовательно, ион NO2- потерял 2 электрона и окислился:
MnO4- + 8H++ 5ē ® Mn2+ + 4H2O
NO2- + H2О –2ē ®NO3- + 2Н+
6. Для соблюдения электронного баланса первое уравнение необходимо умножить на 2, второе уравнение умножить на 5, после чего просуммировать уравнения:
 MnO4- + 8H++ 5ē ® Mn2+ + 4H2O ∙ 2
MnO4- + 8H++ 5ē ® Mn2+ + 4H2O ∙ 2
 NO2- + H2О – 2ē ®NO3- + 2Н+ ∙ 5
NO2- + H2О – 2ē ®NO3- + 2Н+ ∙ 5
2MnO4- + 16H+ +5NO2- + 5H2О ®2Mn2+ + 8H2O + 5NO3- + 10Н+
В левой и правой частях уравнения имеются одинаковые частицы: H+ и H2O. После их сокращения получаем сокращенное ионно-молекулярное уравнение:
2MnO4- + 6H+ +5NO2- ® 2Mn2+ + 3H2O + 5NO3-.
7. Далее переносим коэффициенты в исходное уравнение:
2KMnO4 + 5 KNO2 +3H2SO4 =2MnSO4 + 5 KNO3 + K2SO4 + 3 H2O
и проверяем материальный баланс.
II. В нейтральной среде реакция протекает по уравнению:
KMnO4 + KNO2 + H2O ®MnO2 + KNO3 + KOH
1. Записываем это уравнение в ионно-молекулярной форме. Сильные электролиты записываем в виде ионов, а слабый электролит H2O и малорастворимый MnO2 в виде молекул:
K+ + MnO4- + K+ +NO2- +H2O ®MnO2 + K++ NO3- + K+ + OH-
2. В уравнении присутствует Н2О, следовательно, реакция протекает в нейтральной среде.
3. Определяем частицы, изменившие свой заряд и состав:
MnO4- ® MnO2 и NO2- → NO3-
4. На основании этих превращений составляем материальный баланс с участием частиц среды. Ион MnO4- потерял 2 моля атомов кислорода, которые в нейтральной среде связываются 2 молями H2О и образуют 4 моля OН-. Ион NO2- с участием молекул воды приобрел 1 моль атомов кислорода:
MnO4- + 2H2О ® MnО2 + 4OН-
NO2- + H2О ®NO3- + 2 Н+
5. Полученные полуреакции необходимо уравнять по зарядам. В первом уравнении слева суммарный заряд равен (-1), а справа – (-4), значит, перманганат-ион присоединил 3 электрона и восстановился. Во втором уравнении слева суммарный заряд (-1), а справа – (+1), следовательно, ион NO2- потерял 2 электрона и окислился:
MnO4- + 2H2О+ 3ē ® MnО2 + 4OН-
NO2- + H2О – 2ē ®NO3- + 2 Н+
6. Для соблюдения электронного баланса первое уравнение необходимо умножить на 2, второе уравнение умножить на 3, после чего просуммировать уравнения:
|
|
|
 MnO4- + 2H2О+ 3ē ® MnО2 + 4OН- ∙ 2
MnO4- + 2H2О+ 3ē ® MnО2 + 4OН- ∙ 2
 NO2- + H2О –2ē ®NO3- + 2 Н+ ∙ 3
NO2- + H2О –2ē ®NO3- + 2 Н+ ∙ 3
 2MnO4- + 4H2О +3NO2- + 3 H2О ®2MnO2+8ОH- + 6H++3NO3-
2MnO4- + 4H2О +3NO2- + 3 H2О ®2MnO2+8ОH- + 6H++3NO3-
6H2O +2OН-
В правой части уравнения имеются 8ОH- и 6H+, которые в сумме образуют 6 молей H2O и 2 моля ионов OН-. В левой части уравнения имеется 7 молей H2О. После сокращения H2О в левой и правой частях уравнения получаем сокращенное ионно-молекулярное уравнение:
2MnO4- +3NO2- + H2О ® 2MnO2+2ОH- +3NO3-
7. Далее переносим коэффициенты в исходное уравнение:
2KMnO4 + 3 KNO2 +H2O =2MnO2 + 3 KNO3 + 2KOH
и проверяем материальный баланс.
III. В щелочной среде реакция протекает по уравнению:
KMnO4 + KNO2 + KOH ®K2MnO4 + KNO3 + H2O
1. Записываем это уравнение в ионно-молекулярной форме. Для этого все сильные электролиты представляем в виде ионов, а слабый электролит H2O оставляем в виде молекул:
K+ +MnO4- + K++NO2- +K++OH- ®2K++ MnO42- +K++NO3- + H2O
2. В уравнении присутствуют ионы OH-, следовательно, реакция протекает в щелочной среде.
3. Определяем частицы, изменившие свой заряд или состав:
MnO4- ® MnO42- и NO2- → NO3-
4. На основании этих превращений составляем материальный баланс с участием частиц среды. Ион MnO4- сохранил свой состав, но изменил заряд. Ион NO2- в щелочной среде с участием 2 молей OH- приобрел 1 моль атомов кислорода:
MnO4- ® MnO42-
NO2- + 2 OH-→ NO3- + Н2O
5. Полученные полуреакции необходимо уравнять по зарядам. В первом уравнении слева суммарный заряд равен (-1), а справа – (-2), значит, ион MnO4- присоединил 1 электрон и восстановился. Во втором уравнении слева (-3), а справа – (-1), следовательно, ион NO2- потерял 2 электрона и окислился:
MnO4- + ē ® MnO42-
NO2- + 2 OH- + 2ē → NO3- + Н2O
6. Для соблюдения электронного баланса первое уравнение необходимо умножить на 2, после чего просуммировать уравнения:
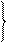 MnO4- + ē ® MnO42- ∙ 2
MnO4- + ē ® MnO42- ∙ 2
NO2- + 2 OH- + 2ē → NO3- + Н2O
 2MnO4- + NO2- + 2 OH- ® 2MnO42- + NO3- + Н2O
2MnO4- + NO2- + 2 OH- ® 2MnO42- + NO3- + Н2O
7. Далее переносим коэффициенты в исходное уравнение:
|
|
|
2KMnO4 + KNO2 +2KOH =2K2MnO4 + KNO3 + H2O
и проверяем материальный баланс.
В некоторых ОВР окислитель одновременно является и средой. Рассмотрим этот случай на примере реакции:
I2 + HNO3® HIO3 +NO2 +H2O
В этой реакции азотная кислота HNO3 содержит окислитель ион NO3- и создает кислую среду (наличие ионов H+).
1. Представим молекулярное уравнение в ионно-молекулярном виде. Простое вещество I2, газ NO2, и слабый электролит H2O оставляем в виде молекул:
I2 + H+ + NO3-® IO3- +NO2 +H2O
2. Далее составляем полуреакции окисления и восстановления. С учетом того, что реакция протекает в кислой среде, для соблюдения материального баланса используем ионы H+ и H2O:
NO3- + 2H+ + ē ®NO2 +H2O
I2 + 6H2O - 10ē ® 2IO3- + 12H+
3. Для соблюдения электронного баланса первое уравнение необходимо умножить на 10, после чего просуммировать уравнения:
 NO3- + 2H+ + ē ®NO2 +H2O ∙ 10
NO3- + 2H+ + ē ®NO2 +H2O ∙ 10
 I2 + 6H2O - 10ē ® 2IO3- + 12H+
I2 + 6H2O - 10ē ® 2IO3- + 12H+
10NO3- + 20 H+ + I2 + 6H2O®10NO2 +10 H2O +2 IO3- +12H+
После сокращения ионов H+ в левой и правой частях уравнения получим суммарное ионно-молекулярное уравнение:
10NO3- + 8 H+ + I2 ®10NO2 +4 H2O + 2 IO3-
4. Затем полученные коэффициенты перенесем в молекулярное уравнение реакции. Учитывая, что ионы NO3- и H+ входят в состав одного и того же соединения, а количество их разное, перед HNO3 ставится максимальный коэффициент, так как часть азотной кислоты расходуется на создание кислой среды. Таким образом, полное уравнение:
I2 + 10HNO3®2HIO3 +10NO2 +4H2O
Метод полуреакций позволяет уравнивать не только атомы окислителя и восстановителя, но и атомы водорода и кислорода, что значительно упрощает подбор дополнительных коэффициентов.
Вопрос о принципиальной возможности или невозможности окислительно-восстановительных реакций решается так же, как и для всех других. Реакция термодинамически разрешена, если она протекает с уменьшением свободной энергии Гиббса, т. е. DGхр< 0.
Раздел 6.
|
|
|


