 |
Определение молярной массы эквивалента цинка
|
|
|
|
Тверь. Типография ТГТУ
Ó Тверской государственный
технический университет, 2002
Определение молярной массы эквивалента цинка
Стр 1 из 12Следующая ⇒ Тверь. Типография ТГТУ
Ó Тверской государственный технический университет, 2002 |
ВВЕДЕНИЕ
Лабораторные работы являются одной из важнейших составных частей курса химии. Для их выполнения студенту необходимо ознакомиться с лабораторным оборудованием, измерительными приборами, а также с техникой проведения эксперимента.
Поскольку в химической лаборатории находятся электроприборы, газ, ядовитые и огнеопасные вещества, студенты должны строго соблюдать правила работы в химической лаборатории, правила техники безопасности и противопожарной безопасности, а также должны уметь оказывать первую помощь при несчастных случаях.
ПРАВИЛА РАБОТЫ В ХИМИЧЕСКОЙ ЛАБОРАТОРИИ
Общие правила работы в лаборатории
Выполнение лабораторных работ связано с использованием разнообразного оборудования, химических реактивов, химической посуды, которые при неумелом обращении способны нанести травмы и отравления. Поэтому работающие обязаны строго соблюдать правила техники безопасности и внутреннего распорядка.
1. Для успешной работы и лучшего усвоения темы необходима предварительная подготовка к лабораторной работе. Перед каждым занятием студент должен проработать по учебникам, пособиям или лекциям теоретический материал, относящийся к теме лабораторной работы, а также выполнить самостоятельную работу по заданию преподавателя.
2. Не разрешается входить в лабораторию в верхней одежде и категорически запрещается принимать пищу.
3. Для работы в лаборатории студенту отводится постоянное рабочее место, которое следует содержать в чистоте и порядке, так как грязь нередко бывает причиной искажения результатов опытов.
|
|
|
4. Не следует загромождать рабочий стол посторонними вещами. На рабочем столе должны находиться только необходимое оборудование, посуда и лабораторный журнал.
5. Записи всех проведенных опытов, полученных экспериментальных результатов производят в специальном лабораторном журнале.
6. По окончании работы следует тщательно вымыть посуду, выключить электроприборы, проверить закрыт ли водопроводный кран, вытереть влажной тряпкой поверхность стола и вымыть руки.
Реактивы и правила обращения с реактивами
1. По степени чистоты реактивы делятся на технические (техн.), чистые (ч.), чистые для анализа (ч.д.а.), химически чистые (х.ч.).
2. Необходимые для работы реактивы выставляются на рабочий стол или на полки рабочего стола. - Концентрированные кислоты, а также растворы вредных и неприятно пахнущих веществ, хранятся в вытяжном шкафу. - Часть реактивов для общего пользования может находиться на специальных полках или на общем столе.
3. Реактивы общего пользования, в том числе реактивы, хранящиеся в вытяжном шкафу, не следует уносить к себе на рабочее место.
4. Не следует пользоваться реактивом, не снабженным этикеткой! Для проведения опыта нужно брать указанное в руководстве количество реактива. Если не указано количество реактива, то берут возможно меньшее количество.
5. Сухие реактивы отбирают шпателем, жидкие - пипетками. При отборе жидкого реактива из склянки, следует ее держать так, чтобы этикетка была сверху.
6. Излишек реактива, ни в коем случае нельзя вливать (высыпать) обратно в сосуд, из которого он был взят. Его надо сдавать лаборанту или студенту, которому он нужен.
7. Нельзя брать одной и той же пипеткой или шпателем разные реактивы, во избежание их загрязнения.
Меры предосторожности при работе в лаборатории
1. К проведению опыта следует приступать после внимательного ознакомления с его содержанием и уяснения техники его выполнения.
|
|
|
2. Опыты с ядовитыми и неприятно пахнущими веществами следует проводить в вытяжном шкафу.
3. Опыты с легко воспламеняющимися веществами необходимо проводить вдали от огня и нагревательных приборов.
4. При разбавлении концентрированных кислот, особенно серной, следует вливать небольшими порциями кислоту в воду, а не наоборот.
5. Не следует наклоняться над нагреваемой жидкостью или сплавляемыми веществами, во избежание попадания брызг на лицо.
6. Не следует нагревать дно пробирки во избежание выброса содержимого. Отверстие пробирки должно быть направлено в сторону противоположную от себя и окружающих.
7. При определении выделяющегося газа по запаху нужно легким взмахом кисти направлять струю его к себе и осторожно вдохнуть.
8. В случае воспламенения горючих веществ, следует засыпать пламя песком, или накрыть кошмой (одеялом, куском ткани), но не следует пользоваться водой.
9. Концентрированные кислоты и щелочи ни в коем случае не выливать в раковину, а сливать в специальные склянки. Бумагу и другие твердые отходы следует бросать в урны.
10. Остатки щелочных металлов следует сдавать лаборанту и ни в коем случае не бросать в раковину или в урну.
Оказание первой помощи
1. При попадании на кожу концентрированных кислот следует тотчас же смыть ее большим количеством воды из крана, а затем обработать пораженный участок 2% -м раствором питьевой соды.
2. При попадании на кожу щелочи надо тщательно промыть водой до прекращения ощущения скользкости, а затем - 2%-м раствором уксусной кислоты.
3. При термических ожогах на пораженный участок накладывают повязку, пропитанную 2%-м раствором перманганата калия (KMnO4)или 3%-м раствором танина.
4. При отравлении хлором, бромом, сероводородом, окисью углерода необходимо вывести пострадавшего на воздух.
5. При всех несчастных случаях следует немедленно обратиться к преподавателю и дежурному лаборанту.
Лабораторный журнал и
Оформление лабораторных работ
1. Лабораторный журнал должен быть подписан, т.е. на его обложке должны быть написаны фамилия студента, его инициалы, номер группы и название предмета, а также номер варианта.
|
|
|
2. Перед каждым лабораторным занятием студент должен изучить соответствующий раздел учебника, конспекта лекций и описание лабораторной работы.
3. Дома необходимо законспектировать лабораторную работу. Можно рекомендовать следующую схему записи:
- дата и название выполняемой лабораторной работы;
- цель работы;
- теоретические сведения (краткий конспект);
- название каждого опыта и его номер;
- уравнения реакций, схема прибора, таблицы;
4. Записи в журнале производят лаконично, аккуратно и обязательно непосредственно после проведения опыта, запись каждого опыта необходимо завершать соответствующим выводом.
5. Перед выполнением лабораторной работы всем студентам необходимо получить допуск у преподавателя, для которого необходимо:
1) проработать теоретический материал по данной теме;
2) решить домашние задачи согласно варианту;
3) оформить лабораторную работу (согласно п.3).
Лабораторная работа №1
ОПРЕДЕЛЕНИЕ МОЛЯРНОЙ МАССЫ ЭКВИВАЛЕНТА ЦИНКА
(Глинка Н.Л.,2000, 1.1-1.5, Коровин Н.В., 2000, §§1 - 3)
Цель занятия: научиться вычислять молярную массу эквивалента вещества и определять ее экспериментально.
Теоретические сведения
Единицей количества вещества является моль.
Моль – это количество вещества, которое содержит столько структурных единиц (молекул, атомов, ионов, катионов, электронов, эквивалентов и т.д.), сколько атомов содержится в 12 г изотопа углерода –12, а именно, 6,02.1023 (число Авогадро).
Эквивалентом элемента или вещества называется такое его количество, которое соединяется с одним молем атомов водорода или замещает один моль водорода в химических реакциях. Массу одного моля эквивалентов называют молярной массой эквивалентов вещества (Мэ), г/моль.
Пример. В веществах HCl, H2O, NH3 с одним моль атомов водорода связан один моль атомов Cl, 1/2 моль кислорода и 1/3 моль азота, следовательно, эквиваленты этих элементов в указанных соединениях соответственно равны 1, 1/2 и 1/3 моль (1, ½, ⅓ – фактор эквивалентности). В рассмотренном примере молярная масса эквивалента Мэ(Н) = 1 г/моль, Мэ(О) = 8 г/моль, Мэ(N) = 4,6 г/моль.
|
|
|
Молярная масса эквивалента элемента в соединении не является величиной постоянной, зависит от валентности элемента в данном соединении и выражается уравнением:
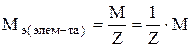 ,
,
где М – молярная масса элемента, г/моль; Z – валентность элемента в данном соединении; 1/z – фактор эквивалентности.
Молярные массы эквивалентов сложных соединений рассчитываются по формулам 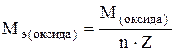
где n – число атомов кислорода; Z – валентность кислорода
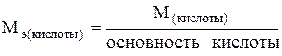
где основность кислоты – это общее число атомов водорода или число атомов водорода, замещенных в реакции атомами металла. Например, основность фосфорной кислоты в реакции
H3PO4 + 2 NaOH = Na2HPO4 + 2 H2O
равна 2, т.к. 2 атома водорода заместилось атомами натрия.
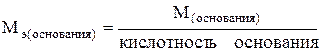

где кислотность основания – это общее число OH- - групп или число OH- - групп, замещенных в процессе реакции кислотными остатками. Например, кислотность гидроксида алюминия в реакции:
Аl(ОН)3 + 2 НС1 = А1(OH)С12 + 2 H2O
равна 2, т.к. 2 группы OH- заместились двумя хлорид-ионами (Cl-).
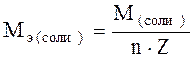
где n – число атомов металла; Z – валентность металла.
Согласно закону эквивалентов массы (объемы) всех веществ, реагирующих между собой в химических реакциях, прямо пропорциональны их молярным массам эквивалентов (молярным объемам эквивалентов):
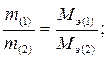
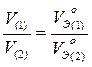 ;
; 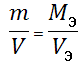
где m1 и m2 – масса веществ, вступивших или получившихся в результате реакции, г; Mэ1, Мэ2 – молярные массы эквивалентов этих веществ, г/моль; V1, V2-объемы газообразных веществ при н.у.; V10 и V20 - объем, который занимает эквивалент вещества при н.у.
Молярный объем эквивалента вещества Vэо – это объем, занимаемый одним моль эквивалентом газообразного вещества, при нормальных условиях.
Газовые законы и расчет молярных масс газообразных веществ
|
|
|
