 |
Правило смешивания (правило «креста»)
|
|
|
|
Применяют для быстрого расчета масс или объемов при приготовлении раствора из двух растворов различной концентрации
Задача: Рассчитать и приготовить 3 кг 30% раствора H2SO4 из 98% раствора H2SO4 (ρ=1,86 г/мл) и воды. Рассчитать объем 98% раствора и объем воды необходимые для приготовления заданного раствора.
Составляем крест:

 H2SO4 98% 30 г H2SO4
H2SO4 98% 30 г H2SO4
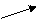
 30%
30%
H2O 0 %  68 г H2O
68 г H2O
 98 г 30% р-ра
98 г 30% р-ра
В левый столбик записываем исходные растворы и их процентные концентрации, причем процентная концентрация воды равна 0%. Далее между ними посередине записываем ту концентрацию, которую необходимо приготовить, и по направлению стрелок вычитаем из большего значения меньшее и по диагонали записываем полученное число. В правой части получили весовые соотношения двух исходных растворов. Общая масса полученного 30%-го раствора равна сумме 30 г 98% H2SO4 + 68 г H2O = 98 г.
Для приготовления 98 г (30%) р-ра необходимо взять 30 г H2SO4 (98%) и добавить 68 г воды.
Затем находим массу m 98% р-ра H2SO4, необходимую для приготовления 3 кг 30 % р-ра H2SO4. Составляем пропорцию:
1) Для приготовления
98 г (30%) нужно взять - 30 г (98%) р-ра H2SO4
3000 г (30%) - X г
X =  г (98 % р-ра H2SO4).
г (98 % р-ра H2SO4).
Рассчитываем объем:  мл (98 % р-ра H2SO4)
мл (98 % р-ра H2SO4)
2)  г
г
 =1 г/мл, следовательно, V
=1 г/мл, следовательно, V  =2080 мл = 2,08 л.
=2080 мл = 2,08 л.
Итак, для приготовления 3 кг 30% р-ра H2SO4 нужно отмерить 2,08 л дистиллированной воды и добавить 0,495 л 98% H2SO4.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Опыт №1. Приготовление раствора заданной концентрации.
Задание: из сухой соли и дистиллированной воды приготовить, согласно варианту (см.табл.) раствор заданной концентрации. Рассчитать массу сухой соли и объем воды, необходимые для приготовления заданного раствора.
| № п.п | Опыт №1 | Опыт №2 |
| 50 г 5% р-ра CuSO4 55 г 4% р-ра K2Cr2O7 53 г 4,5% р-ра Na2CO3 52 г 5% р-ра K2CrO4 54 г 3,5% р-ра Na2SO4 57 г 5,5% р-ра CuSO4 | 60 г 3% р-ра CuSO4 65 г 3% р-ра K2Cr2O7 60 г 2,5% р-ра Na2CO3 61 г 3% р-ра K2CrO4 55 г 2,5% р-ра Na2SO4 60 г 3,5% р-ра CuSO4 |
|
|
|
Ход работы:
1. Сделать расчет.
2. Технология приготовления заданной %-ой концентрации раствора.
· На технических весах взвесить рассчитанную массу соли и перенести ее в коническую колбу.
· Цилиндром отмерить рассчитанный объем дистиллированной воды и перенести в ту же колбу.
· Содержимое колбы перемешать до полного растворения соли.
3. Измерить плотность полученного раствора ареометром.
4. Зарисовать коническую колбу, цилиндр, ареометр.
Опыт №2.
Задание: Из раствора, полученного в опыте №1 и дистиллированной воды приготовить раствор заданной концентрации (см.таблицу), используя правило «креста». Рассчитать объем раствора и объем воды, которые необходимо смешать, для получения раствора. Измерить плотность приготовленного раствора ареометром.
Домашнее задание:
Рассчитать все виды концентрации: См, Сm, Сн, Nр.в-ва и Nр-ля. Данные взять из опыта №1и 2.
Лабораторная работа № 3
ОПРЕДЕЛЕНИЕ ЭНТАЛЬПИИ РЕАКЦИИ НЕЙТРАЛИЗАЦИИ
(Глинка Н.Л.,2000, 6.1, Коровин Н.В., 2000, §§ 5.1 – 5.4)
Цель занятия: выполнить калориметрические измерения и термодинамические расчеты, связанные с энергетикой химических процессов.
Теоретические сведения
Химический процесс, фазовые превращения сопровождаются энергетическими изменениями. Законы взаимного превращения различных видов энергии, а также состояние химического равновесия и зависимость его от различных факторов изучает наука – химическая термодинамика.
Химическая термодинамика базируется на законах.
I закон термодинамики: Теплота, сообщенная системе расходуется на изменение внутренней энергии D U и работы расширения или сжатия системы А.
Q = DU + A, A = p DV
Q = DU + p DV
Внутренняя энергия U – это функция состояния системы, включающая энергию движения атомов и молекул, электронов и ядер в атомах, внутриядерную энергию, энергию межмолекулярного взаимодействия и другие виды энергий, за исключением кинетической и потенциальной энергии системы, как целого.
|
|
|
Абсолютную величину запаса внутренней энергии химической системы измерить невозможно. Определяют изменение внутренней энергии системы при переходе её из начального в конечное состояние (из исходных веществ в продукты реакции):
DU = Uк – Uн
Если процесс идёт с поглощением тепла, внутренняя энергия возрастает, если с выделением, то уменьшается.
В изобарном процессе (p = const), U + pV = H – функция состояния, называемая энтальпия(теплосодержание). Qp = DH
В изохорном процессе (V = const) QV = DU.
Раздел термодинамики, изучающий тепловые эффекты называется термохимией.
Тепловым эффектом реакции Q называется количество тепла, поглощаемое или выделяемое в процессе химической реакции (кДж).
Если процесс идет с выделением тепла (экзотермический), тепловой эффект условно берется со знаком плюс (+Q), если тепло поглощается (эндотермический процесс) – со знаком минус (–Q).
При записи термохимических уравнений реакции указывается тепловой эффект с соответствующим знаком, агрегатное состояние вещества; допускаются дробные коэффициенты:
H 2 (г) + 1/2 О 2 (г) = Н 2 О(ж) + 285,8 кДж/моль.
Стандартной теплотой образования ( DНо298) называется тепловой эффект образования 1 моль сложного вещества из простых веществ, находящихся в устойчивом агрегатном состоянии при стандартных условиях:
tо = 25 оC (298 K); P = 101,3 кПа.
Стандартные энтальпии образования простых веществ принимают равными нулю: DНоСа(к) = 0; DНоО 2 (г)= 0.
Для экзотермических процессов DH < 0, для эндотермических – DH > 0.
Основными законами термохимии являются:
1. Закон Лавуазье-Лапласа: энтальпия разложения сложного вещества равна по абсолютной величине, но противоположна по закону энтальпии образования этого вещества из продуктов разложения DНразл = – DН обр.
2. Закон Гесса: тепловой эффект реакции, протекающий при постоянных давлении и температуре, не зависит от пути протекания процесса, а зависит только от начального и конечного состояния веществ.
Для расчётов удобно пользоваться следствием из закона Гесса:
|
|
|
тепловой эффект химической реакции равен алгебраической сумме теплот образования продуктов реакции за вычетом алгебраической суммы теплот образования исходных веществ, с учётом стехиометрических коэффициентов.
DНх.р=S nDНобр. прод – S nDНобр. исх. вещ-в
Пример:
СН 4 (г) + 2О 2 (г) = 2Н 2 О (ж) + СО 2 (г)
D Н ох.р = D Н ообр СО 2 (г) + 2D Н ообр Н 2 О (ж) – D Н ообр СН 4 (г)
Большинство химических процессов протекают самопроизвольно в сторону уменьшения запаса внутренней энергии или энтальпии системы. Но известны и такие процессы, которые протекают самопроизвольно без изменения внутренней энергии системы, движущей силой таких процессов является энтропия S системы. Энтропия характеризует беспорядок в системе, чем выше беспорядок, тем выше энтропия. В изолированных от внешней среды системах процессы протекают самопроизвольно в направлении увеличения энтропии (DSх.р >0). Энтропия реакции рассчитывается по следствию из закона Гесса и имеет единицу измерения Дж/моль.К.
DSх.р= SnSoобр. прод. – SnSoобр. исх. вещ-в
Таким образом, существуют два основных фактора самопроизвольного протекания процессов:
1) уменьшение внутренней энергии или энтальпии системы (DU<0; DН<0);
2) увеличение беспорядка или энтропии системы (DS > 0).
В термодинамике существует функция, которая отражает влияние на направление процесса двух рассмотренных факторов одновременно. Такой функцией для процессов, протекающих при постоянной температуре и давлении, является изобарно-изотермический потенциал G (или энергия Гиббса, свободная энергия системы, кДж).
Изменение изобарно-изотермического потенциала химической реакции можно рассчитать по формуле Гиббса:
DGх.р= DНх.р– Т DSх.р,
где Т – абсолютная температура процесса.
DG х.р характеризует общую движущую силу процесса. Если процесс протекает в стандартных условиях, то DG ох.р рассчитывается также по следствию из закона Гесса.
Величина и знак DG х.р характеризуют принципиальную возможность протекания химического процесса. Если DG х.р <0, процесс протекает самопроизвольно при данных условиях.
|
|
|
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Задание. Определить теплоту нейтрализации сильной кислоты сильным основанием и рассчитать энергию Гиббса данной реакции.
Согласно теории электролитической диссоциации нейтрализация сильной кислоты сильным основанием в разбавленном растворе отвечает ионно-молекулярному уравнению:
Н+ + ОН- = Н2О.
H2SO4 + NaOH = NaHSO4 + H2O
Для проведения реакции используют калориметрическую установку (рис.2).

| Рис.2. Калориметрическая установка: 1 – внешний изолирующий сосуд; 2 – калориметрический стакан; 3 – реакционная смесь; 4 – подставка; 5 – термометр; 6 – мешалка; 7 – воронка. |
Во внутренний стакан калориметра налить 50 мл 1 н. раствора щёлочи замерив объём раствора цилиндром. Измерить температуру раствора щёлочи с точностью до 0,1 оС. В другой мерный цилиндр налить такой же объём 1 н. раствора кислоты. Быстро влить кислоту в калориметрический стакан и перемешивая раствор мешалкой замерять изменение температуры через каждые 30 секунд в течение 4,5 минут. Показания термометра определять с точностью до 0,1ОС. Данные опыта занести в табл. 2.
 Таблица 2
Таблица 2
Результаты опыта
| Время τ, мин | 0,5 | 1,0 | 1,5 | 2,0 | 2,5 | 3,0 | 3,5 | 4,0 | 4,5 | |
| Температура t,0С |
Построить график зависимости t,ОС - τ, мин. На рис.3 приведен примерный вид этого графика. По графику нужно определить величину Δt, для этого экстраполируют линии АВ и СD. Точка К равноудалена от tm (максимальная температура) и tн (начальная температура). Затем проводим через точку К прямую, параллельную оси X до пересечения ее с линией ВС, затем, через точку Р проводим перпендикулярную оси Y прямую (участок EF). Δt находим как разность tк - tн.

| Рис.3. График изменения температуры со временем. Масштаб Время: 4 клетки – 1 мин Температура с разрывом графика: 1 клетка – 1оС |
Записать уравнение реакции нейтрализации и рассчитать D Н ох.р, пользуясь следствием из закона Гесса и данными табл. 3.
Таблица 3
|
|
|


