 |
1. Реакции радикального замещения у насыщенного атома углерода (SR).
|
|
|
|
1. Реакции радикального замещения у насыщенного атома углерода (SR).
В насыщенных углеводородах (алканах и циклоалканах) имеются только SP3-гибридизованные атомы углерода. Для них характерны прочные неполярные С− С и почти неполярные С− Н δ -связи. Эти связи не склонны к гетеролитическому разрыву под действием электрофильных или нуклеофильных реагентов. Поэтому для насыщенных углеводородов характерны реакции радикального замещения (SR). Они протекают по свободно-радикальному механизму при участии высокоэнергетических радикалных частиц. Так идет галогенирование насыщенных углеводородов при облучении. Рассмотрим реакцию монохлорирования метана, которая идет по механизму радикального замещения (SR):
CH4 + Cl2  CH3Cl + HCl
CH3Cl + HCl
Приведенное уравнение отражает суммарный процесс, который включает несколько стадий:
1. Инициирование – гомолитический разрыв связи в реагенте под действием облучения, образование радикалов:
Cl 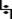 Cl → Cl• + Cl•
Cl → Cl• + Cl•
2. Рост цепи – атака радикалом молекулы субстрата; гомолитический разрыв связи С− Н в субстрате; образование новой молекулы и нового радикала:
CH3 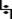 H + •Cl à CH3• + HCl
H + •Cl à CH3• + HCl
CH3• + Cl 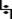 Cl à CH3Cl + Cl• и т. д.
Cl à CH3Cl + Cl• и т. д.
На каждой стадии роста цепи образуется продукт реакции и свободный радикал, который атакует новые молекулы, т. е. происходит цепная реакция.
3. Обрыв цепи возможен при взаимодействии двух любых радикалов:
Cl• + Cl• = Cl2; CH3• + Cl• = CH3Cl; CH3• + CH3• = C2H6
Галогенирование алканов, содержащих неэквивалентные количества атомов Н, происходит в соответствии с правилом региоселективности:
 Предпочтительное протекание реакции по одному из нескольких возможных реакционных центров молекулы, называется региоселективностью.
Предпочтительное протекание реакции по одному из нескольких возможных реакционных центров молекулы, называется региоселективностью.
|
|
|
Радикальной атаке подвергаются третичные углеродные атомы, затем вторичные и в последнюю очередь первичные.
2. Реакции, идущие по механизму электрофильного присоединения.
Ненасыщенные углеводороды – алкены, циклоалкены, алкины проявляют способность к реакциям присоединения, т. к. содержат двойные и тройные связи. Однако, для многих биохимических процессов более важной является двойная связь – её возникновение и превращения. В связи с этим реакции электрофильного присоединения будут рассмотрены на примере алкенов.
Механизм реакции: при сближении реагента с π -связью его молекула поляризуется с образованием активной электрофильной частицы. Эта частица затем атакует π -связь. В результате образуется устойчивый π -комплекс. Далее происходит:
1) гетеролитический разрыв связи в реагенте;
2) присоединение электрофила к молекуле;
3) отщепление нуклеофильной частицы и образование σ -комплеса (карбокатиона).
Затем образовавшийся нуклеофил атакует карбокатион и присоединяется в транс-положение. Так получается продукт реакции:
нуклеофил
|
|

 |  |
3. Реакции электрофильного замещения
Механизм таких реакций включает следующие стадии:
1. генерирование электрофильной частицы с помощью катализатора:
2. атака электрофилом бензольного ядра и образование π -комплекса;
3. образование σ -комлекса: электрофил “забирает” два электрона π -системы и образует σ -связь с одним из атомов углерода бензольного кольца. Ароматичность нарушается, т. к. этот атом углерода переходит в sp 3 -гибридизованное состояние;
4. отщепление протона от σ -комплекса, восстановление ароматической системы;
|
|
|
5. связывание отщепившегося протона с нуклеофилом.
 |
Место вступления электрофильного заместителя определяется характером уже присутствующих – одного или нескольких заместителей в бензольном цикле. Заместители делятся на 2 группы:
а) заместители 1 рода (орто- пара- ориентанты), облегчают (ускоряют) вступление электрофильного заместителя в орто- и пара- положение по отношению к себе. Ориентанты даются в порядке убывающей ориентирующей способности.
– Оˉ, − NR2; − NHR; − NH2; – OH; –OR; − CH3; алкины, алкены, − I; − Br; − Cl; − F.
Эти группы, проявляющие положительный индуктивный эффект и положительный мезомерный эффект.
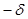
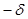
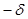
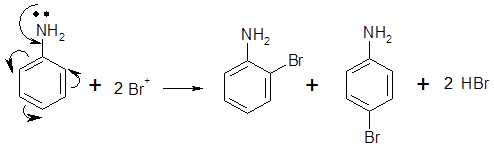
б) заместители 2-го рода (мета-ориентанты) затрудняют (замедляют) вступление электрофильного заместителя в мета - положение
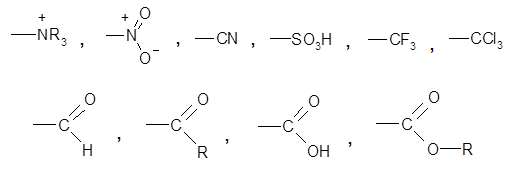
Это группы, проявляющие отрицательный индуктивный или отрицательный мезомерный эффекты.
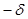 |
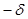

|
|
|


