 |
Элементы системы регуляции вентиляции
|
|
|
|
Система регуляции вентиляции состоит из трех основных звеньев:
1) рецепторы, воспринимающие информацию о газовом составе крови и ее КОС и передающие ее в регуляторный центр;
2) регуляторный центр;
3) эффекторы — дыхательные мышцы.
Регуляторный центр. Вентиляция — тот удивительный процесс, который может регулироваться как автоматически, без участия сознания, так и сознательно, подчиняясь волевому усилию. Это связано с тем, что дыхательные мышцы — обычные поперечно-полосатые мышцы, деятельность которых, как известно, управляется корой головного мозга.
Автоматизм дыхания обусловлен зарождением импульсов в стволе мозга. Считается, что дыхательные центры расположены в варолиевом мосту и продолговатом мозге и представляют собой диффузные скопления нескольких групп нейронов.
В ретикулярной формации находится медуллярный дыхательный центр, состоящий из дорсальной и вентральной зон. Нейроны дорсальной зоны активизируются при вдохе, вентральная зона связана с выдохом. Нейронам дорсальной (инспираторной) зоны свойствен автоматизм (подобный автоматизму проводящей системы сердца). Нарастание импульсации от инспираторных нейронов может быть прервано тормозящими импульсами из пневмотаксического центра, вследствие чего вдох укорачивается и растет ЧДД. Вентральная (экспираторная) зона при спокойном дыхании не активна (как уже упоминалось, при спокойном дыхании выдох пассивен).
В нижних отделах варолиевого моста расположен апнейстический центр. Перерезание ствола мозга животных непосредственно выше этого центра вызывает апнейзисы — длительные судорожные вдохи, прерываемые кратковременными выдохами. По-видимому, апнейстический центр возбуждает инспираторную зону, удлиняя время генерирования ее потенциалов действия. Точных данных о роли этого центра в нормальном дыхании нет, но иногда при тяжелых поражениях мозга у больных может возникать апнейстическое дыхание.
|
|
|
В верхних отделах варолиевого моста расположен пневмотаксический центр. Его импульсы подавляют вдох, регулируя частоту и глубину дыхания. Нормальный ритм дыхания может сохраняться и в отсутствие этого центра, по-видимому он связан лишь с «тонкой» настройкой дыхательного ритма.
На вентиляцию легких может влиять, как указано выше, кора головного мозга, а также лимбическая система и гипоталамус (в частности, при аффективных состояниях).
Эффекторы — дыхательные мышцы, к которым относят диафрагму, межреберные мышцы, мышцы брюшной стенки и вспомогательные мышцы (например, грудино-ключично-сосцевидные). Для нормальной вентиляции очень важна координированная работа этих мышц, что обеспечивается регуляторным центром.
Рецепторы.
Центральные хеморецепторы. Важнейшие из них расположены у вентральной поверхности продолговатого мозга около выходов IX и X пар черепно-мозговых нервов. Обработка этих центров растворами H+ или CO2 через несколько секунд приводит к гипервентиляции. Центральные хеморецепторы омываются внеклеточной жидкостью головного мозга и реагируют на ее pH. Состав этой жидкости зависит в наибольшей степени от состава СМЖ, а также от местного кровотока и метаболизма. СМЖ отделена от крови гематоэнцефалическим барьером (ГЭБ), плохо проницаемым для H+ и 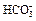 , но свободно пропускающим молекулярный CO2. При повышении pCO2 в крови CO2 диффундирует в СМЖ, в результате чего в СМЖ накапливаются H+ (благодаря реакциям
, но свободно пропускающим молекулярный CO2. При повышении pCO2 в крови CO2 диффундирует в СМЖ, в результате чего в СМЖ накапливаются H+ (благодаря реакциям  ), стимулирующие хеморецепторы. Следующая за этим гипервентиляция снижает pCO2 и, следовательно, повышает pH СМЖ. Повышение pCO2 (гиперкапния) в артериальной крови приводит к расширению сосудов мозга, что способствует диффузии CO2 в СМЖ, гипокапния же (снижение pCO2) вызывает сужение сосудов. pH СМЖ в норме составляет 7,32, ее буферная емкость невелика (из-за низкого содержания белков), поэтому pH СМЖ в большей степени зависит от pCO2, чем pH крови. При длительном снижении pH СМЖ (24-48 часов) в нее переходят бикарбонаты (
), стимулирующие хеморецепторы. Следующая за этим гипервентиляция снижает pCO2 и, следовательно, повышает pH СМЖ. Повышение pCO2 (гиперкапния) в артериальной крови приводит к расширению сосудов мозга, что способствует диффузии CO2 в СМЖ, гипокапния же (снижение pCO2) вызывает сужение сосудов. pH СМЖ в норме составляет 7,32, ее буферная емкость невелика (из-за низкого содержания белков), поэтому pH СМЖ в большей степени зависит от pCO2, чем pH крови. При длительном снижении pH СМЖ (24-48 часов) в нее переходят бикарбонаты ( ), и pH СМЖ возвращается к норме, хотя в крови может сохраняться гиперкапния и ацидоз. Поскольку pH СМЖ быстрее возвращается к норме и именно этот параметр оказывает преимущественное влияние на вентиляцию и paCO2, то у больных с длительной гиперкапнией (например, при бронхиальной астме) этот механизм регуляции теряет свое значение (поскольку в этом случае при росте paCO2 pCO2 и pH в ликворе остается нормальным).
), и pH СМЖ возвращается к норме, хотя в крови может сохраняться гиперкапния и ацидоз. Поскольку pH СМЖ быстрее возвращается к норме и именно этот параметр оказывает преимущественное влияние на вентиляцию и paCO2, то у больных с длительной гиперкапнией (например, при бронхиальной астме) этот механизм регуляции теряет свое значение (поскольку в этом случае при росте paCO2 pCO2 и pH в ликворе остается нормальным).
|
|
|
Периферические хеморецепторы находятся в каротидных тельцах, расположенных в области бифуркации общих сонных артерий, и в аортальных тельцах, залегающих в дуге аорты. Наибольшую роль в регуляции дыхания среди периферических хеморецепторов играют каротидные тельца. Периферические хеморецепторы реагируют на снижение pO2, pH и на повышение pCO2 артериальной крови. Особо важна реакция периферических хеморецепторов на pO2. При его снижении до 60 мм рт. ст. и ниже периферические хеморецепторы чрезвычайно быстро реагируют увеличением частоты импульсации. Гипервентиляция, развивающаяся при гипоксии, объясняется именно реакцией периферических хеморецепторов. В их отсутствие гипоксемия, наоборот, вызывает гиповентиляцию через угнетение дыхательных центров. Снижение pH крови любого происхождения стимулирует каротидные (но не аортальные) тельца, что тоже приводит к гипервентиляции.
У здоровых людей ведущую роль в регуляции вентиляции играет реакция центральных хеморецепторов (регуляторный, или дыхательный, центр) на уровень pCO2. Этот механизм регуляции наиболее новый в филогенетическом отношении, весьма чувствительный, однако недостаточно надежен и может легко угнетаться повреждающими воздействиями (отек мозга, отравление психотропными ядами и т.д.). В случае угнетения этого механизма, когда дыхательный центр уже не реагирует на гиперкапнию, развивается (при дыхании атмосферным воздухом) гипоксия, и при снижении pO2 до уровня 60 мм рт. ст. и ниже начинает работать другой механизм регуляции дыхания — по pO2 с участием периферических хеморецепторов. Этот механизм более старый в филогенетическом отношении, включается довольно поздно (pO2=60 мм рт. ст. — уже выраженная гипоксия), но является более надежным. Однако при дыхании атмосферным воздухом гипервентиляция не может в достаточной мере повысить pO2, зато приведет к гипокапнии (см. далее).
|
|
|
Рецепторы легких делятся на 3 типа.
1. Легочные рецепторы растяжения находятся в гладких мышцах дыхательных путей и реагируют на растяжение легких. Возбуждение этих рецепторов приводит к уменьшению ЧДД в результате увеличения времени выдоха (инфляционный рефлекс Геринга-Брейера). У взрослых этот рефлекс вызывается только при достижении ДО 1л.
2. Ирритантные рецепторы реагируют на едкие газы, табачный дым, пыль и холодный воздух. Возбуждение этих рецепторов приводит к сужению бронхов, гиперпноэ, чиханию, кашлю и ларингоспазму.
3. J-рецепторы (юкстакапиллярные) залегают в альвеолярных стенках около[2] капилляров. Раздражение этих рецепторов вызывает частое поверхностное дыхание вплоть до его остановки при сильном их раздражении. Возможно, они играют определенную роль в возникновении одышки при интерстициальном отеке легких и повышении КД в легочном сосудистом русле.
Кроме выше перечисленных рецепторов, в регуляции вентиляции принимают определенное участие рецепторы суставов и мышц (движение конечностей, даже пассивное, может стимулировать дыхание), мышечные веретена, особенно дыхательных мышц (могут обусловливать ощущение одышки, когда дыхание требует больших усилий), артериальные барорецепторы (повышение АД приводит к рефлекторной гиповентиляции, а понижение — к гипервентиляции), болевые и температурные рецепторы (в ответ на боль часто наблюдается задержка дыхания с последующей гипервентиляцией).
|
|
|


