 |
Итоговое занятие по теме «Буферные растворы. Электрохимия»
|
|
|
|
План занятия
1. Проверка посещаемости и информация
2. Решение ситуационных задач
3. Подведение итогов занятия
Ситуационные задачи
Задача 53.
Кривая кондуктометрического титрования 20 мл раствора смеси кислот 0,1 н раствором гидроксида натрия имеет следующий вид:
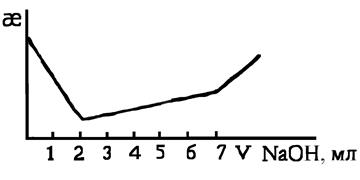
Вопрос: Чему равны концентрации сильной и слабой кислоты в растворе? Ответ обоснуйте.
Задача 54.
Кривая кондуктометрического титрования 20 мл раствора смеси кислот 0,1 н раствором гидроксида натрия имеет следующий вид:

Вопрос: Чему равны концентрации сильной и слабой кислоты в растворе? Ответ обоснуйте.
Задача 55.
Кривая кондуктометрического титрования 20 мл раствора смеси кислот 0,1 н раствором гидроксида натрия имеет следующий вид:
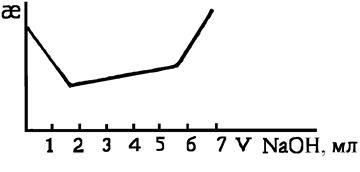
Вопрос: Чему равны концентрации сильной и слабой кислоты в растворе? Ответ обоснуйте.
Задача 56.
Водородный электрод погружен в раствор с рН = 0. Затем этот раствор нейтрализовали до рН = 7.
Вопрос: На сколько изменился потенциал водородного электрода? Ответ обоснуйте.
Задача 57.
Цинковый электрод погружен в раствор соли цинка. Затем этот раствор разбавили в 10 раз.
Вопрос: На сколько изменился потенциал цинкового электрода? Ответ обоснуйте.
Эталоны ответов НА ЗАДАНИЯ В ТЕСТОВОЙ ФОРМЕ
«ОСНОВНЫЕ ПОНЯТИЯ И ОПРЕДЕЛЕНИЯ
ХИМИЧЕСКОЙ ТЕРМОДИНАМИКИ. I ЗАКОН ТЕРМОДИНАМИКИ»
| № | Ответ | № | Ответ | № | Ответ |
| 1 | B | 11 | C | 21 | B |
| 2 | C | 12 | A | 22 | BC |
| 3 | B | 13 | A | 23 | B |
| 4 | B | 14 | B | 24 | AB |
| 5 | A | 15 | AC | 25 | C |
| 6 | C | 16 | C | 26 | AB |
| 7 | C | 17 | B | 27 | BC |
| 8 | A | 18 | C | 28 | BC |
| 9 | A | 19 | B | 29 | AC |
| 10 | B | 20 | A | 30 | C |
«II ЗАКОН ТЕРМОДИНАМИКИ.
КРИТЕРИИ САМОПРОИЗВОЛЬНОГО ПРОТЕКАНИЯ ПРОЦЕССА»
|
|
|
| № | Ответ | № | Ответ | № | Ответ |
| 1 | ACD | 11 | AD | 21 | B |
| 2 | D | 12 | AB | 22 | A |
| 3 | AD | 13 | D | 23 | A |
| 4 | B | 14 | C | 24 | B |
| 5 | ABC | 15 | D | 25 | C |
| 6 | BC | 16 | A | 26 | B |
| 7 | C | 17 | BD | 27 | D |
| 8 | B | 18 | ABDF | 28 | A |
| 9 | BC | 19 | AD | 29 | AB |
| 10 | B | 20 | BC | 30 | AB |
«ТЕРМОДИНАМИЧЕСКИЕ ПОТЕНЦИАЛЫ. ТЕРМОДИНАМИКА ХИМИЧЕСКОГО РАВНОВЕСИЯ»
| № | Ответ | № | Ответ | № | Ответ |
| 1 | B | 7 | A | 13 | C |
| 2 | C | 8 | C | 14 | AB |
| 3 | BD | 9 | D | 15 | AD |
| 4 | B | 10 | A | 16 | B |
| 5 | AD | 11 | B | 17 | BC |
| 6 | C | 12 | C | 18 | BC |
«ТЕРМОДИНАМИКА ФАЗОВЫХ РАВНОВЕСИЙ. ОСНОВНЫЕ ПОНЯТИЯ. ОДНОКОМПОНЕНТНЫЕ СИСТЕМЫ»
| № | Ответ | № | Ответ | № | Ответ |
| 1 | A | 13 | A | 25 | B |
| 2 | B | 14 | C | 26 | B |
| 3 | BC | 15 | B | 27 | C |
| 4 | BC | 16 | B | 28 | B |
| 5 | B | 17 | AB | 29 | C |
| 6 | AC | 18 | AC | 30 | A |
| 7 | BC | 19 | B | 31 | B |
| 8 | C | 20 | ABC | 32 | B |
| 9 | C | 21 | BC | 33 | B |
| 10 | B | 22 | A | 34 | C |
| 11 | B | 23 | BC | 35 | C |
| 12 | C | 24 | B | 36 | C |
«БУФЕРНЫЕ СИСТЕМЫ И РАСТВОРЫ»
| № | Ответ | № | Ответ | № | Ответ |
| 1 | C | 8 | B | 15 | D |
| 2 | B | 9 | A | 16 | A |
| 3 | A | 10 | C | 17 | B |
| 4 | A | 11 | B | 18 | B |
| 5 | AD | 12 | A | 19 | D |
| 6 | B | 13 | C | 20 | C |
| 7 | B | 14 | B |
«ТЕОРИЯ РАСТВОРОВ СИЛЬНЫХ ЭЛЕКТРОЛИТОВ ДЕБАЯ И ХЮККЕЛЯ»
| № | Ответ | № | Ответ | № | Ответ |
| 1 | B | 5 | C | 9 | B |
| 2 | C | 6 | B | 10 | A |
| 3 | A | 7 | A | 11 | B |
| 4 | A | 8 | B | 12 | A |
«ЭЛЕКТРОХИМИЯ»
| № | Ответ | № | Ответ | № | Ответ |
| 1 | C | 19 | A | 37 | B |
| 2 | C | 20 | D | 38 | AC |
| 3 | C | 21 | C | 39 | D |
| 4 | B | 22 | D | 40 | B |
| 5 | A | 23 | C | 41 | C |
| 6 | A | 24 | B | 42 | C |
| 7 | A | 25 | D | 43 | AC |
| 8 | A | 26 | A | 44 | CD |
| 9 | B | 27 | A | 45 | BCD |
| 10 | C | 28 | C | 46 | D |
| 11 | B | 29 | AC | 47 | BC |
| 12 | B | 30 | A | 48 | A |
| 13 | B | 31 | D | 49 | AB |
| 14 | A | 32 | C | 50 | D |
| 15 | D | 33 | A | 51 | ACD |
| 16 | B | 34 | B | 52 | B |
| 17 | B | 35 | A | 53 | AB |
| 18 | D | 36 | CD | 54 | BCD |
ЛИТЕРАТУРА
а). Основная литература:
1. Физическая и коллоидная химия [Текст]: учеб. пособие для вузов / А.П. Беляева [и др.]. - М., ГЭОТАР – Медиа, 2010. – 300 с.
б). Дополнительная литература:
1. Жолнин А.В. Общая химия [Текст] / А.В. Жолнин. - ГЭОТАР – Медиа, 2012. – 350 c.
ПРИЛОЖЕНИЕ 1
ТЕРМОДИНАМИЧЕСКИЕ ВЕЛИЧИНЫ
| ВЕЩЕСТВО | ∆Н0f, 298 кДж/моль | S0298, Дж/моль•К | ∆G0f,298, кДж/моль | С0р, Дж/моль•К |
ПРОСТЫЕ ВЕЩЕСТВА
|
|
|
НЕОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
УГЛЕВОДОРОДЫ
КИСЛОРОДСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
ГАЛОГЕНСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
|
|
|


