 |
Тема 6.1. Законы идеальных газов. Уравнение состояния идеальных газов.
|
|
|
|
I. Цель практического занятия:
- Закрепить и углубить знания основных законов идеальных газов.
- Учиться применять полученные знания для решения задач по данной теме.
II. Расчёт учебного времени:
| Содержание занятия | Время (мин.) |
Вступительная часть:
Объявление темы и цели занятия.
Контрольный опрос:
|
Контрольный опрос
1. Закон Бойля-Мариотта: для постоянной массы газа при неизменной температуре: 
2. Законы Гей-Люссака:
а) Для постоянной массы газа при неизменном давлении: 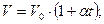
 -объём при температуре t=0° С и
-объём при температуре t=0° С и  или
или 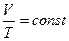
б) Для постоянной массы газа при неизменном объёме: 
Р0 - давление при t=0° С. Или 
3. Закон Дальтона для давления смеси n идеальных газов: 
4. Уравнение состояния идеального газа:  -уравнение Менделеева-Клапейрона.
-уравнение Менделеева-Клапейрона.  - другая форма уравнения состояния идеального газа.
- другая форма уравнения состояния идеального газа.
5. Основное уравнение М.К.Т. идеальных газов: 
 , Е – суммарная кинетическая энергия поступательного движения всех молекул газа.
, Е – суммарная кинетическая энергия поступательного движения всех молекул газа.
6. Формула средней квадратичной скорости молекул газа: 
Основная часть
Пример №1 Чер.№ 9.4
В баллоне объёмом V =5 л содержится кислород массой m =20 г. Определить концентрацию n молекул в баллоне.
|
|
|
Дано:

| Решение:


|
| n-? |
Пример №2 Тр.№ 2.3
В закрытом сосуде вместимостью 20 л находятся водород массой 6 г и гелий массой 12 г. Определить: 1)давление; 2)молярную массу газовой смеси в сосуде, если температура смеси Т =300 К.
Дано:

| Решение:
Согласно закону Дальтона:
  .
Из уравнения Менделеева-Клапейрона для смеси: .
Из уравнения Менделеева-Клапейрона для смеси:
  Тогда:
Тогда: 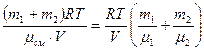 и и 
|

|
Пример №3 Тр.№2.5
В баллоне вместимостью 15 л находится азот под давлением 100 кПа при температуре t1 =27°С. После того как из баллона выпустили азот массой 14 г, температура газа стала равной t2 =17°С. Определить давление азота, оставшегося в баллоне.
Дано:

| Решение:
Из уравнения Менделеева для первого состояния газа: 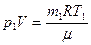 Найдём первоначальную массу газа:
Найдём первоначальную массу газа:  Из уравнения Менделеева для второго состояния:
Из уравнения Менделеева для второго состояния:  , учитывая, что , учитывая, что  , найдём давления газа , найдём давления газа 

|
| р2-? |
Пример №4 Тр.№2.7
Азот массой 7 г находится под давлением p =0,1 МПа и температуре Т1 =290 К. Вследствие изобарного нагревания азот занял объём V2 =10 л. Определить: 1)объём V1 газа до расширения; 2)температуру Т2 газа после расширения; 3) плотности газа до и после расширения.
Дано:

| Решение:
Из уравнения М.-К. для первого состояния газа:  , найдём первоначальный объём газа: , найдём первоначальный объём газа:  Так как с газом происходит изобарный процесс, то:
Так как с газом происходит изобарный процесс, то:  , поэтому , поэтому  .
Плотность газа можно найти из уравнения М.-К., учитывая, что .
Плотность газа можно найти из уравнения М.-К., учитывая, что   , тогда , тогда 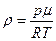 .
Плотность газа в первом и втором состоянии соответственно: .
Плотность газа в первом и втором состоянии соответственно:
 и и 
|

|
Пример №5 Тр.№2.9
В сосуде вместимостью 5 л при нормальных условиях находится азот. Определить: 1)количество вещества v; 2)массу азота; 3)концентрацию n его молекул в сосуде.
Дано:

| Решение:
Из уравнения Менделеева- Клапейрона:

|

|
Пример №6 Тр.2.11
В сосуде вместимостью V =0,3 л при температуре Т =290 К находится некоторый газ. На сколько понизится давление р газа в сосуде, если из него из-за утечки выйдет N =1019 молекул.
|
|
|
Дано:

| Решение:
Используем уравнение состояния идеального газа: 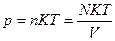 Для первого и второго состояний:
Для первого и второго состояний:  и и 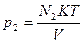 .
Вычтем из второго уравнения первое: .
Вычтем из второго уравнения первое:  ,
таким образом ,
таким образом 
|

|
Пример №7 Тр.№2.10
Средняя квадратичная скорость некоторого газа при нормальных условиях равна 480 м/с. Сколько молекул содержит 1 г этого газа.
Дано:

| Решение:
Число молекул газа  , где , где  -масса одной молекулы. Используя формулу средней квадратичной скорости: -масса одной молекулы. Используя формулу средней квадратичной скорости:  Найдём
Найдём  , тогда , тогда 
|
| N-? |
Пример №8 Тр.№2.14
Определить среднюю кинетическую энергию  поступательного движения молекул газа, находящегося под давлением 0,1 Па. Концентрация молекул газа равна 1013см-3.
поступательного движения молекул газа, находящегося под давлением 0,1 Па. Концентрация молекул газа равна 1013см-3.
Дано:

| Решение:
Так как 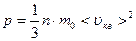 и и  , то , то  Поэтому
Поэтому 
|

|
Пример №9 Тр№2.12
Определить давление, оказываемое газом на стенки сосуда, если его плотность равна 0,01 кг/м3, а средняя квадратичная скорость молекул газа составляет 480 м/с.
Дано:

| Решение:
Используем формулу средней квадратичной скорости: 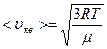 Из уравнения М.-К.:
Из уравнения М.-К.:  ,
учитывая, что ,
учитывая, что  : :  ; ;  .
Тогда: .
Тогда:  и и 
|
| р-? |
Пример №10 Чер.№8.22
В баллонах объёмом V1 =20 л и V2 =44 л содержится газ. Давление в первом баллоне р1 =2,4 МПа, во втором – р2 =1,6 МПа. Определить общее давление р и парциальное  и
и  после соединения баллонов, если температура газов осталась прежней.
после соединения баллонов, если температура газов осталась прежней.
Дано:

| Решение:
Так как температура не изменяется то с газами происходит изотермический процесс:
 и и
 По закону Дальтона установившееся давление после соединения сосудов:
По закону Дальтона установившееся давление после соединения сосудов: 
|

|
Пример №11 Чер.№8.3
В U-образный манометр налита ртуть. Открытое колено манометра соединено с окружающим пространством при нормальном атмосферном давлении р0 и ртуть в открытом колене стоит выше, чем в закрытом, на  =10 см. При этом свободная от ртути часть трубки закрытого колена имеет длину l =20 см. Когда открытое колено присоединили к баллону с воздухом, разность уровней ртути увеличилась и достигла
=10 см. При этом свободная от ртути часть трубки закрытого колена имеет длину l =20 см. Когда открытое колено присоединили к баллону с воздухом, разность уровней ртути увеличилась и достигла  =26 см. Найти давление р воздуха в баллоне.
=26 см. Найти давление р воздуха в баллоне.
Дано:
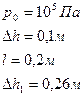
| Решение:
С газом находящемся в запаянном конце трубки происходит изотермический процесс:




|
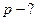
|
Пример №12 Волькенштейн №5.63
При какой температуре средняя кинетическая энергия теплового движения атомов гелия будет достаточна для того, чтобы атомы гелия преодолели земное тяготение и навсегда покинули земную атмосферу? Решить аналогично задачу для Луны.
|
|
|
Дано:

| Решение:
Для средней квадратичной скорости:  Чтобы атом гелия покинул земную атмосферу необходимо:
Чтобы атом гелия покинул земную атмосферу необходимо:
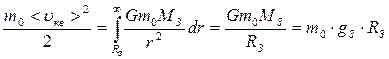 Тогда:
Тогда:  и и  ; ; 
|
| Т-? |
Заключительная часть
- Подводятся итоги занятия
- Задаётся задание на самостоятельную работу по пройденной теме:
Т.И.Трофимова «Сборник задач по курсу физики» № 2.4; 2.6; 2.8; 2.13.
- Объявляется тема следующего занятия.
|
|
|


