 |
Диагностические критерии узелкового периартериита
|
|
|
|
1. Похудание >4 кг с начала заболевания, не связанное с особенностями питания.
2. Сетчатое ливедо (ветвистое изменение рисунка кожи на конечностях и туловище).
3. Болезненность в яичках, не связанная с инфекцией, травмой и т.п.
4. Миалгии (исключая плечевой пояс или поясничную область), слабость или болезненность в мышцах нижних конечностей.
5. Мононеврит или полинейропатия.
6. Диастолическое давление >90 мм рт. ст.
7. Повышение уровня мочевины >14,4 ммоль/л (40 мг%) или креатинина >133 ммоль/л (1,5 мг%) в крови, не связанное с дегвдратацией или обструкцией мочевыводящих путей.
8. Наличие поверхностного антигена вируса гепатита В или антител к нему в сыворотке крови.
9. Аневризмы или окклюзии висцеральных артерий при ангиографии, не связанные с атеросклерозом, фибромышечной дисплазией и другими невоспалительными заболеваниями.
10. Обнаружение в биоптате мелких и средних артерий гранулоцитарной и мононуклеарноклеточной инфильтрации стенки сосуда.
Наличие трех и более критериев позволяет поставить диагноз УП.
Диагностические критерии УП, (Н.П. Шилкиной), представлены в таблице 4.
Таблица 4
Диагностические критерии, разработанные Н.П. Шилкиной
| Критерии | Определение | Балл |
| 1. Сетчатое ливедо | Пятнисто-сетчатый рисунок на коже конечностей или туловища | |
| 2. Узелки по ходу сосудов | Кожные или подкожные узелки (аневризматически измененные артерии), определяемые при пальпации, располагающиеся по ходу сосудистого пучка, чаще на конечностях | |
| 3. Астма | Эпизоды удушья в анамнезе или диффузные свистящие хрипы на выдохе | |
| 4. Аллергия в анамнезе и/или эозинофилия | Сезонная аллергия в анамнезе или другая документированная аллергия, включая пищевую, контактную, исключая лекарственную, и/или эозинофилия >10% | |
| 5. Артериальная гипертензия | Развитие артериальной гипертензии с уровнем диастолического давления >90 мм рт. ст. | |
| 6. Миалгии | Диффузные миалгии, исключая поражение плечевого и тазового пояса, слабость или болезненность мышц нижних конечностей | |
| 7. Полиневрит асимметричный | Полинейропатия, характеризующаяся значимой асимметричностью клинических и/или электрофизиологиче ских показателей | |
| 8. Биопсия: некротизирующие васкулиты | Гистологические изменения, свидетельствующие о некротизирующем васкулите с преобладанием нейтрофильных гранулоцитов в стенке сосуда |
|
|
|
5 балов и более при наличии биопсии позволяют поставить достоверный диагноз УП;
6 - 7 балов - вероятный УП без морфологического подтверждения.
Прогноз, несмотря на значительный прогресс в лечении, остаётся сомнительным. Он зависит главным образом от тяжести поражения почек и артериальной гипертензии, а также желудочно-кишечных осложнений.
МИКРОСКОПИЧЕСКИЙ ПОЛИАНГИИТ
Микроскопический полиангиит - гипоиммунный некротизирующий системный васкулит с преимущественным поражением микроциркуляторноп русла (артериол, капилляров и венул), ассоциированный с антинейтрофильными цитоплазматическими антителами.
Впервые заболевание было описано в 1948 г. как особая форма УП протекающая с некротизирующим гломерулонефритом. Мужчины болеют чаще, чем женщины, средний возраст начала заболевания составляет 50 лет.
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ
Этиология MПA не изучена. Развитие некротизирующего васкулита и гломерулонефрита при МПА обусловлено синтезом аутоантител к различным цитоплазматическим компонентам нейтрофилов (АНЦА). При МПА данные антитела имеют высокую специфичность к миелопероксидазе (перинуклеарное свечение) и реже реагируют с протеиназой-3 (цитоплазматическое свечение). В активную фазу болезни АНЦА обнаруживаются практически у 100% больных.
|
|
|
ПАТОМОРФОЛОГИЯ
При высокой степени активности васкулита поражение сосудистой стенки развивается быстро и проявляется фибриноидными изменениями, а также деструктивным и деструктивно-продуктивным васкулитом.
Выделяют три стадии фибриноидного некроза.
1. стадия характеризуется пропитыванием тканей белками плазмы, реакция на фибриноид на данной стадии отрицательная.
2. стадия - по мере повышения проницаемости сосудистой стенки в ткани начинает попадать фибриноген, который откладывается в виде фибрина.
3. стадия - некроз пропитанных фибрином коллагеновых волокон (фибриноидный некроз).
Фибриноидый некроз может быть сегментарным (поражается часть окружности сосуда), кольцевидным (с охватом сосуда по периметру), а также может распространяться на всю толщину сосудистой стенки. В случае, когда фибриноидный некроз поражает все слои сосудистой стенки и переходит на периадвентициальную соединительную ткань, речь идет о деструктивном васкулите.
Обычно к фибриноидным изменениям стенок сосудов присоединяется клеточная реакция различной степени выраженности. Инфильтрат может состоять из лимфоцитов, плазмоцитов, макрофагов, нейтрофилов и эозинофилов, выявляются единичные эпителиоидные клетки. В адвентиции и периваскулярной ткани инфильтрат более выражен. Если инфильтрация и фибриноидный некроз выражены в равной степени, речь идет о деструктивно-продуктивном васкулите.
При низкой степени активности заболевания на первый план выступает продуктивно-инфильтративная реакция. Клетки воспалительного инфильтрата не отличаются от таковых при деструктивном васкулите и представляют собой лимфоциты, нейтрофилы, фиброциты и эозинофилы.
По локализации инфильтрата васкулит подразделяется на эндо-, мезо-, пери- и панартериит. На практике же чаще всего встречается панартериит.
При иммуногистохимическом исследовании биоптатов кожно-мышечного лоскута было выяснено, что 40% инфильтрата составляют Т-лимфоциты (в основном СD4-клетки), 40% составляют макрофаги. Нейтрофилы составляют от 0 до 45% и обнаруживаются в основном в сосудах с ярко выраженной инфильтрацией и фибриноидным некрозом.
|
|
|
КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ
Клинические проявления МПА весьма схожи с такими при УП, но отличаются по распространенности повреждений циркуляторного русла. Основное отличие МПА в отсутствии поражений сосудов среднего калибра.
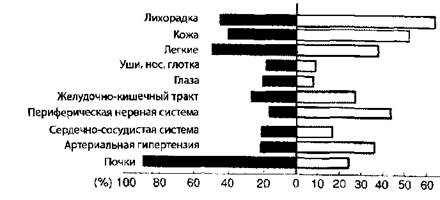


МИКРОСКОПИЧЕСКИЙ ПОЛИАНГИИТ УЗЕЛКОВЫЙ ПОЛИАРТЕРИИТ
Рис. 2. Частота поражения органов и систем при узелковом полиартериите и микроскопическом полиангиите
Поражение кожи. Частота поражения кожи колеблется от 40 до 60% (рис. 7). Спектр клинических проявлений включает в себя пурпуру, локализующуюся на нижних конечностях, болезненные красные узлы и сетчатое ливедо. Перечисленные поражения могут трансформироваться в язвы, скорость их заживления зависит от эффективности лечения васкулита.
Кроме того, у больных может наблюдаться крапивница, которая имеет свои особенности по сравнению с обычной аллергической крапивницей:
1. продолжительность высыпаний в течение дня и более;
2. возможность трансформации крапивницы в пурпуру;
3. гипокомплементемия.
Поражение суставов. Частота вовлечения в патологический процесс суставов при МПА составляет около 50%. Примерно в 25% случаев у больных МПА наблюдается транзиторный артрит крупных суставов (локтевых, коленных, голеностопных).
Поражение мышц встречается с такой же частотой, что и поражение суставов, и характеризуется развитием миозита.
Среди вариантов поражения сердечно-сосудистой системы встречается коронариит, приводящий к развитию стенокардии и инфаркта миокарда.
Частота поражения желудочно-кишечного тракта достигает 40%. Пациенты жалуются на боль в животе, диарею и тошноту. При проведении ФГДС обнаруживают язвы различных отделов пищеварительного тракта, нередко осложняющиеся перфорацией и кровотечением. Частота встречаемости холецистита, аппендицита и панкреатита при МПА не отличается от их распространенности в общей популяции.
Поражение ЦНС не характерно для МПА. У больных МПА на первый план выступает поражение периферической нервной системы в виде множественных мононевритов (вовлечение в воспалительный процесс чувствительных и двигательных нервов), которые обусловлены васкулитом эпиневральных сосудов. Описаны случаи поражения белого вещества головного мозга при МПА.
|
|
|
Поражение глаз у больных МПА встречается примерно в 20% случаев. Могут развиваться эписклерит, склерит, кератит, увеит и васкулит сетчатки. Наиболее лёгким из вышеперечисленных поражений считается эписклерит, который проявляется минимальным дискомфортом и, как правило, не угрожает потерей зрения.
Склерит и кератит - наиболее тяжелые поражения глаз при МПА, проявляются сильными болями с иррадиацией в голову. Описаны случаи, когда тяжело протекавшие кератит и склерит приводили к потере зрения и вызывали разрушение глазного яблока. Необходимо отметить, что кератит и склерит могут встречаться у одного и того же больного. Если кератит развивается изолированно, он чаще начинается в варианте периферического язвенного кератита. У больных МПА нередко развивается промежуточный и задний увеит.
Поражение почек типично для МПА и по частоте встречаемости у больных достигает 100%. Ряд авторов отмечает, что нефропатия при МПА в сравнении с ГрВ имеет худший прогноз. Поражение почек - основная черта МПА, характеризуется развитием фокально-сегментарного гломерулонефрита (так называемого «гломерулонеф- рита с полулуниями»). Данная форма гломерулонефрита имеет крайне неблагоприятный прогноз.
МПА может развиваться со скудной клинической симптоматикой до появления выраженных симптомов поражения почек, так что при биопсии обнаруживаются как активные гломерулярные повреждения, так и признаки склероза. Экстракапиллярная пролиферация ведет к образованию полулу ний в более 60% клубочков.
В целом гистологические изменения в почках при МПА соответствуют таковым при некротизирующем гломерулонефрите. При МПА гломерулонефрит достаточно быстро осложняется формированием ХПН или нефротическим синдромом (отеки, гипопротеинемия, гиперпротеинурия, гиперхолестеринемия). Последний является прогностически неблагоприятным признаком заболевания и требует интенсификации лечения. В некоторых случаях встречается васкулит сосудов стенки мочеточников или периуретральной клетчатки, что ведет к стенозу мочеточников. Клинически эта патология характеризуется болями в животе и развитием анурии, в некоторых случаях возможно бессимптомное течение.
Частота поражения легких при МПА составляет 10 -30%. Клинически поражение лёгких проявляется кашлем (20%), кровохарканьем (10%), болями при дыхании вследствие плеврита (10%), а также одышкой, обусловленной фиброзом легочной ткани в результате рубцевания очагов воспаления.
|
|
|
При рентгеновском исследовании в легочной ткани выявляются инфильтраты, не имеющие склонности к распаду (в отличие от таковых при гранулематозных васкулитах).
Иногда поражение легких клинически может протекать бессимптомно и выявляется только при проведении рентгеновского обследования.
ДИАГНОСТИКА
У больных МПА выявляется умеренная гипохромная анемия, лейкоцитоз, нейтрофи-лез, ускорение СОЭ, повышение СРБ, снижение концентрации компонентов комплемента (СЗ и С4). При поражении почек наблюдается повышение креатинина и мочевины, микрогематурия, протеинурия.
МПА относится к АНЦА-ассоциированным СВ, в связи с чем у больных МПА выявляется достоверное повышение уровня АНЦА к миелопероксидазе, реже к ПР-3.
Высокие титры АНЦА определяются при МПА с быстро прогрессирующим гломерулонефритом даже при отсутствии нефротического синдрома и прогрессирования почечной недостаточности.
Повышение уровня неоптерина характерно для активной фазы заболевания и коррелирует с индексом клинической активности МПА.
Прогноз во многом определяется степенью вовлечения в патологический процесс почек и развитием почечной недостаточности, хотя причинами смерти больных МПА могут стать массивные лёгочные кровотечения, а также инфекционные осложнения, возникающие на фоне проводимой иммуносупрессивной терапии.
ГРАНУЛЕМАТОЗ ВЕГЕНЕРА
Гранулематоз Вегенера - это системный гранулематозный заскулит с поражением сосудов мелкого и среднего калибра.
ЭТИОЛОГИЯ
Этиологические факторы, вызывающие ГрВ, неизвестны. По данным ряда авторов, пик развития ГрВ приходится на весенний период, что косвенно может отражать участие вирусных инфекций в этиологии заболевания. Описан больной с системной цитомегаловирусной инфекцией, у которого развился ГрВ. Т. Finkel и соавт. в 1992 г. с помощью полимеразной цепной реакции обнаружили присутствие парвовирусной инфекции у двух больных ГрВ. Однако другие исследователи не отмечали сезонных колебаний заболеваемости ГрВ и связи между инфекцией и ГрВ.
В то же время имеются данные о том, что инфицирование золотистым стафилококком является способствующим фактором обострения данного заболевания. Результаты иммунологического анализа выявили определенную ассоциацию HLA-B7, -В8 и DR2, а также DQW7 и DR4 с риском развития ГрВ.
КЛИНИЧЕСКАЯ КАРТИНА
В клинической картине ГрВ на первый план выступают поражения респираторного тракта и почек.
Нередко обращает внимание последовательное поражение верхних дыхательных путей с вовлечением придаточных пазух носа, перфорацией носовой перегородки и седловидной деформацией носа, поражение трахеи, гортани, легких, а также формирование быстропрогрессирующего гломерулонефрита и некротизирующего васкулита с поражением глаз, суставов, периферических нервов.
Описаны клинические случаи, когда у больных ГрВ не наблюдались характерные поражения легких и верхних дыхательных путей, но выявлялись тяжелые поражения желудочно-кищечного тракта с развитием язвенно-некротических изменений кишечника с перфорацией и развитием перитонита. Имеются наблюдения, свидетельствующие об отсутствии у больных ГрВ признаков СВ, что выделяет такие формы в особые варианты данного заболевания.
Поражения кожи. При ГрВ частота поражений кожи составляет 13 - 50%. При этом они весьма похожи на таковые при УП и МПА и проявляются в виде пурпуры, локализующейся преимущественно на нижних конечностях, в виде гранулем и крапивницы.
Поражения суставов и мышц при ГрВ выявляются у 70% больных и характеризуются артралгиями и артритами крупных суставов. Нередко у данной категории пациентов развиваются миалгии или миозит.
Поражение сердечно-сосудистой системы. Частота поражения сердца при ГрВ составляет приблизительно 40%. Во многих случаях выявляется экссудативный перикардит, реже - коронарит, проявляющийся стенокардитическими болями, и миокардит, на фоне которого могут развиваться тяжелые нарушения ритма и проводимости вплоть до AVблокады, требующей постановки водителя ритма. На фоне ГрВ может развиваться недостаточность аортального или митрального клапана, а также митральный стеноз. В литературе имеются немногочисленные сведения о поражении аорты в виде проксимальной дилатации, склерозирования стенок и расширений нисходящего отдела аорты.
Поражение желудочно-кишечного тракта. Поражение желудочно- кишечного тракта при ГрВ встречается примерно в 40% случаев. В качестве клинических проявлений описаны поражения толстой и тонкой кишки, манифестирующие болями в животе, перфорацией и кровотечением. Нередко у больных развивается эрозивный эзофагит. Встречаются поражения ротовой полости в виде гиперпластического гингивита и изъязвления перианальной области, а также стенозы гортани, требующие постановки постоянной трахеостомы.
Поражение ЦНС. Наблюдаются поражения как центральной, так и периферической нервной системы. Со стороны ЦНС наблюдаются острые нарушения мозгового кровообращения, образование субарахноидальных и субдуральных гематом, эпилепсия. Поражение спинного мозга встречается редко. Наблюдаются случаи поражения черепно-мозговых нервов (II, VI, VII пары). Большинство клиницистов отмечает, что периферическая полинейропатия и множественные мононевриты у больных ГрВ встречаются чаще, чем поражения ЦНС.
Поражение глаз при ГрВ встречается чаще, чем при узелковом полиартериите и микроскопическом полиангиите и диагностируется у 15 - 58% больных. Характерно развитие проптоза, который наблюдается в 25% случаев и связан с воспалительными и фиброзными изменениями ретробульбарного пространства, что может приводить к потере зрения вследствие ишемии п. opticus. Описаны случаи прорастания гранулемы в глазные яблоки с потерей зрения.
Поражение дыхательных путей. Частота поражения верхних отделов дыхательных путей при ГрВ достигает 70%, нижних - примерно 50% случаев. Выявляются хронический синусит (встречается у 80% больных), изъязвления слизистой носа с перфорацией или разрушением перегородки и образованием «седловидного носа», хронический ларинготрахеит, который может привести к стенозу трахеи и тяжелым нарушениям дыхания, а также рецидивирующие инфильтраты в легких, склонные к распаду.
Поражение почек. При ГрВ часто встречается фокально-сегментарный гломерулонефрит (20 - 80% случаев), возможно развитие мембранозно- пролиферативного гломерулонефрита, инфарктов почек. Нередко нефропатия при ГрВ осложняется нефротическим синдромом.
ДИАГНОСТИКА
Диагностика ГрВ основывается в первую очередь на его клинических проявлениях. Лабораторные показатели не специфичны. Обращает на себя внимание нормохромная анемия, лейкоцитоз, тромбоцитоз, ускорение СОЭ. Отмечается положительная корреляционная связь между уровнем СРБ и индексом клинической активности васкулита. Уровень иммунных комплексов нередко остаётся в пределах нормы. Гипокомплементемия для ГрВ не характерна.
Особое значение для диагностики ГрВ имеют АНЦА. На основе современных данных можно отметить связь между высоким уровнем АНЦА и обострением гломерулонефрита у больных ГрВ. Высокие титры АНЦА определяются практически у большинства пациентов с ГрВ, при этом часто наблюдаются такие клинические проявления, как лихорадка, суставной синдром, поражение легких, глаз, кожный васкулит, язвенно-некротический ринит. Установлена прямая зависимость между уровнем АНЦА и СОЭ, содержанием СРБ, РФ и IgM. При динамическом наблюдении выявляется зависимость уровня АНЦА в сыворотке крови от течения ГрВ. Так, при обострении заболевания они значительно увеличиваются, а во время ремиссии значительно снижаются. Для стадии обострения ГрВ также характерно повышение фактора Виллебранда, содержание которого не связано с повышением АНЦА. При активной фазе течения заболевания наблюдается повышение уровня сывороточного неоптерина, СОЭ и СРБ.
Таким образом, определение АНЦА и неоптерина позволяет более адекватно оценивать активность течения ГрВ, чем использование рутинных биохимических показателей. Данные критерии активности васкулита имеют преимущества перед такими лабораторными маркерами воспаления, как СОЭ, СРБ и фибриноген.
Патоморфология характеризуется наличием гранулем и признаками некротического васкулита. Полная триада из гранулем, васкулита и некроза встречается примерно в половине случаев заболевания. Отсутствие данной морфологической триады не исключает диагноз ГрВ. При биопсии тканей больных ГрВ выявляется деструктивно-продуктивный васкулит, полиморфноклеточные гранулемы с наличием многоядерных гигантских клеток Лангханса, плазматических клеток, лимфоцитов и эозинофилов, очаги фибриноидного некроза с деструкцией стенок артерий среднего и мелкого калибра, а также вен. Субэпителиально располагаются иммунные депозиты. Клеточный состав гранулем различной давности не одинаков. Во вновь образованных гранулемах основную массу составляют лимфоциты, гистиоциты и нейтрофилы, а в зрелых - клетки фибробластического ряда и плазмоциты.
Выявлено два механизма развития некроза. В первом случае некроз развивается по типу распространённого микроабсцедирования. Сначала скапливаются нейтрофилы, окруженные палисадовидными гистиоцитами, фокусы постепенно увеличиваются и становятся базофильными, формируются очаги некроза, напоминающие географическую карту. Обычно такие очаги некроза окружены гистиоцитами и гигантскими клетками (типа клеток Лангханса). Для второго варианта некротического процесса характерно разрушение коллагена, который имеет равномерное или неравноме распределение в участках развития патологического процесса.
Распад гранулем с образованием некроза характерен для органов, контактирующих с внешней средой. В органах же, не имеющих прямой связи с внешней средой (печень, почки), гранулемы склонны к рубцеванию. Показано, что в гранулемах, которые склонны к распаду, содержится мало фибробластов, в то время как рубцующиеся гранулемы содержат большое количество клеток Лангханса и фибробластов.
Морфологические особенности воспаления при ГрВ:
1. гранулематозный характер поражения как гранулематозная периваскулярная инфильтрация, а не сумма отдельных гранулем.
2. полиморфизм гигантских многоядерных клеток и бессистемность локализации в гранулематозной ткани.
3. сочетание мелкоочаговых некрозов иммунопатологического происхождения с массивными некрозами ишемического типа.
4. сосуществование очагов сухого коагуляционного некроза с влажным колликвационным.
Классификационные критерии гранулематоза Вегенера Американской ассоциации ревматологов представлены в таблице 5.
Таблица 5
|
|
|


